Dijabetesna retinopatija
| Dijabetesna retinopatija | |
|---|---|
 | |
| Klasifikacija i spoljašnji resursi | |
| Specijalnost | oftalmologija endokrinologija |
Dijabetesna retinopatija, bolest mrežnjače u šećernoj bolesti (DR) (lat. Retinopathia diabetica) jedna je od komplikacija šećerne bolesti koja dovodi do oštećenja mreže kapilara koja krvlju snabdeva mrežnjaču oka.
Histopatološke promene u dijabetesnoj retinopatije rezultat su mikrovaskularnih disfunkcija mrežnjače nastale u okruženju sistemske hiperglikemije. Histološke promene koje se javljaju pre nego što bolest postane klinički manifestna obuhvataju osipanje i zadebljanja pericita vaskularne bazalne membrane. Najraniji klinički nalaz je pojava mikroaneurzmatskih formacija, koje su odraz preproliferative promena. Ostale promene u mrežnjače uključuju preproliferativni edem žute mrlje, meki eksudat, trdi eksudat, krvarenja unutar mrežnjače i abnormalnosti veličine venskih kapilara (vensko izvlačenje i dilatacija). Proliferativne promene u DR odigravaju se zbog nametnutih preproliferativnih promenama i obuhvataju vaskularizaciju i proliferaciju fibroznog tkiva u preretinalnom prostoru, na periferiji i šupljini staklastog tela. Najverovatnije je da su navedene morfološke promene u DR uslovljene interakcijom brojnih faktora koji dovode do promena genske ekspresije i funkcije proteina u okruženju sistemske hiperglikemije.[1][2][3][4]
Bolest se manifestuje promenama na očnom dnu koje su praćene padom oštrine vida, a u najtežim slučajevima i trajnim gubitkom vida.[5] Dijabetesna retinopatija je ne samo učestala već i podmukla komplikacija šećerne bolesti najčešće bez ranih simptoma, koji i kada se pojave zahtevaju kompikovano lečenje koje je ne tako često bezuspešno i najčešće završava slepilom.[6]
Kako se kod velikog broja bolesnika sa šećernom bolešću može sprečiti progresija DR, dobro organizovan i pravovremeni skrining (rano otkrivanje) retinopatije od velike je važnosti, za uspešno lečenje i prevenciju slepila.[7] U tom smislu kod bolesnika sa tipom 1 šećerne bolesti: oftalmološki ili optometrijski pregled započinje u prvih 5 godina nakon postavljene dijagnoze a kod bolesnika sa tipom 2 šećerne bolseti: čim se dijagnoza postavi. Zatim se kod obe grupe bolesnika kontrolni oftalmološki ili optometrijske pregled vrše svake 1 do 2 godine u zavisnosti od stanja mrežnjače.[8]
Kod 100% osoba sa šećernom bolešću, tokom bolesti, razviće se neki vid, više ili manje, izražene retinopatije. Zato se može reći da je dijabetesna retinopatija ozbiljan, ne samo medicinski već i socio-ekonomski problem društva, kao najčešći uzrok slepila kod radno sposobne populacije starosti od 20 do 65 godina. To potkrepljuje i podatak da se i do 25 puta češće javlja kod bolesnika sa šećernom bolešću, nego kod opšte populacije, sa npr incidncom od 50 do 65 na 100.000 bolesnika sa šećernom bolešću godišnje u Evropi.[9]
Istorija[uredi | uredi izvor]
Najraniji poznati pisani zapis o šećernoj bolesti potiču, najverovatnije iz ranog 6. veka p. n. e., od indijskog lekara Maharišija Sušrute koji je bolest opisao kao stanje sa „medenom mokraćom“. Sušruta je u svom, sanskritskim jezikom napisanom, delu Sušruta Samhita opisao 76 očnih bolesti (od kojih 51 hirurških), kao i nekoliko oftalmoloških hirurških instrumenta i tehnika.[10][11]
Opisi šećerne bolesti takođe se pojavljuje u ranim egipatskim zapisima, a grčki lekari objavili su podatke o grčevima u mišićima udova praćenim promenama u mokraći, sličnim današnjim opisima simptoma kod šećerne bolesti. Komplikacije u šećernoj bolesti, kao što su slepilo i druge bolesti oka, malo su opisane kroz istoriju medicine, jer su verovatno takvi slučajevi bili retki, zbog relativno kratkog životnog veka bolesnika nakon razvoj šećerne bolesti.
Herman fon Helmholc (1821—1894) i Ernst Abe (1840—1905), suvlasnik fabrike Cajs u Nemačkoj, značajno su doprineli mnogim oblastima nauke. Fon Helmholc je prvi konstruisao oftalmoskop 1851. što je lekarima omogućilo proučavanje patoloških promena u unutrašnjosti oka, uključujući i one kod dijabetesne retinopatije.
Dijabetesnu retinopatiju prvi je opisao fon Jager Bajtrag 1855. godine.[12] U početku, promene na očnom dnu tumačene su kao posledica hipertenzije koja je dosta često udružena sa šećernom bolešću, a retinopatija kod dijabetičara je objašnjavana kao inflamatorni odgovor mrežnjače na povišeni nivo albumina i uree. Nešto kasnije, utvrđeno je postojanje veze između šećerne bolesti i vaskularnih promena u mrežnjači. I pored ovih otkrića, dijabetesna retinopatija je duži vremenski period bila relativno retka komplikacija u šećernoj bolesti.
Otkriće insulina od strane Ser Frederik Grant Banting i Čarls Herbert Besta 1921. unelo je revoluciju u lečenje šećerne bolesti i značajno produžilo život osoba sa ovom bolešću. Banting, Best i saradnici (posebno hemičar Kolip) uspeli su da izoluju insulin iz pankreasa govečeta na Univerzitetu u Torontu, što je 1922. godine omogućilo njegovu masovnu primenu u terapiji šećerne bolesti. Godinu dana kasnije, Banting i direktor laboratorije Maklaud za ovo otkriće su dobili Nobelovu nagradu.[13]
Nehumano zvuči, ali povećana „dugovečnost bolesnika“ nakon masovne prinmene insulina obezbedila je bolesnicima sa šećernom bolešću „da imaju više vremena“ za razvoj kasnih komplikacija kao što je retinopatija i slepilo. Gubitak vida i slepilo kod dijabetesne retinopatije tako je postao jedan od vodećih i sve većih problema u oftalmologiji, a njeno lečenje je u prvoj polovini 20. veka bilo bezuspešno.
Na direktan odnos između nivoa šećera u krvi i dijabetesne retinopatija posumnjalo se početkom 20. veka ali dugo ta sumnja nije dokazana ili bar univerzalno prihvaćena. Dok je deo oftalmologa tvrdio da šećerna bolest ima primarni efekat na bazalnu membranu krvnih sudova nezavisno od nivoa glukoze u krvi,[14] drugi su čvrsto verovali da kontrola nivoa glukoze u krvi usporava napredovanje vaskularnih promena u mrežnjači. Tek kada su razvijeni aparati, koje su pacijenti mogli da koriste za proveru nivo šećera u krvi, u više navrata tokom dana, omogućena je intenzivna preventivna kontrola nivoa glukoze u krvi. Brojne kliničke studije s kraja 20. veka dokazale su da su redovnom kontrolom glukoze stvoreni uslovi za dobru glukoregulaciju u krvi što je sprečilo ili bar usporiti progresije retinopatije kod većeg broja bolesnika.[15]
Izučavanje gubitka vida, nastog gledanjem u Sunce, poznato vekovima još iz vremena Platona (427—347), koje se karakteriše opekotinama na mrežnjači imalo je veliki značaj za dalji razvoj oftalmoskopije i primenu fotokoagulacije u lečenju bolesti mrežnjače. Mogućnost korišćenja Sunčevog svetla za lečenje bolesti mrežnjače postepeno je evoluirao i u praksu uveo nemački oftalmolog nem. Gerhard Rudolph Edmund Meyer-Schwickerath, na osnovu sopstvenih zapažanja, koje je uočio nakon pomračenja Sunca 10. jula 1945, kada je veliki broj ljudi izgubio vid zbog sunčevom svetlošću izazvanih opekotina. Gerhard je došao na ideju da primeni kontrolisanu upotrebu svetlost Sunca u lečenju bolesti mrežnjače. Na krovu operacione sale izgradio je specijalni uređaj za hvatanje sunčeve svetlosti (poznat kao Meyer-Schwickerath koagulator) i uz pomoć njega doveo snop usmerene sunčeve svetlosti na mrežnjaču bolesnika. Time je on vršio prve fotokoagulacija oka tj uz pomoć nje veštački stvarao opekotine na mrežnjači koje je trebalo da smanje progresiju bolesti.[16] Kako se u praksi ova metoda pokazala kao nepraktična, a oprema preglomazna, eksperimente je Gerhard nastavio sa drugim izvorima svetlosti. Gerhard je prve rezultate u lečenju otoka mrežnjače i suspektnih melanoma mrežnjače primenom sunčeve svetlosti zvanično objavio 1949. godine. Slična istraživanja, nezavisno su radili i Moran-Sales, i ubrzo nakon Gerharda, objavili svoje rezultate 1950. godine. Ova istraživanja bila su zapravo uvod u danas masovno primenjivanu metodu fotokoagulacije. Prvi aparat za fotokoagulaciju sa svetlosnim lukom koji je poticao od ksenonskih sijalica visokog pritiska (umesto sunčeve svetlosti), 1950. konstruisala je i primenila jedna Američka firma (engl. American Optical Corporation in Southbridge, Massachusetts).

Početni rezultati u lečenju dijabetesne retinopatije primenom fotokoagulacije ksenonskom lampom bili su obeshrabrujući. Međutim nakon upornog istraživanja tokom 1950-ih i 1960-ih od strane Vetcinga, Amalrika, Okuna i Vesinga i sve većeg broja drugih oftalmologa širom sveta dobijajani su sve bolji rezultati u lečenju DR.[17][18][19][20][21][22][23] Kembel i Zveng, nešto kasnije, nezavisno koristite talasne dužine rubinskog lasera sa ograničenim uspehom u lečenju u ranim 1960-im, da bi još kasnije Betham i Ajelo dobili znatno bolje rezultate u lečenju dijabetesne retinopatije rubinskom laserfotokoagulacijom, naročito nakon primene širokopojasne panretinalne fotokoagulacije (PRP).[24][25]
Istorija lečenja dijabetesne retinopatije duga je više od 60 godina i nastavlja da se razvija sa novim inovacijama. One se sastoje od mnogo važnih, kreativnih i novi koncepata, elaborata, brojnih laboratorijskih i kliničkih istraživačkih projekata, razvoja revolucionarnih instrumenata i procedura i sofisticiranih metoda koje se korist za kontrolu šećera u krvi, kao i od odgovarajuće fotokoagulacije i očne hirurgije. Budućnost za bolesnike sa DR je ohrabrujuća zbog novih otkrića koja će nadamo se dodatno povećati sposobnost da se sačuva i povrati vid ljudi sa šećernom bolešću.
Anatomija i fiziologija mrežnjače[uredi | uredi izvor]
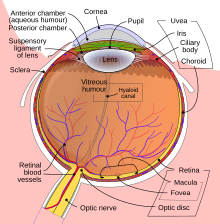

Mrežnjača (lat. Retina), jedan je od najvažnijih funkcionalnih delova oka i njen unutrašnjih omotač na zadnjem zidu. Ona je oko 0,5 mm debela ovojnica i fotosenzitivno tkivo složene, slojevite građe, koje oblaže unutrašnju površinu očne jabučice. Mrežnjača je struktura složene, slojevite građe koja se sastoji od više vrsta ćelijskih elemenata: neurona, glijalnih ćelija, mikroglije, krvnih sudova, pigmentnog epitela. Nekoliko slojeva nervnih ćelija u mrežnjači međusobno je povezanih sinapsama. Jedine nervne ćelije u organizmu koje su direktno fotosenzitivne su fotoreceptorske ćelije. Fotoreceptorske ćelije čine većim delom dva tipa ćelija, štapići i čepići, koji pomažu u stvaranju osećaja svetla i raspoznavanju boja. Štapići se uglavnom aktiviraju kod slabijeg svetla u sumrak i noću i osiguravaju crno beli (noćni) vid dok čepići omogućavaju vid danju i opažaj boja. Treći daleko ređi tip fotoreceptorskih ćelija čine fotosenzitivne ganglijske ćelije koje su važne za refleksne reakcije oka na intenzivno dnevno svetlo.[26] Vidne ćelije oka povezane su sa nervnim vlaknima koji se po izlasku iz mrežnjače udružuju u vidni živac.
Optika oka stvara sliku vidnog sveta na mrežnjači i ima funkciju sličnu onoj koju ima film u fotografskom aparatu. Svetlost koja pada na mrežnjaču izaziva čitav niz električnih i hemijskih nadražaja koji u daljem toku, fizioloških funkcija, aktiviraju nervne nadražaje i šalju ih u vidne centre u mozgu putem vlakana vidnog živca. Mrežnjača se funkcionalno smatra delom centralnog nervnog sistem, a budući da se tokom embrionalnog razvoja kičmenjaka ona i vidni živac formiraju kao izdanci razvijajućeg mozga. To je jedini deo centralnog nervnog sistema koji se može neinvazivno prikazati u živom organizmu.[26]
Za normalnu funciju vida neophodna je nenarušena veza i komunikacija između svih ćelija mrežnjače oka, koje detaljnije opisujemo u nastavku teksta.
- Neuroni

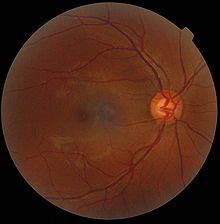
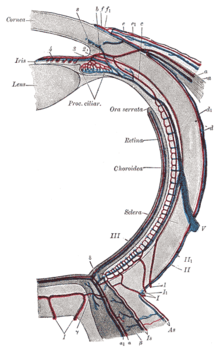
Neuroni i glijalne ćelije mrežnjače čine više od 95% ukupne mase mrežnjača. Kako su transparentni za vidljivu svetlost, njihova struktura i funkcija se ne može ustanoviti na kliničkom pregledu. Kao što je pokazano na slici desno, mrežnjača se primarno sastoji od nervnog tkiva, ili neurona mrežnjače, tj ćelija koje omogućavaju vid. One uključuju fotoreceptore, amakrine, bipolarne, horizontalne i ganglijske ćelije.[27]
Električni „ulazi“ iz sve četiri vrste neurona konvergiraju ka ganglijama, a ektrični impulsi iz gangliona prenose seka mozgu preko aksona nervnih vlakana i optikog živca. Visok stepen konvergencije i integracije signala u mrežnjači registruje se u odnosu 10:1, u fotoreceptorima (≈ 130 miliona) i ganglionima (≈ 1,2 miliona) po ljudskom oku. Stoga, poremećaj u bilo kom od neuronskih slojeva može da omete vid. Zbog specifične strukture i redundantne građe, mrežnjača ima sposobnost da pretrpi smrt mnogih ćelija pre gubitka funkcije vida. [a]
- Glijalne ćelije
Glijalne ćelije mrežnjače - Milerove ćelija i astrociti - su potporne ili ćelije podrške za neurone i krvne sudove mrežnjače.[28] One regulišu ekstracelularnu koncentraciju materija potrebnih za stvaranje jonskog akcionog potencijala, metabolizam neurotransmitera (kao što je glutamat), i transport supstrata kroz krvne sudove potrebnog za metabolizam neurona mrežnjače (glukoze, lipida, amino kiselina). Njihova uloga u regulaciji glutamata naročito je važna, jer višak glutamata kao odgovor na ishemiju mrežnjače ili šećernu bolest, deluje toksično na neurone što može izazvati smrt neuronskih ćelija.[29] Vaskularni endotelni faktor rasta (VEGF) je glavni citokin uključen u ovaj proces kao proizvod astrociti i Milerovih ćelija.
Astrociti signališu kada krvni sudovi treba da stvore barijeru u mrežnjači i izmene protok krvi,[29] razvojem uskih raskrsnica u endotelijalnim ćelijama mrežnjače,[30] i preko funkciju sinapsi mrežnjače,[31] regulišu funkciju vida.[32] Međutim, mnogi detalji načina na koji glijalne ćelije kontrolišu normalne funkcije retine ostaju i dalje nepoznanica.
- Mikroglijalne ćelije
Mikrogliju čine iz koštane srži izvedeni makrofagi koji borave u metaboličkoj sredini mrežnjače. Oni reaguju na raznovrsne nadražaje, kao što su, infekcije ili traume mrežnjače (uključujući i laserfotokoagulaciju) sve do proliferacije, migracije i otpuštanje inflamatornih citokina, kao što su interleukin-1, VEGF i faktor nekroze tumora-α.[33][34]
Oštećenja mrežnjače povećava migraciju iz koštane srži izvedenih imunskih ćelija u mrežnjači i diferencijaciju mikroglijalnih ćelija.[35] U kratkom roku, ovi mehanizmi mogu predstavljati povoljan odgovor na leziju, ali produžena dejstva lezije aktiviraju hronični odgovor na ćelijska oštećenja.
- Krvni sudovi
Fotoreceptorske i druge ćelije mrežnjače oka primaju kiseonik i druge hranljive materije iz sićušnih krvnih sudova (mikrocirkulacije) u njihovoj okolini. Ovi krvni sudovi koji čine vaskularnu mrežu mrežnjače sastoje se od krvnih sudova u i izvan mrežnjače.[36] Mikrocirkulaciju mrežnjače čine prekapilarne arteriole, kapilari i postakpilarne vene. Arteriole poseduje glatke mišićne ćelije, koje im omogućavaju da promeni svoj prečnik i regulišu dinamiku lokalne distribucije krvi u mrežnjači. Prekapilarne arteriole su primarni sudovi za regulaciju otpora protoku krvi, dok venula imaju visoku gustinu receptora za vazoaktivne supstance, kao što je histamin. Venula su pre svega pasivni krvni sudovi, koji služe za dreniranje krvi iz mrežnjače. Kapilari i venula su primarna mesta kroz koja se vrši difuzije tečnosti u mrežnjači pod normalnim uslovima. U patološkim stanjima kao što je šećerna bolest kroz njihove zidove difuzija arasta.[37]
Autoregulacija mrežnjače kao i kod ostalih krvnih sudova u drugim organima je pod uticajem centralnog nervnog sistem koji u određenom organu održava odgovarajuću protok krvi uprkos promenama sistemskog arterijskogi pritiska.[36] Arterijski krvni sudovi mrežnjače u svom zidu imaju glatke mišićne ćelije, dok kapilari, arteriole i venula poseduju pericite, koji funkcionišu kao modifikovane glatke mišićne ćelije. Ove karakteristike krvnih sudova omogućavaju mrežnjači da se njena cirkulacija procesom autoregulacije prilagodi i odgovori na odgovarajuće sistemske i lokalne metaboličke zahteve. Autoregulacija krvnih sudova takođenastaje i kao odgovor na promene parcijalnog pritiska kiseonika (pO2) i ugljen-dioksida (pCO2). Stoga, se krvni sudova skupljaju kao odgovoru na hiperoksemiju i šire kao odgovor na hiperkapniju.
Arteriole mrežnjače se sužavaju kod bolesnika sa hipertenzijom što je oftalmoskopski znak autoregulatorog odgovora za održavanje normalnog intravaskularnog (hidrostatog) pritisak preko obima vaskularnog zida i protoka tečnosti kroz mrežnjaču. Kada autoregulatorni mehanizmi protoka krvi naiđu na barijeru u mrežnjači, kao kada su prepunjeni u hipertenziji, krv, serozni eksudat i lipidni eksudat se akumuliraju u makuli, pa optički disk može da nabubri (postane edematozan). To je, karakteristika hipertenzivnih retinopatija koje mogu da se shvate u svetlu ovih patofiziološkim procesa.[38]
Pod normalnim uslovima, protok krvi kroz mrežnjaču uravnotežen je, kako bi isporuka hranljivih materija i uklanjanje otpadnih produkata omogućilo u mrežnjači odvijanje normalanog metabolizma. Zidovi ovih krvnih sudova su veoma tanki, kako bi hranljive materije bez poteškoća mogle da kroz njih prođu do čepića i štapića. Tokom godina visok nivo šećera u krvi ima za posledicu pojavu sistemski promena u metabolizmu ugljenih hidrata, lipida i proteina, što dovodi do vaskularnih i tkivnih oštećenja u organu kao što je mrežnjače. Tako, nastaje dijabetesna retinopatija kao fundamentalni poremećaj funkcija mrežnjače zbog sistemski narušenog metabolizma glukoze koji oštećuje nervne strukture tkiva mrežnjače i njima pridružene krvne sudove, što dovodi do neurovaskularne degeneracije ili senzorne neuropatije.[26]
- Žuta mrlja

Žuta pigmentirn zona na mrežnjači oka,[39] po kojoj je dobila naziv žuta mrlja (lat. macula lutea), deo je mrežnjače koji sadrži najveći broj čulnih ćelija. Cela oblast žute mrlje sastoji se od centralne ili fovealne jame (lat. fovea centralis), jamskog (fovealnog) nagiba, parafovee i perifovee. Žuta mrlja je zona najjasnijeg vida na mrežnjači oka jer sadrži najveći broj gusto zbijene čulnih ćeli ja.[40] Nalazi se na mrežnjači gde horizontalna osa deli očnu jabučicu na gornju i donju polovinu. U žutoj mrlji, stvara se obrnuta i umanjena slika onoga što vidimo, koja je prethodno prošla kroz rožnjaču, zenicu, očno sočivo i staklasto telo.[41]
Smatra se da žuta mrlja deluje kao filter kratke talasne dužine, koji se dodaje objektiv fotoaparata.[42] Centralni deo žute mrlje je centralna jama koja je od suštinskog je značaja, kao najvažniji deo mrežnjače, za ljudski vid, jer poseduje zaštitne mehanizme za izbegavanje štetnog dejstva intenzivne svetlosti i ultraljubičastog zračenja. Ako uništimo žutu mrlju postajemo slepi.[43]
Šećernom bolešću izazvane bolesti oka[uredi | uredi izvor]
Sa ovom grupom bolesti oka, kao statistički značajnim komplikacijama šećerne bolesti, susreće se sve veća grupa bolesnika u svetu. U najčešće bolesti oka koje se javljaju kao komplikacija šećerne bolesti spadaju:
- MKB-H36.0 — Dijabetesna retinopatija, kao posledica oštećenja krvnih sudova u mrežnjači oka.
- MKB-H28.1 — Katarakta (zamućenje očnog sočiva). Katarakta, koja je se javlja i kao fiziološki znak starenja (rana senilna katarakta), kod bolesnika sa šećernom bolešću razvija se u ranijem životnom dob kao prava dijabetesana katarakta (Snowflake). Ovaj oblik katarakte specifične za šećernu bolest uzrokovan je promenama u kontroli nsulina.
- MKB-H22.0 — Rekurentni iritis, može se javiti u šećernoj bolešeću kod bolesnika sa lošom glikoregulacijom. Ovo je jako bolno stanje oka koje zahteva hitnu oftalmološku procenu i lečenje.
- MKB-H42.0 — Glaukom (povećanje pritiska tečnosti unutar oka), koji kao posledično dovodi do oštećenja optičkog nerva i gubitka vida. Osobe sa šećernom bolešću imaju skoro dva puta veću „šansu“ da dobiju glaukom u odnosu na druge odrasle osobe.
Klasifikacija dijabetesne retinopatije[uredi | uredi izvor]
Klasifikacija dijabetesne retinopatije u osnovi se zasniva na pojavi i anatomskom rasporedu oštećenja koje se javljaju na mrežnjači.
| Stepen retinopatije | Oftalmoskopski nalaz kroz široku zenicu |
|---|---|
| |
(Mild nonproliferative DR) |
|
(Moderate nonproliferative) |
|
(Severe nonproliferative DR) |
|
(Proliferative DR) |
|
Na osnovu karakteristika DR (opisanih u gornjoj tabeli), ETDRS (Early Treatment Diabetic Retinopathy Study Research Group) grupa lekara koja je sprovela obimnu studiju, predložila je pravilo da se klinički izdvoje pacijenti sa velikim stepenom rizika za proliferativnu DR. Oni su to zasnovali na dokazima da umerena NPDR u 15% slučajeva može da pređe u PDR unutar godinu dana, a teška NPDR ako ima dve od navedenih karakteristka, u 45% slučajeva u proliferativnu dijabetesne retinopatiju.[45]
Epidemiologija[uredi | uredi izvor]
Šećerna bolest je masovno hronično oboljenja u stalnom porastu. Početkom 21. veka u svetu je registrovano 171 miliona obolelih od šećerne bolesti (2,8% populacije). Predviđanja su da će do 2030. godine taj broj biti više nego udvostručen i iznosiće 366 miliona (4,4% populacije). Naročito je izražen porast broja obolelih od šećerne bolesti u razvijenim zemljama u kojima je samo od 1995.—2000. godine incidenca porasla za 8,5%, a u zemljama u razvoju i dvostruko više 18%.[46]
Rana invalidnost do koje dovodi šećerna bolest razvojem brojnih komplikacija među kojima dominantno mesto zbog gubitka vida i 100% invalidnosti, ima dijabetesna retinopatija, sve više postaje veliko opterećenje za medicinski sistem i nacionalni budžet, pre svega zemalja u razvoju.[47]
| Zemlja | Obeležje posmatranja | Prevalenca u % |
|---|---|---|
| Sjedinjene Američke Države |
|
|
| Ujedinjeno Kraljevstvo |
|
|
| Indija |
|
|
| Kina |
|
|
| Australija |
|
|
DR je jedan od vodećih uzročnik slepila i slabovidosti kako u razvijenim tako i u zemaljama u razvoju, među kojima spada i Srbija.[49] Globalno u svetu DR, kao uzročnik oštećenja vida i slepila na petom je mestu zastupljenosti sa 4,8%. U razvijenim zemljama Evrope DR je na trećem mestu posle senilne degeneracije makule i glaukoma i zastupljena je sa oko 17%.[50] Kao vodeći uzročnik slepila radno aktivne populacije (između 45 i 65 godine) DR pored medicinskog veliki je i socio-ekonomski problem.
Prema podacima iz jedne od najrazvijenijih zemalja sveta (Sjedinjene Američke Države), od oko 16 miliona Amerikanaca koji boluju od šećerne bolesti, samo oko 50% osoba zna da boluje od DR. Od onih koji za to znaju, samo polovina sprovodi redovnu i odgovarajuću negu očiju. Stoga, ne iznenađujuće činjenica da je dijabetesna retinopatija jedan od vodećih uzroka slepila kod lica starosti od 25 do 74 godina u Sjedinjenim Američkim Državama. Oko 700.000 Amerikanaca boluje od proliferativnog oblika dijabetesne retinopatije, sa godišnjom učestalosti od 65.000. Oko 500.000 lica ispoljava klinički značajan edem makule, sa godišnjom učestalosti od 75.000.[51]
Samo u SAD šećerna bolest je odgovorna za oko 8.000 gubitka vida svake godine, što znači da je DR odgovorna za 12% slepila.[52]
Prevalenca retinopatije značajno se ne razlikuje između muškaraca i žena (taj odnos je 11,5% : 12,7%).[5] Studije sprovedena u Danskoj pokazale su da je ukupna prevalenca retinopatije kod danske populacije od 77% kod muškaraca i 74% kod žena sa dijabetesom tipa 1.[53]
Međutim stopa slepila je različita među određenim etničkim grupama. Povećan rizik od dijabetesne retinopatije, utvrđen brojnim istraživanjima, postoji kod američkih pacijenata hispanocrnaca (16,3%) i meksičkih Amerikanaca (18,0%) u poređenju sa nehispano belcima (11,4%).[54]
Sa povećanjem dužine trajanja šećerne bolesti ili sa starenjem od njenog početka, postoji veći rizik za razvoja dijabetesne retinopatije i njenih komplikacija, uključujući i dijabetesni edema makule ili proliferativna dijabetesnu retinopatiju. Tako se kod pacijenata sa dijabetesom tipa 1, klinički manifestni oblik retinopatije može javiti u prvih 5 godina nakon postavljanja dijagnoze šećerne bolesti. Nakon 10 do 15 godina, 25 do 50% pacijenata pokazuju neke znake retinopatije. Pevalenca DR raste na 75 do 95% posle 15 godina bolesti i približava se vrednosti od 100% nakon 30 godina bolovanja od šećerne bolesti.[5]
Proliferativni oblik dijabetesne retinopatijae (PDR) retko se javlja u prvoj deceniji bolesti kod tipa 1 šećerne bolesti, ali se zato učestalije dijagnostikuje (od 14 do 17%) do 15 godina života, i neprestano raste sa godinama.[5]
Kod bolesnika sa šećernom bolešću tipa 2, incidenca dijabetesne retinopatije neprestano raste sa trajanjem bolesti. Tako 2,23% bolesnika sa šećernom bolešću tipa 2, ima manifestnu nonproliferativu dijabetesnu retinopatiju (NPDR) posle 11 do 13 godina, 41% posle 14 do 16 godina, a 60% nakon 16 godina.[5]
Etiologija[uredi | uredi izvor]
Dijabetesna retinopatija je posledica ili jedna od težih komplikacija kod bolesnika sa šećernom bolešću zbog patoloških promena na krvnim sudovima očnog dna, tj mrežnjače ili retine. Uzrokovana je dugotrajno povišenenim vrednosti šećera u krvi koje oštećuju zidove krvnih sudova celog organizma pa i očiju. Šećernom bolešću oštećeni krvni sudovi postaju propustljiva i dovode do krvarenja u mrežnjači. Na ove promene, nakon više godina bolesti zbog suženja lumena krvnih sudova dolazi do zapušenja kapilara mrežnjače, što za posledicu ima ishemiju u području koje oni ishranjuju. U ovom slučaju nedostatak kiseonika za ishranu ćelija mrežnjače, predstavlja stimulans za rast (umnožavanja) novih kapilara i fibroznog (ožiljnog) tkiva. Tako stvoreni novi krvni sudovi su krhki, pa lako dolazi do njihovog pucanja i krvarenja u oku, koje ima za posledicu propadanje tkiva mrežnjače. Tako na očnom dnu nastaju ireverzibilne promene koje vode ka trajnom gubitku vida ili slepilu.[5]
Faktori rizika[uredi | uredi izvor]
Dužina trajanje šećerne bolesti[uredi | uredi izvor]
Najjači prediktor za rasprostranjenost retinopatije kod bolesnika sa tipom 1 i tipom 2 šećerne bolesti je dužina trajanje šećerne bolesti. U sprovedenim studijama, prevalenca retinopatija je 0% do 8% među bolesnicima sa trogodišnjim trajanjem, 25% do 28% sa petogodišnjim, 60% sa desetogodišnjim i 80% sa petnaestogodišnjim trajanjem šećerne bolesti.[55][56][57][58].
U drugim studijama navedena prevalencija proliferativne retinopatije je 0% za bolesnike sa šećernom bolešću u trajanju do 3 godine, i povećava se na 25% nakon 15 godina trajanja bolesti od momenta dijagnostikovanja. U principu, veća je prevalenca retinopatije kod tipa 2 šećerne bolesti u odnosu na tip 1 šećerne bolesti jer su efekti dužeg trajanja šećerne bolesti, pre postavljanja dijagnoze kod pacijenata sa tipom 2 šećerne bolesti, često nepoznati, ili prema nekim studijama iznose približno 4 do 7 godina pre postavljanja dijagnoze tipa 2 šećerne bolesti.[59] Među bolesnicima sa šećernom bolešću u starijoj životnoj dobi, 2% su oni kod kojih se za manje od 5 godina razvija DR, ili 5% onih kod kojih će se za 15 ili više godina razviti DR. Kod osoba koje nisu primenjivale insulin kao osnovni vid lečenja šećerne bolesti, znaci proliferativne DR javili su se nakon četvorogodišnjeg perioda praćenja.[60]
Neadekvatna glikoregulacija[uredi | uredi izvor]
Jedan od najvažnijih faktora rizika za oboljevanje od dijabetesne retinopatije je ostvareni nivo glikoregulacije u dužem vremenskom periodu.[61][62][63][64][65][66]
Veći broj studija pokazao je da su i mlađi i starije bolesnici sa šećernom bolešću koji nisu imali manifestne znake DR imale značajno niže srednje vrednosti glikoziliranog hemoglobina u odnosu na vrednosti koje su imali pacijente sa retinopatijom. Pacijenti sa višim vrednostima glikoziliranog hemoglobina dokazano je da imaju veći rizik od retinopatija, tako da su oni sa srednjim nivoima HbA1c preko 12% imali 3,2 puta veće šanse za razvoj DR nakon 4 godine od osoba sa nivoima HbA1c ispod 12%.[67]
Kod bolesnika sa šećernom bolešću tipa 1 na strogoj glikoregulaciji ili konvencionalnom lečenju tokom istraživanja u jednoj studiji u periodu od 6,5 godina, smanjena je incidencija retinopatije od 76% i rano napredovanje bolesti za 54%. Svako smanjenje od 10% HbA1c (npr., od 9,0% do 8,1%, odnosno od 8,0% do 7,2%) dovelo je do smanjenja rizika od DR za 39%.[68]
Na osnovu napred navedenih i drugih brojnih epidemiološka i klinička ispitivanja dokazano je da intenzivna terapija i metaboličko održavanje nivoa (blizu-normalnih vrednosti), glikoziliranog hemoglobina može imati značajne i dugoročno dobre rezultate na dalji razvoj DR. Značajno je da ovaj učinak nema prag, i da se dugo i dalje održava nakon inicijacije takve terapije. Međutim, treba naglasiti da na rizik od DR najverovatnije u velikoj meri utiče na kraći rok sprovedena glikoregulacija, kao i da postoji kašnjenje od oko 1 ½ do 2 ½ godine između metaboličke kontrole i merljivih promene rizika za pojavu retinopatije.[67]
Hipertenzija[uredi | uredi izvor]
Uobičajeno stanje kod pacijenata sa šećernom bolešću je i hipertenzija (povišen krvni pritisak >130/80 mm Hg). U jednoj američkoj studiji utvrđeno je da 17% pacijenata sa šećernom bolešću tipa 1 imalo hipertenziju, i da se u daljem toku istraživanja u 25% bolesnika razvila hipertenzija nakon 10 godina.[69]
Kod pacijenata sa dijabetesnom retinopatijom, čvrsto kontrola krvnog pritiska odlaže progresiju bolesti, a sve više dokaza ukazuje na to da renin angotenzin sistem (RAS) igra važnu ulogu u regulaciji krvnog pritiska. RAS je enzimska kaskada u kojoj je angiotenzinogen prekursor angiotenzin peptida. Kaskadni proces počinje konverzijom neaktivnog oblika renina i prorenina, do aktivnog renina.[70] Renin pretvara angiotenzinogen u angiotenzin - 1 (Ang I) koji se dalje cepa uz pomoć angiotenzin konvertujućeg enzima (ACE) do angiotenzina-II (Ang II). Ang II je glavni efektorni peptid RAS, koji deluje pre svega na dva receptora, tipa angiotenzin tip 1 (AT-1) i angiotenzin tip 2 ( AT2 ). Ang II je poznat po tome da izaziva sistemski i lokalni krvni pritisak preko svog efekta pozitivne regulacije preko angiotenzin II tip 1 receptora.
Brojni istraživača proučavali su komponente RAS mrežnjače (Ang I, Ang II, renin, ACE, AT-1, AT-2) u mrežnjači i ustanovili su povećan nivo prorenina, rennina i angiotenzin II u staklastom telu pacijenata sa PDR i dijabetesnim edemom makule (DME), sugerišući time učešće RAS u patogenezi dijabetesne retinopatije.[71][72] Ang II je takođe jedan od faktor rasta, koji promoviše diferencijaciju, apoptozu i uklanjanja ekstracelularnog matriksa.[73][74] Ang II potencira štetan efekat AGEs indukcijom RAGE ekspresije kod hipertenzije u oku jer blokira inhibitore ACE, što ukazuje na vezu između AGE-RAGE i RAS i moguće njihovo uključenje u patogenezu dijabetesne retinopatije.[70]
Anemija[uredi | uredi izvor]
Progresivno povećanje rizika za razvoja proliferative dijabetesne retinopatije kod dijabetičara u anemiji, povezana je sa smanjenjem hematokrita.[75] U najnižu vrednost hematokrita od uticaja na povećani rizik od DR, za muškarce i žene u jednoj američkoj studiji bila je vrednost od 52%. Slični nalazi su viđeni i u studija sa pacijenatima na klinici za dijabetes u Finskoj.[76]
Dislipidemija - hiperlipidemija[uredi | uredi izvor]
Hiperholesterolemija kao faktor rizika prevashodno je zastupljena kod starijih bolesnika sa tipom 2 DM, češće kod sekundarno insulin zavisnih. Iako veliki procenat bolesnika sa retinopatijom ima povišene vrednosti holesterola u krvi, u preko 50% slučajeva nije nađena statistički značajna razlika u povišenom nivou holesterola u bolesnika sa i bez retinopatije. Naime, bolesnici bez retinopatije su takođe imali visoke vrednosti holesterola, što ne isključuje uticaj povišenog nivoa holesterola na razvoj DR.[77]
Dijabetesna nefropatija[uredi | uredi izvor]
Dijabetesna nefropatija je jedna od mnogobrojnih komplikacija šećerne bolesti i predstavlja vodeći pojedinačni uzrok terminalne bubrežne insuficijencije. Javlja se kod 30-40% bolesnika sa šećernom bolesti. S obzirom da je dijabetes tip 2 mnogo češći, veći broj bolesnika sa terminalnom bubrežnom insuficijencijom čine oboleli od ovog tipa šećerne bolesti.[78][79]
Trudnoća[uredi | uredi izvor]
Prema nekim istraživanjima dijabetesna retinopatija kod trudnica sa šećernom bolešću najverovatnije je povezana sa nižim nivoima aktivnosti plazma renina (PRA) i aldosteron, natriuretskih peptida (ANP) u poređenju sa njihovim vrednostima kod zdravih trunica. Snižena aktivnost renin-angiotenzin-sistema (RAS) može da uslovi hiperdinamičniji protok krvi i time doprinese progresiji DR tokom trudnoće u šećernoj bolesti.[80]
Teorija o nastanku DR[uredi | uredi izvor]
Tačan mehanizam kojim šećerna bolest izaziva DR ostaje i dalje nejasan, ali nekoliko teorija pokušava da objasni tipičan tok i istoriju bolesti:
Hormon rasta[uredi | uredi izvor]
Hormon rasta najverovatnije ima uzročnu ulogu u razvoju i progresiji dijabetesne retinopatije. Istraživanjem u dijabetesnoj retinopatiji utvrđene su značajne reverzibilne promene kod žena koje su imale u toku porođaja hemoragijsku nekrozu hipofize (Šehanov sindrom). To je dovelo do kontroverzne primene u praksi, metode ablacije hipofize za lečenje ili prevenciju dijabetesne retinopatije. Od 1950. godini ova tehnika je napušten zbog brojnih sistemskih komplikacija i otkrića efikasnog laserskog tretmana.
Aldoza, reduktaze i vazoproliferativni faktori[uredi | uredi izvor]
U osnovi šećerne bolesti poremećaj je metabolizma glukoze kao rezultat smanjenih nivoa ili aktivnosti insulina. Povećani nivo glukoze u krvi ima strukturni i fiziološki učinak na kapilare mrežnjače, izazivajući u njima brojne patološke procese koji ih čine funkcionalno i anatomski nekompetentnim.
Uporni porast nivoa glukoze u krvi i njegov višak reguliše metabolizam reduktaze i aldoze u određenim tkivima, koje konvertuju šećer u alkohol (npr., glukozu u sorbitol, galaktozu u dulcitol). Unutarzidni periciti kapilara mrežnjače najverovatnije su pod uticajem povećanog nivoa sorbitola, što na kraju dovodi do gubitka njihove primarne funkcije (tj, autoregulacione funkcije kapilara mrežnjače), što dovodi do slabosti i propustljivosti kapilarnih zidova. Povećana propustljivost ovih krvnih sudova rezultati izlaskom tečnosti i proteinskih materijala, koje se nagomilavaju i klinički manifestuju kao zadebljanje i eksudat. Ako otok i eksudacija zahvate makulu, nastaje smanjenje funkcije centralnog vida.
Ruptura mikroaneurizmatskih promena nastalih na izmenjenim krvnim sudovima rutine rezultuje krvarenjem u mrežnjači, površnim (krvarenje u obliku „plamena“) ili u dubljim slojevima mrežnjače (blot i dot krvarenja).
Primenom nailfold video kapilaroskopije, otkrivena je visoka prevalenca kapilarnih promena kod pacijenata sa šećernom bolešću, posebno kod onih sa oštećenjem mrežnjače, što je u suštini odraz opšteg učešće mikrovaskularnih promena u oba tipa, 1 i 2 šećerne bolesti.[5]
Trombociti i viskoznost krvi[uredi | uredi izvor]
Raznovrsnost hematoloških abnormalnosti koje se mogu videti u šećernoj bolesti; povećana agregacije i smanjena savitljivost crvenih krvnih zrnaca, povećana agregacija i adhezija trombocita itd, samo su neki od predisponirajućih faktora koji usporavanjem protoka krvi i kiseonika, oštećuju endotel mrežnjače, i izazivaju žarišnu kapilarnu okluziju. Navedene promene zapravo uzrokuju ishemiju mrežnjače, koja, posledično, doprinosi razvoju dijabetesne retinopatije.
Edem makule[uredi | uredi izvor]
Sa dužinom trajanja šećerne bolesti progresivno raste i pojava dijabetesne retinopatije. Promene u makuli odnosno klinički zanačajan makularni edem je jedan od najčešćih razloga smanjenja odnosno gubika vidne funkcije kod pacijenata sa dijabetesnom retinopatijom. Kod insulin zavisne šećerne bolesti, nakon 25 godina bolesti, makularni edem se javlja kod 20% obolelih, a kod insulin nezavisne šećerne bolesti, kod 15% slučajeve za isti period. Kod bolesnika sa diajbetesnom retinopatijom prisutnom najmanje 10 godina, klinički značajan edem makule prisutan je u proseku kod 14% slučajeva.
Edem makule se može javiti samostalno i biti jedina manifestacija šećerne bolesti ili se može javiti u sklopu ostalih promena dijabetesne retinopatije.
Edem makule je najčešći uzrok gubitka vida kod bolesnika sa neproliferativnom dijabetesnom retinopatijom (NPDR). Međutim, edem makule ne vidi se isključivo ili samo u pacijenata sa NPDR, jer se kao komplikacija može javiti i u slučajevima proliferativne dijabetesne retinopatija. Kod dijagnoze blage neproliferativne retinopatije, edem je prisutan u 3% bolesnika. Kod 38% bolesnika pridružen je dijagnozi umerene neproliferativne retinopatije a čak 78% kod proliferativne retinopatije.[81]
Kako tačan mehanizam nastanka edema makule nije poznat, postoje brojne teorije od kojih se jedna pokušava da objasni razvoj edema makule zasniva, na povećanim nivoima diacilglicerola stvorenog iz viška glukoze. Smatra se da nju aktivira protein kinaza C, koja, zauzvrat, utiče na dinamiku kretanja krvi kroz mrežnjaču, posebno na propustljivost i protok, što dovodi do isticanja tečnosti i zadebljanje mrežnjače. Pored povećanje propustljivosti, postoji i poremećaj u autoregulacija krvnog protoka, zadebljanje bazalne membrane i leukostaza su osnovne karateristike krvnih sudova retine u DR. Rezultati ovih promena imaju za posledice okluziju kapilara, poremećaj retinalne perfuzije i sledstveno, dovodi do ishemije mrežnjače. Na ovaj način nastala ishemija dovodi do nastanka edema i makulopatije, a ujedno je i glavni stimulans patološke neovaskularizacije.
Hipoksija[uredi | uredi izvor]
Kako bolest, hipoksija mrežnjače nastaje zbog, mogućeg začepljenja kapilar mrežnjače. Obimnija retinalna hipoksija izaziva kompenzatorne mehanizme u očima, kako obezbedila dovoljno kiseonika u tkivima. Mikrovaskularni poremećaji mrežnjače, praćeni hipoksijom predstavljaju bitan faktor angiogeneze, ili stvaranja novih krvnih sudova iz već postojećih endotelnih ćelija, proliferacijom ćelija u okviru tkiva mrežnjače, koji su neefikasni jer se ponašaju kao šantovi sa neperfuzionim područjima (vidi sliku ispod).[82]
Neovaskularizacija[uredi | uredi izvor]
Kontinuirano i dugotrajno trajanje i neprestano uvećanje ishemije mrežnjače u šećernoj bolesti pokreće proizvodnju vazoproliferativnih faktora koji stimulišu formiranje (neoangiogenezu) novih krvnih sudova.[83] Ekstracelularni matriks krvnih sudova prvo razara proteaza, a novi kapilari koji proizilaze uglavnom iz venula mrežnjače, prodiru u njenu unutrašnju membranu i formiraju kapilarnu mrežu između unutrašnje površine mrežnjače i njenog zadnjeg hijaloidnog dela.[84]
Najnovijim istraživanjima utvrđeno je da kod bolesnika sa proliferativnom dijabetesnom retinopatijom (PDR), noćna, intermitentna hipoksija/reoksigenacija, koja nastaje u snu zbog poremećaja disanja može biti jedan od faktor rizika za dužičnu i/ili ugaonu neovaskularizaciju.[85]
Neovaskularizacija je najizraženija na granici perfuzije i neperfuzije mrežnjače najčešće se javlja duž vaskularnog luka i na glavnom optičkom nervu. Novostvoreni krvni sudovi probijaju i rastu duž površine mrežnjače u skleru i zadnji hijaloidni deo. Sami po sebi, ovi krvni sudovi retko izazvaju vidne ispade, ali su zbog krhkosti veoma popustljivi i lako se mogu prekinuti u staklastom telu, što može dovesti do krvarenja u šupljinu staklastog tela ili preretinalni prostor.[83][86]
Neovaskularizacijom stvoreni novi i umnoženi krvni sudovi u početku su povezani malom količinom fibroglijalne supstance u formiranom fibroblastnom tkivu. Međutim, kako se gustina neovaskularizovanog dela povećava, tako raste i nivo vlaknastog oblikovanja tkiva.[87]
U kasnijim fazama šećerne bolesti, umnožavanje (neovaskularizacija) krvnih sudova mrežnjače može nazadovati, ostavljajući za sobom samo mrežu fibrovaskularnog tkiva u slojevima mrežnjače i zadnjem hijaloidnom sloju.[83] U staklastom telu ovo novostvoreno fibroblastno tkivo može da vrši, trakcionim silama, povlačenje mrežnjače preko fibroglijalnih veza. Proklizavanje može izazvati edem mrežnjače, heterotropiju mrežnjače i obostrano trakciono odignuće (odlubljivanje) mrežnjače od pigmentnog epiteta.[88]
Patofiziologija[uredi | uredi izvor]
Tačni mehanizmi nastanka dijabetesne retinopatije još uvek nisu dovoljno istraženi. I pored nekoliko biohemijskih teorija koje su do sada objavljene, još uvek se ne mogu u potpunosti prihvatiti mehanizami izneti u njima, niti je pronađena u potpunosti efikasan način lečenja.[89] Ono što je dokazano, uloga je hronične hiperglikemije zajedno sa hiperlipidemijom i hipertenzijom, što doprinosi nastanku dijabetesne retinopatije.[90][91]
Kako dijabetesna retinopatija podrazumeva promene u vaskularnim i nervnim elementima još u ranim fazama šećerne bolesti, sprečavanje gubitka vida kod ovih bolesnika zavisi od boljeg razumevanja osnovnih mehanizama i izmenjenih odnosa između neurona i krvnih sudova mrežnjače. U tom cilju u oftalmologiji su preduzeti mnogi koraci u izučavanju patogeneze dijabetesne retinopatije. Zato će u daljem tekstu biti prikazani samo oni mehanizmi koji su do sada izučeni.
Glavna karakteristika razvoja rane dijabetesne retinopatije su promena u strukturi i ćelijskoj kompoziciji mikrovaskulature mrežnjače (što je šematizovano prikazano na slici desno). Povećanje propustljivosti, poremećaj u autoregulaciji krvnog protoka, zadebljanje bazalne membrane i leukostaza osnovne su karateristike stanja krvnih sudova mrežnjače u dijabetesnoj retinopatiji.[92][93] Ove promene u kapilarnoj mreži mrežnjače imaju za posledicu suženja, sve do okluzije, poremećaj perfuzije i prateću, ishemiju mrežnjače.[94]
Ćelijski i molekularni mehanizam dijabetesne retinopatije[uredi | uredi izvor]
Glavni i ključnih mehanizami uključeni u patofiziologiju dijabetesne retinopatije su:[1]
- Put poliola,
- Izražena glikozilacija i produkcija krajnjih proizvoda napredne glikacije (AGEs)
- Patološko aktiviranje protein kinaze C (PKC)
- Povećani nivo slobodnih radikala izazvan oksidativni stresa.
Put poliola[uredi | uredi izvor]

U šećernoj bolesti put poliola (sorbitol-aldoza reduktaza put), postaje aktivan dejstvom visokih nivoa glukoze u hiperglikemiji, što rezultuje indukcijom aldoza reduktaze i produkcijom sorbitola. Put poliola, zapravo je jedan od metaboličkih procesa koji višak glukoze razlaže na sorbitol koji se zatim konvertuje u fruktozu.
Brojne studija su pokazale da se nivo glukoze, koji se u enormno visokim koncentracijama pojavljuje u šećernoj bolesti, pre svega, metaboliše preko puta poliola koji može dovesti do viška sorbitola i manjka glutationa. koji nastaje zbog smanjene aktivnosti glutation reduktaze usled nedostatka nikotin amid adenin dinukleotid fosfata (NADPH) koji se intenzivno troši u poliol putu glukoze. To posledično rezultuje raznim vaskularnim komplikacijama u mrežnjači zbog ograničenog rastezanja glatkih mišićnih ćelija, usled gubitaka vaskularnih pericita i zadebljanje bazalne membrane.[96]
Ceo mehanizam puta poliola postaje aktivan nakon što visok unutarćelijski nivo glukoze zasititi normalane puteve u metabolizmu glukoze, tako da preostala glukoza nakon podmirenja svih potrebnih metaboličkih procesa u organizmu, ostaje u višku. Tako stvoreni višak glukoze, može dospeti u do tada neaktivan aldoza reduktaza put ili put poliola. Na tom put aldoza reduktaza pretvara glukozu u sorbitol koristeći u tom procesu nikotin amid adenin dinukleotid fosfat (NADPH) kao kofaktor. Sorbitol se u tom procesu dalje oksidira do fruktoze preko sorbitol dehidrogenaze sa NAD(+) kao kofaktorom. Kao što vidimo NADPH je neophodan za aktivnost aldoza reduktaze. Stoga, inteziviranje puta poliola dovodi do povećane potrošnje NADPH.[97] Antioksidativni enzimi kao što su glutation reduktaze koja regeneriše redukovani glutation takođe zahteva NADRN. U skladu sa ovim promenama, povećan je utrošak ovog kofaktora što dovodi do niže aktivnosti glutation reduktaze, što umanjuje intracelularnu koncentraciju redukovanog glutationa, dovodi do redoks-neravnoteže i indukcije okidantivni stres.[98][99][100]
Takođe i hiperprodukcija NADPH i povećanje odnosa sa NADH/NAD dovodi do promenea u sastavu enzima i doprinose formiranju reaktivnih metabolita koji mogu dovesti do ćelijske disfunkcije i oštećenja, koje naknadno mogu izazvati disfunkciju i eventualne gubitke pericita,[101][102][103][104][105] i zadebljanja bazalne membrane.[v][106]
AGEs[uredi | uredi izvor]
AGE (krajnji proizvodi glikacije) formiraju se neenzimskom kondenzacionom reakcijom (neenzimskom glikacijom) između redukcije glukozi i unutarćelijskih i ekstraćelijskih proteine i lipida ili nukleinske kiseline kroz niz složenih reakcije koje daju nepovratnu unakrsno povezanu kompleksnu grupu jedinjenja nazvanu AGEs (engl. Аdvanced glycation end products). Razvoj procesa starenja u direktnoj je vezi sa količinom i trajanjem hiperglikemije. Blaga povećanja koncentracija glukoze, pokazala su istraživanja, daju veliko povećanja nivoa i dovode do akumulacije krajnjih proizvoda napredne glikacije (AGE).[107] AGEs funkcionalno menja matricu bazalne membrane uključujući tu i promene tipa IV kolagena i laminina. AGEs u interakciji sa tipom IV kolagena inhibira bočno spajanje ovih molekula u strukturu mreže bazalne membrane. Efekti laminina uključuju i smanjenje vezivanja za tip IV kolagena i smanjena samomougradnje.[108] Izmene na komponentama matriksa mrežnjače odgovarne su za tkivna zadebljanje u donjem delu membrane kod bolesnika sa šećernom bolešću. AGEs zapravo menja ćelijsku funkciju tako što se vezivanjem za receptore za glikozilaciju krajnjih proizvoda (RAGEs).[109][110]

Vezivanjem AGE na specifičnim receptorima endotelnih ćelije povećavaju koagulacioni faktori (faktor IX and X),[110] a smanjuju antikoagulacioni faktori (trombomodulini),[110] i indukovani vazokonstriktivni faktor (endotelin-1),[111] koji može dovesti do vazokonstrikcije i tromboze u okruženju AGEs.
AGEs, takođe može da promeni i strukturu DNK nuklearnih proteina ćelija nenzimskom modifikacijom kakoja može da rezultuje izmenjenom ekspresijom gena.[112]
AGEs poveća i ekstraluminalnu akumulaciju plazma proteina, uključujući i lipoproteine niske gustine nakon hemijskog vezivanja sa reaktivnim AGE prekursorima matriksa proteina.[113][114]
Zato su AGEs i promene izazvane AGEs, predložen kao odgovoran činilac za nastanak patoloških promena koje se mogu videti u dijabetesnoj retinopatiji.[115]
Protein kinaza C (PKC)[uredi | uredi izvor]
Protein kinaza C (PKC) je porodica od oko 13 izoformi koje su široko rasprostanjene u različitim tkivima sisara. U hiperglikemijskom stanju, neke izoforme PKC su prvenstveno proizvod novonastale, poboljšane sinteze diacilglicerola (DAG) od glukoze do glicerol 3 - fosfata, koji deluju kao aktivator za različite izoforme PKC, iz porodice serin/treonin kinaza, koje poseduju jedinstvenu funkciju.[116] Aktivnosti klasične izoforme (PKC-α, β-1/2, i PKC-δ) u velikoj meri su poboljšana forma diacilglicerola (DAG) koje su povezane sa vaskularnin poremeđajima u patogenezi DR.[117]
Protein kinaza C (PKC) i diacilglicerol (DAG) su unutarćelijske signalne molekule koje su nakon aktivacije odgovorne za pojavu primarne mikrovaskularne ishemija, eksudacije i angiogeneze u DR. Neke od promena usled aktiviranja protein kinaze C (PKC) uključuju: povećanje protoka krvi, zadebljanja bazalne membrane, ekspanziju ekstracelularnog matriksa, vaskularnu propustljivost, angiogenezu, apoptozu, slepljivanje (adheziju) leukocita i aktivaciju citokina.[118][119]
Povećana aktivnost protein kinaze C (PKC) i diacilglicerola (DAG) utvrđena je na životinjskom modelu sa šećernom bolešću,[120] u kome je aktivirana PKC mogla dovesti do vaskularnog oštećenja i povećane ekspresije faktor rasta, koji su predloženi kao faktori patoloških promena koje se razvijaju u dijabetesnoj retinopatiji.[121][122][123]
Povećan nivo slobodnih radikala[uredi | uredi izvor]
Stanje hiperglikemije koja vlada u šećernoj bolesti, deluje kao oksidativni stres, a ovaj preko oksidativne fosforilacija i autooksidacije glukoze povećava nivo slobodnih radikala u organizmu. Tako stvorene reaktivne vrste kiseonika, nastale kao rezultat dejstva oksidativnog stresa, imaju uticaj na razvoj nekih od manifestacija u dijabetesnoj retinopatiji, zbog oštećenja u strukturi DNK molekula ćelija mrežnjače. Zato je održavanje pravilnog redoks balansa ćelija (redukcija — oksidacija) od presudne važnosti, za normalni rad ćelija, u šećernoj bolesti, koja obuhvata ćelijsku varijabilnost, signalizaciju, aktivaciju i proliferaciju.[124] [125][126][127][128]
Na osnovu napred izetih metaboličkim promena i opisanih promene u ekspresiji gena i funkcije proteina može se zaključiti da su one odgovorne za brojne manifestacije ćelijskih disfunkcija i pratećih vaskularnih promena koje se javljaju u šećernoj bolesti. Iako je relativna uloga različite putevi nedovoljno jasna, sa sigurnošću se može tvrditi da je kombinovano ili interaktivno dejstvom svih činilaca i svih navedenih puteva odgovorno za nastanaak promena koje se mogu videti u dijabetesnoj retinopatiji.

Umesto zaključka se može reći, da dugotrajna (višegodišnja) hiperglikemija rezultuje dugogotrajnom višegodišnjom ishemijom koja u šećernoj bolesti može dovesti do metaboličkog disbalansa u ćelijama mrežnjače i aktiviranja vaskularnog endotelnog faktor rasta (engl. vaskular endothelial growth factor VEGF), koji indukujući proliferaciju endotelnih ćelija mrežnjače, povećava propustljivost krvnih sudova i inhibiše apoptozu.[129] Ovim mehanizmom ishemija dovodi do nastanka edema mrežnjače i makulopatije, a ujedno je i glavni stimulans patološke neovaskularizacije.[130][131]
Makula kao specifični anatomski i funkcionalni predeo mrežnjače od posebnog je značaja u dijabetesnoj retinopatiji. Promene u makuli odnosno makularni edem jedan je od najčešćih razloga smanjenja i gubitka vidne oštrine u šećernoj bolesti. Formiranje edema i nakupljanje tečnosti u makularnom predelu dovodi do povećanja volumena ovog prostora. Refraktivni status oka se pomera ka hipermetropiji, a strukturalne promene u ovoj regiji dovode do poremećaja u detekciji i transformaciji svetlosnog zraka u električne impulse. Na taj način vidna oštrina oka se sve više smanjuje.
Faze u razvoju DR[uredi | uredi izvor]
Dijabetesna retinopatija je progresivna bolest koja u svom evolutivnom toku prolazi kroz nekoliko stadijuma.
Neproliferativna dijabetesna retinopatija (NDR)[uredi | uredi izvor]
Ovaj stadijum DR je najraniji i u ovoj fazi bolesti, osobe ne moraju imati smetnje vida, a ako ih imaju, one su posledica makularnog edema (makula je tačka u centralnom delu mrežnjače odgovorna za oštrinu vida). Ona nastaje kao posledica promena u kojima krvni sudovi postaju propustljivije, pa krv izlazi u okolno tkivo - vidljiva su sitna, tačkasta krvarenja.
Makularne edem je otok u području makule koji nastaje zbog curenja tečnosti i krvi iz krvnih sudova toga područja. Smetnje vida u ovom stadijumu bolesti odlikuju se u smanjenju oštrine vida, ili iskrivljenju slike, a moguć je i poremećaj u percepciji boja.
Proliferativna dijabetesna retinopatija (PDR)[uredi | uredi izvor]
Ovaj stadijum DR je uznapredovala faza bolesti koja se javlja zbog smanjenog dopremanja kiseonika u mrežnjaču. Kao posledica ovoakvog stanja, krvni sudovi počinju nenormalno da rastu, kako bi se zadovoljila potreba mrežnjače za kiseonikom. Ovako stvoreni, novi krvni sudovi, lošijeg su kvaliteta i lako pucaju. Može doći do krvarenja u staklasto telo oka (bistra želatinozna masa koja ispunjava očnu jabučicu) što ima za pšosledicu zamagljeni vid i bljeskanje pred očima. Kako bolest napreduje, izražajnije je izmenjeno umnožavanje krvnih sudova i stvaranje ožiljaka koji se pružaju do mrežnjače i povlače je, što može biti uzrok ablacije (odlubljivanja) mrežnjače sa značajnim, naglim slabljenjem vida.
Sekundarni glaukom[uredi | uredi izvor]
Unutaročni (intraokularni) pritisak (IOP) je rezulatat dinamičke ravnoteže stvaranja i odvoda očne vodice. Uslovljen je homeostatskim procesima regulisanim odnosom između produkcije i eliminacije očne vodice. Ista količina od oko 2,2-2,5 mikrolitra koliko se produkuje u oku u minuti biva eliminisana u istom vremenskom intervalu. I produkcija i eliminacija imaju mogućnosti povećanja odnosno smanjenja u cilju održavanja konstantnog IOP-a. Normalan unutaročn pritisak kreće se u rasponu od 10 mmHg - 22 mmHg (prosečno 16 mmHg).[132]
Sekundarni glaukom (povećanje očnog pritiska) javlja se kao jedna od mogućih mikrovaskularnih komplikacija kod DR, najčešće sa ablacijom mrežnjače u poslednjem stadijumu dijabetesne retinopatije. Uzrok su novonastali krvni sudovi u DR koji uzrokuju otežano oticanje očne vodice i povećanje unutaročnog pritiska, što u krajnjem ishodu dovodi do atrofiju očnog živca i potpuni gubitak vida. U zavisnosti od stepen oštećnja krvnih sudova i nakupljanje očne vode i ćelijskih metabolita u ekstracelularnom matriksu daje karakterističan oftalmoskopski izgled oka u sekundarnom glaukomu kod DR.[133]
Katarakta[uredi | uredi izvor]
Promena na očnom sočivu u smislu (katarakte), skrame ili očne mrene još jedna je komplikacija u DR. Naime, u brojnim studijama primećeno je da se kod bolesnika sa šećernom bolešću katarakta lakše i češće razvijaja.
- Juvenilna dijabetesna katarakta razvija se kod mladih bolesnika sa dugom i teškom šećernom bolešću. Karakteriše se brzim razvojem i snežno belim zamućenjem sočiva.
- Kod starijih bolesnika sa dugom i teškom šećernom bolešću katarakta se razvija češće i ranije nego senilna (staračka) katarakta. Ona se po morfološkom izgledu ne razlikuje od juvenilne katarkte. Kod pacijenata koji boluju od šećerne bolesti postoji 3-4 puta veća mogućnost za nastanak katarakte.[134]
Klinička slika[uredi | uredi izvor]
Ovaj odeljak bi trebalo proširiti. Možete pomoći dodavanjem sadržaja. |
Dijagnoza[uredi | uredi izvor]
Ovaj odeljak bi trebalo proširiti. Možete pomoći dodavanjem sadržaja. |
Testovi za rano otkrivanje DR (oftalmološki skrining)[uredi | uredi izvor]
- Testovi za određivanje oštrine vida
- Direktna fundoskopija (kroz proširenu pupilu)
- Indirektna fundoskopija
- Retinalna fotografija
- Merenje intraokularnog (unutaročnog) pritiska
Diferencijalna dijagnoza[uredi | uredi izvor]
- Hemiretinalna okluzija vena mrežnjače kao moguća varijante centralne venske okluzije mrežnjače.
- Okluzija centralne vene mrežnjače
- Makroaneurizma mrežnjače, koja se najčešće javlja kao loptasta dilatacije nastala iz velikih arteriola mrežnjače.
- Šećernom bolešću izazvan edem makule
- Očni ishemijski sindrom, koji nastaje kao posledica hronične insuficijencije vaskularnog sistema oka.
- Neproliferativna dijabetesna retinopatija
- Retinopatija u hemoglobinopatiji
- Valsalva retinopatija, kod srednjeg do naglog povećanja unutargrudnog pritiska.
- Bolest srpastih ćelija
- Tersonov sindrom, ili krvarenje unutar mrežnjače kao posledica subarahnoidalne hemoragije oka.
Terapija[uredi | uredi izvor]
Lečenje šećerne bolesti je primarno u prevenciji DR i postiže se regulacijom hiperglikemije, dijetom, peroralnim antidiajbeticima/ ili insulinom. Uz to, je veoma bitno tretirati dodatne fakor koji doprinose razvoju DR; arterijsku hipertenziju, hiperlipoproteinemiju, bubrežnu disfunkciju, anemiju, gojaznost, propagirati umerenu fizičku aktivnost, izbegavanje pušenja i stres.
Lečenje već prisutne DR sprovodi se putem blagovremene laser terapije i u novije vreme farmakološkom upotrebom lekova intravitrealno i operativnim rešavanjem poodmaklih slučajeva.
Kao najvažniji činilac u evaluaciji i terapiji bolesnika sa DR u šećernoj bolesti javlja se oftalmolog, sa svojim metodama lečenja. Iako oftalmolog ima ključnu ulogu, on mora da bude i koordinator između pacijenta i medicinskog tima koji primarno neguje i leči bolesnika sa šećernom bolešću, uključujući endokrinologa, lekara osnovne zdravstvene zaštite, internistu i/ili drugo medicinsko osoblja. U ovom složenom procesu oftalmolog treba zajedno sa timom da predloži i optimalnu kontrolu metabolizma, koja će značajno da utiče na tok bolesti kod bolesnika sa DR i šećernom bolešću.
Dobro obrazovan tim lekara i ostvarena dobra saradnje tima sa bolesnikom, važan je korak u terapiji DR, koji je najčešće dovoljna da dovede do povoljne rezolucije promena u oku. Pri tome treba imati u vidu da ima i izuzetaka, što svakako ne zavisi od organizacije lečenja, već od rezultata lečenja iskazanih kroz nivoe terapijom ostvarene glikemije, hipertenzije i lipida u krvi, što je najčešće od presudnog značaja za početi uspeh lečenja. Na kraju može se reći da uspeh lečenja DR od strane oftalmologa u velikoj meri zavisi od ostvarene metaboličke kontrole i njenog uticaja na oko.
Opšte mere[uredi | uredi izvor]
Terapiju DR, u svakog pacijenta treba da prate i opšte mere lečenja šećerne bolesti, koje obuhvataju tri osnovna oblika:
- 1. Lečenje poremećaja glikoregulacije
Terapija poremećaja glikoregulacije ima za cilj, definisanje i postizanje definisati individualnih ciljnih vrednosti glikemije i HbA1c u skladu sa sledećim kriterijumima,
| Parametar | Vrednost |
|---|---|
(%) |
|
(mmol/l) |
|
Nepobitno je dokazano, da je intenzivna regulacija hiperglikemije, na nivo kao što je to navedeno u tabeli (HbA1c <7.0), povezana sa smanjen stope razvoj i napredovanje retinopatiju u tip 1 šećerne bolesti. Takođe, u velikoj Britanskoj studije šećerna bolesti, sprovedaana intenzivna kontrola glukoze u krvi (smanjen HbA1c na 7,0%) u tipua 2 šećerne bolesti dovelo je do smanjenja rizika do 25% od mikrovaskularnih promena na krajnjim tačakam, na osnovu čijeg stanja se određuje potrebna za laserfotokoagulaciju mrežnjače. Podaci iz ovih studija poslužili su kao osnova za izradu preporuke, da je za uspešno lešenje DR potrebna intenzivna kontrole glikemije, sa nivoom HbA1c ispod 7%, kako bi se smanjio rizik i napredovanje retinopatija, čime se može postići očuvanje vida kod osoba sa šećernom bolešću.[135]
- 2. Lečenje poremećaja metabolizma lipoproteina
Opservacione studije su takođe pokazale da su povišeni nivoi serumskih lipida direktno povezani sa težinom tvrdih eksudata mrežnjače i smanjene oštrine vida. Da su trigliceridi povezani sa težim oblicima retinopatije, a da je visoka gustina i nivo LDL holesterola obrnuto proporcionaln, navode neke od referenciranih studija. Zato se snižavanje nivoa lipida, preporučuju kao obavezno u terapiji DR, kako bi se sprečile kardiovaskularne bolesti, koje prati i hipertenzija kao važan uzrok gubitka vida.[136][137][138]
- 3. Lečenje povišenog arterijskog pritiska.
Kontrola hipertenzije je od suštinskog značaja u terapiji dijabetesne retinopatije i obavezno se preporučuje saradnja sa internistom. Da pored glikoregulacije, kontrola krvnog pritiska igra važnu ulogu u dijabetsnoj retinopatiji pokazale su sprovedene studije, u kojima je pravilno sprovedena kontrola krvnog pritisaka direktno bila povezana sa smanjenim rizikom od progresije retinopatije.[139] To pokazuju rezultati iz tih studija u kojima se navodi smanjenjenje od 37% mikrovaskularnih bolesti.[140]
Oftalmološka terapija DR[uredi | uredi izvor]
Postoje tri načina lečenja dijabetesne retinopatije koja su vrlo uspešna u sprečavanju gubitka vida uzrokovanog ovom bolešću. Zapravo 90% ljudi sa uznapredovalom dijabetičkom retinopatijom imaju šansu spasiti vid ako se terapijom otpočnu pre nego mrežnjača bude trajno oštećena. Ta tri načina lečenja su: laserfotokoagulacija, vitrektomija, ubrizgavanje triamcinolona u oko.
Postojanje retinopatije nije kontraindiacija za kardioprotektivno terapiju aspirinom, s obzirom da takva terapija ne povećava rizik za nastanak retinalne hemoragije.
Laserfotokoagulacija[uredi | uredi izvor]
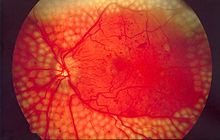
Za sada, jedini terapijski postupak koji se pokazao efikasnim u lečenju dijabetesne retinopatije je laserfotokoagulacija očnog dna, pod uslovom da je pre toga postignuta zadovoljavajuća metabolička kontrola šećerne bolesti.[143] Terapija se sprovodi uz primenu lokalne anestezije, kako bi u toku aplikacije pomeranja glave pacijent bila moguća.
Značaj
- Laserfotokoagulacija razara ishemična područja mrežnjaače, i na taj način smanjujući potencijal proliferacije, utiče ne samo na procese u mrežnjači već i na pokretanje procesa neovaskularizacije dužice i iridokornealnog ugla.
- Blagovremeno primenjena laserfotokoagulacija može da smanji rizik od gubitka vida za 70% kod proliferativne dijabetesne retinopatije (PDR) visokog rizika.
- Cilj terapije je da stvori 1.000 do 2.000 rupica (koagula) u mrežnjači sa pretpostavkom da će smanjiti oštećenje mrežnjače i sprečiti mogućnost ishemije.
- U lečenju uznapredovale dijabetesne retinopatije koagulacije se koriste za uništavanje abnormalnih krvnih sudova koje su se stvorile u mrežnjači.
- Laser lečenje klinički značajog makularnog edema može da smanji rizik od gubitka vida za 50% u slučajevima fokalne ili difuzne makulopatije. Ova metoda se nije pokazala od koristi kod ishemične makulopatije.
Indikacije
Laserfotokoagulaciona terapija je indikovana kod bolesnika sa proliferativne dijabetesne retinopatije (PDR), klinički značajnim makularne edemom i u nekim slučajevima teške neproliferativne dijabetesne retinopatije (NPDR) u cilju smanjenja rizika gubitka vida.
Laserfokokooagulaciju treba primeniti i kod svih bolesnikaa sa šećernom bolešću i neovaskularizacijom u predelu diskusa ili irisa i krvarenja u korpus vitreumu.
Modifikovana engl. ETD RS grid laser fotokoagulacija koristi se kod pacijenata sa klinički značajnim makularnim edemom u odsustvu značajne makularne ishemije.
Neženjeni efekti
Neželjeni efekti laserfokokooagulacije mogu biti
- Gubitak perifernog vida, tunelski vid,
- Noćno slepilo
- Slepilo za boje
Vrste laserfotokoagulacije[uredi | uredi izvor]
Laserfotokoagulaciona terapija, koja se danas primenjuje u praksi, u zavisnosti od indikacija može biti,[144]
Panretinalna fotokoagulacija
Panretinalna fotokoagulacija, se primenjuje se kod proliferativne retinopatije i u osnovi smanjuje učestalost pojave glaukoma sprečavajući nastanak neovaskularnog glaukoma.
| Parametri | Karakteristike ili vrednosti |
|---|---|
| Veličina | 500 mikroma |
| Trajanje | 0,1 do 0,5 sekunde |
| U karajnjoj tačci | Umereno intenzivna sivo-bela opekotina |
| Razmak | Pojedinačne odvojene opekotine |
| Veličina | U obliku dva diska prečnika od gore do dole, i na rastojanju od centra makule po 500 mikrona od ivica diska, koji se protežu do ekvatora ili izvan njega |
| Talasna dužina | Argon–zelena |
Usmerena (fokalna) ili mrežasta fotokoagulacija
Usmerena (fokalna) ili mrežasta fotokoagulacija, primenjuje se kod makularnog edema.
| Parametri | Karakteristike ili vrednosti |
|---|---|
| Veličina | 50–100 mikroma |
| Trajanje | 0,1 sekunda |
| U karajnjoj tačci | Jedva vidljiva promena boje |
| Obim | Sve propuštajuće mikroaneurizme između 500 i 3.000 mikrona od centra makule |
| Talasna dužina | Argon–zelena |
Brojne studije potvrdile su izuzetno povoljene rezultata primene panretinalne laserfotokoagulacije kod proliferativnih retinopatija dok je fokalna fotokoagulacija smanjila u značajnoj meri gubitak vidne oštrine kao poledice makularnog edema.[142]
Vitrektomija[uredi | uredi izvor]

Vitrektomija jedna je od metoda vitreoretinalna hirurgije koj obuhvata procedure koje se rade na unutrašnjim strukturama oka, u ovom slučaju, staklastom telu. Staklasta telo ili vitreum je želatinozna providna struktura koja se nalazi iza sočiva a ispred mrežnjače oka.
Indikacije
Vitrektomiju treba primeniti u bolesnika sa tipom 1 šećerne bolesti i perzistentnim krvarenjem u korpus vitreumu.
Vitrektomiju bi trebalo uraditi i kod bolesnika sa trakcionim odlubljivanjem mrežnjače koje ugrožava makulu a trebalo bi razmotriti primenu ove metode i kod pacijenata sa fibrovaskularnom proliferacijom. Ukoliko je indikacija bila odlubljivanje mrežnjače kao posledica postojanja fibrovaksularnih membrana kod proliferativne dijabetesne retinopatije, uklanjanjem tih membrana i tamponadom silikonskim uljem mrežnjača se vraća na njeno mesto i smanjuje mogućnost za njeno ponovno odlubljivanje.
Kod bolesnika sa tipom 2 šećerne bolesti i krvarenjem u korpus vitreumu koje je teško i onemogućava fotokoagulaciju, obavezno treba razmotriti primenu vitrektomije. Ukoliko je indikacija za vitrektomiju bilo krvarenje u staklastom telu, uklanjanjem staklastog tela i prisutne krvi ponovo se omogućava prolazak svetlosti kroz unutrašnjost oka do mrežnjače.
Ekstrakcija katarakte kod pacijenata sa šećernom bolešću[uredi | uredi izvor]

Operaciju katarakte ne bi trebalo odlagati kod pacijenata sa šećernom bolešću. Zato se ona preporučuje kada se ne može isključiti postojanje retinopatije koja ugrožava vid.
Kada se planira ekstrakcija katarakte u sklopu postojanja uznapredovale bolesti, koja se nije stabilizovala pre operacije treba porazgovarati sa bolesnikom o mogućuoj progresiji bolesti i potrebi za postoperativnim praćenjem.
Intravitrealna farmakoterapija DR[uredi | uredi izvor]
Trenutno, se nekoliko lekova koristi u lečenju dijabetesne retinopatije. Ovi lekovi se ordiniraju u oko intravitrealnim ubruzgavanjem, po čemu je ova vrsta lečenja i dobila naziv, intravitrealna farmako terapija dijabetesne retinopatije. Ova vrsta farmakoterapije za sada se koristi samo kao dodatak u lečenju tradicionalnom laserskom fotokoagulacijom dijabetesne retinopatije. Da je opravdana kombinovana primena nekih od intravitrealnih lekova sa fokalnom laserskom terapijom potvrdila su klinička ispitivanja u jednoj studiji (engl. Diabetic Retinopathy Clinical Research Network (DRCR.net)), koja je pokazala određenu efikasnost, koju daljim istraživanjima treba pratiti.[145][146]
Kod pacijenata sa dugogodišnjim edemom makule koja ne reaguje na konvencionalne načine lečenja, kao što je fokalna ili mrežasta laserska fotokoagulacija, primena intravitrealno ubrizganog triamcinolon može se smatrati opravdanom. Takođe čekaju se i rezultati opesžnijih studija u primeni bevacizumaba (Avastin) i ranibizumaba (Lucentis) u lečenju dijabetesnog edema makule.[147]
Triamcinolon (Triamcinolone)
Intravitrealni triamcinolon je jedan od najčešće korišćenih preparata u lečenju dijabetesnog edema makule.[148] Nedavna klinička ispitivanja (engl. Diabetic Retinopathy Clinical Research Network (DRCR.net)) pokazala su kod nekih bolesnika smanjenje edema makule posle intravitrealne primene triamcinolona, mada ovaj učinak nije bio tako izražen, kao učinak koji se postiže fokalnim laserskim tretmanom u trajanju od dve godine.[145]
Pored toga, intravitrealna primena triamcinolon može imati neke negativne efekte, uključujući steroidi odgovor praćen uvećanjem očnog pritiska,[149][150][151] infektivnim (bakterijski endooftelmitis) i nezaraznim endoftalmitisom i kataraktom.[152][153][154]
Bevacizumab (Avastin) i ranibizumabom (Lucentis)
Drugi lekovi koji se koriste u kliničkoj praksi i u kliničkim ispitivanjima uključuju intravitrealne bevacizumab i ranibizumabom (Lucentis).[155] Ovi lekovi su VEGF antitela i fragmenti antitela. Oni mogu pomoći u smanjenju dijabetesnog edema makule (žute mrlje) i vaskulogeneze diska ili mrežnjače. Međutim, rezultati i poboljšanju funkcije vida su manje impresivan. Da li je to zbog trajnog oštećenje fotoreceptora u vreme ubrizgavanja leka u slučajevima gde je on primenjeni ili se radi o refraktarnim slučajevima daljim istraživanjima treba da se utvrdi.[156]
Mere prevencije[uredi | uredi izvor]
Mere prevencije dijabetesne retinopatije u principu se zasnivaju na strogoj regulaciji insulina i i svih drugih poremećaja u šećernoj bolesti i obahvataju:
Redovno uzimanje lekove prema uputstvu lekara
Korišćenje insulina, ako je to potrebno
Pravilna regulacija nivoa šećera u krvi i krvnog pritiska
- Pravilna regulacija nivoa šećera obuhvata dobru kontrolu glikemije (HbA1c <7%). Brzo popravljanje kontrole glikemije može dovesti do pogoršanja bolesti mrežnjače. Laser fotokoagulaciju, ako je neophodna treba uraditi pre brzog postizanja optimalne glikoregulacije.
- Pravilna regulacija vrednosti krvnog pritiska (<130/80 mmHg)
Telesno vežbanje
- Telesno vežbanje ima za cilj smanje nivoi šećera u krvi, redukciju telesne težine i psihorelaksaciju.
Redovno laboratorijsko ispitivanje
- Redovno ispitivanje nivoa šećera u krvi
- Redovno ispitivanje nivoa ketonskih tela u mokraći
Redovne zdravstvene kontrole
- Redovnu kontrolu zdravlja treba sprovoditi u cilju praćenja toka šećerne bolesti i isključivanja ili lečenje drugih faktora rizika, kao što su visok krvni pritisak i visok holesterol.
Redovni oftalmološki pregledi
- Odrasli i deca uzrasta 10 godina i starija sa tipom 1 šećerne bolesti trebalo bi da imaju inicijalni detaljni i sveobuhvatni oftalmološki ili optometrijske pregled oka u prvih 5 godina po po pojavi simptoma i znakova šećerne bolesti.
- Bolesnici sa tipom 2 šećerne bolesti trbalo bi da imaju inicijalni i detaljni oftalmološki ili optometrijske pregled neposredno po postavljanju dijagnoze šećerne bolesti.
- Žene sa dijagnostikovanom šećernom bolesti koje planiraju trudnoću ili koje su trudne treba da imaju sveobuhvatni pregled okakako bi dobile savet vezan za razvoj i/ili progresiju dijabetesne retinopatije. Pregled oka trudnice treba obavljati u prvom trimestru uz striktno praćenje celog toka trudnoće i u prvih godinu dana po porođaju.
- Naknadne oftalmološke ili optometrijske preglede pacijenta sa tipom 1 i tipom 2 šećerne bolestia treba ponavljati jednom godišnje.
- Ređi pregledi (na svake 2 do 3 godine) mogu se raditi u slučaju prethodnih normalnih pregleda. Češći pregledi su neophodni u slučaju progresije retinopatije. Retinalna fotografija ili biomikroskopija u redovnim oflamološkim pregledima koriste se za sistematski skrining dijabetesne retinopatije. Direktna oftalmoskopija koristi se alternativno.
Prognoza[uredi | uredi izvor]
Ovaj odeljak bi trebalo proširiti. Možete pomoći dodavanjem sadržaja. |
Napomene[uredi | uredi izvor]
- ^ Na primer, oštećenje najmanje 50% ganglijskih ćelija mogu da izgube funkciju pre klinički utvrđenog oštećenja vida, što je očigledno kod pacijenata sa glaukomom. Oko može da zadrži i 20/20 vidnu funkciju i sa manje od 10% konusa sa fotoreceptorima.
- ^ IRMA (intraretinalne mikrovaskularne abnormalnosti)
- ^ Najnovija istraživanja pokazala su da se upotrebom inhibitor aldoza reduktaze u terapiji može smanjiti formiranje sorbitola i na taj način usporiti napredovanje, ili čak sprečiti, dijabetesna retinopatija.[95]
Izvori[uredi | uredi izvor]
- ^ a b Robert N. Frank (2004). „Diabetic retinopathy”. New England Journal of Medicine. 350 (1): 48—58. PMID 14702427. doi:10.1056/NEJMra021678.
- ^ Lorenzi M. „The polyol pathway as a mechanism for diabetic retinopathy: attractive, elusive and resilient”. Exp Diabetes Res. PMID 18224243. doi:10.1155/2007/61038.
- ^ Williamson JR, Chang K, Frangos M; et al. (1993). „Hyperglycemic pseudohypoxia and diabetic complications”. Diabetes. 42: 801—813. doi:10.2337/diab.42.6.801..
- ^ Mizutani M, Kern TS, Lorenzi M. (1996). „Accelerated death of retinal microvascular cells in human and experimental diabetic retinopathy”. J Clin Inves. 97: 2883—2890. doi:10.1172/JCI118746..
- ^ a b v g d đ e Duh, Elia (2008). Diabetic Retinopathy. Springer. ISBN 978-1-59745-563-3.
- ^ Bertram, B. (1997). „Prevalence of patients with DM without and with retinopathy in an ophthalmology practice”. Ophthalmologe. 94 (6): 401—4.
- ^ Nathan DM. The pathophysiology of diabetic complications: how much does the glucose hypothesis explain? Ann Intern Med 1996; 124(1Pt2): 86-9.
- ^ The Diabetic Retinopathy Study Research Group (1981). „Photocoagulation Treatment of Proliferative Diabetic Retinopathy”. Ophthalmology. 88 (7): 583—600. doi:10.1016/S0161-6420(81)34978-1.
- ^ The Diabetic Retinopathy Study Research Group. (1976). „Preliminary report on the effects of photocoagulation therapy”. Am J Ophthalmol. 81 (4): 383—96..
- ^ Bidyadhar, N.K. (1939), Sushruta's Ophthalmic Operations, Archives of Ophthalmology, 22, page 553.
- ^ Agarwal, R.K. (1965). „Ancient Indian Ophthalmology”. The Ophthalmic Optician. 5 (21): 1093—1100. (the title of this journal was changed to Optometry Today in 1985), published by the Association of Optometrists, London, England.
- ^ von Jaeger E. Beitrage zur Pathologie des Auges. 2 1.. Lieferung, S. 33, Tafel XII. Wien, K.K. Hof- and Staatsdruckerei; 1855.
- ^ Banting FG, Best CH. (1922). „The internal secretion of the pancreas”. J Lab Clin Med. 7: 251—266..
- ^ Hutton, W. L.; Snyder, W. B.; Vaiser, A.; Siperstein, M. D. (1972). „Retinal microangiopathy without associated glucose intolerance”. Trans Amer Acad Ophthalmol Otolaryngol. 76 (4): 968—980. PMID 4666943..
- ^ Diabetes Control and Complications Trial Research Group; Nathan, D. M.; Genuth, S.; Lachin, J.; Cleary, P.; Crofford, O.; Davis, M.; Rand, L.; Siebert, C. (1993). „The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus”. New England Journal of Medicine. 329 (14): 977—986. PMID 8366922. S2CID 21528496. doi:10.1056/NEJM199309303291401..
- ^ G. Meyer-Schwickerath, E. Grüterich, H. Weyers: „Mikrophthalmus-Syndrome.”. Klinische Monatsblätter für Augenheilkunde. Stuttgart. 131: 18—30. 1957..
- ^ Wetzig, P. C.; Jepson, C. N. (1966). „Treatment of diabetic retinopathy by light coagulation”. Am JOphthalmol. 62 (3): 459—465. PMID 5921994. doi:10.1016/0002-9394(66)91325-0..
- ^ Amalric MP (1960). „Essai de traitement de la rétinopathie diabétique exsudative”. Bulletin des Societes d'Ophtalmologie de France.
- ^ Amalric, P. (1967). „New considerations concerning the evolution and treatment of diabetic retinopathy”. Ophthalmologica. 154 (2): 151—160. PMID 6057541. doi:10.1159/000305159..
- ^ Okun, E.; Cibis, P. A. (1966). „The role of photocoagulation in the treatment of proliferative dia-betic retinopathy”. Arch Ophthalmol. 75 (3): 337—352. PMID 5903819. doi:10.1001/archopht.1966.00970050339007..
- ^ Okun, E. (1968). „The effectiveness of photocoagulation in the therapy of proliferative diabetic retinopathy (PDR). (A controlled study in 50 patients)”. Trans Am Acad Ophthalmol Otolaryngol. 72 (2): 246—252. PMID 5659907..
- ^ Okun E, Johnston G, Boniuk I. Management of Diabetic Retinopathy; a StereoscopicPresentation. St. Louis: The C.V. Mosby Co; 1971.
- ^ Wessing AK, Meyer-Schwickerath G. Results of photocoagulation in diabetic reti-nopathy. In: Goldberg MF, Fine SL, eds. Symposium on the Treatment of Diabetic Retinopathy. Airlie House, Warrenton, VA, September 29 to October 1, 1968. Washington, DC, US Government Printing Office (PHS Publ No 1980), (1969), str. 569–592.
- ^ Beetham, W. P.; Aiello, L. M.; Balodimos, M. C.; Koncz, L. (1970). „Ruby laser photocoagulation of early diabetic neovascular retinopathy. Preliminary report of a long-term controlled study”. Arch Ophthalmol. 83 (3): 261—272. PMID 5461208. S2CID 35983038. doi:10.1001/archopht.1970.00990030263001..
- ^ Aiello LM, Beetham WP, Balodimos MC, et al. Ruby laser photocoagulation in treatment of diabetic proliferating retinopathy: preliminary report. In: Goldberg MF, Fine SL, eds. Symposium on the Treatment of Diabetic Retinopathy. Airlie House, Warrenton, VA, September 29–October 1, 1968. Washington, DC, US Government Printing Office (PHS Publ No 1980), (1968), str. 437–463.
- ^ a b v Browning, David J. (2010). Diabetic Retinopathy: Evidence-Based Management. Springer. str. 1—10. ISBN 978-0-387-85900-2.
- ^ „Simple Anatomy of the retina”. Pristupljeno 9. 1. 2014.
- ^ Stone, J.; Dreher, Z. (1987). „Relationship between astrocytes, ganglion cells and vasculature of the retina”. J Comp Neurol. 255 (1): 35—49. PMID 3819008. S2CID 37889243. doi:10.1002/cne.902550104..
- ^ a b Lieth, E.; Lanoue, K. F.; Antonetti, D. A.; Ratz, M. (2000). „Diabetes reduces glutamate oxidation and glutamine synthesis in the retina. The Penn State Retina Research Group”. Exp Eye Res. 70 (6): 723—730. PMID 10843776. doi:10.1006/exer.2000.0840..
- ^ Gardner, T. W.; Lieth, E.; Khin, S. A.; Barber, A. J.; Bonsall, D. J.; Lesher, T.; Rice, K.; Brennan Jr, W. A. (1997). „Astrocytes increase barrier properties and ZO-1 expression in retinal vascular endothelial cells”. Invest Ophthalmol Vis Sci. 38 (11): 2423—2427. PMID 9344364..
- ^ Newman, Eric A. (2004). „Glial modulation of synaptic transmission in the retina”. Glia. 47 (3): 268—274. PMC 2322937
 . PMID 15252816. doi:10.1002/glia.20030..
. PMID 15252816. doi:10.1002/glia.20030..
- ^ Newman, E. A. (2003). „New roles for astrocytes: Regulation of synaptic transmission”. Trends Neurosci. 26 (10): 536—542. PMID 14522146. S2CID 14105472. doi:10.1016/S0166-2236(03)00237-6..
- ^ Schuetz, E.; Thanos, S. (2004). „Microglia-targeted pharmacotherapy in retinal neurodegenerative diseases”. Curr Drug Targets. 5 (7): 619—627. PMID 15473251. doi:10.2174/1389450043345164..
- ^ Lee JE, Liang KJ, Fariss RN, Wong WT. (2008). „Ex vivo dynamic imaging of retinal microglia using time-lapse confocal microscopy”. Invest Ophthalmol Vis Sci. 49: 4169—4176..
- ^ Kaneko, Hiroki; Nishiguchi, Koji M.; Nakamura, Makoto; Kachi, Shu; Terasaki, Hiroko (2008). „Characteristics of Bone Marrow–Derived Microglia in the Normal and Injured Retina”. Invest Ophthalmol Vis Sci. 49 (9): 4162—4168. PMID 18487364. doi:10.1167/iovs.08-1738..
- ^ a b Wise GN, Dollery CT, Henkind P. The Retinal Circulation. New York: Harper & Row; (1971), str. 34–54.
- ^ Barber, A. J.; Antonetti, D. A. (2003). „Mapping the blood vessels with paracellular permeability in the retinas of diabetic rats”. Invest Ophthalmol Vis Sci. 44 (12): 5410—5416. PMID 14638745. doi:10.1167/iovs.03-0244..
- ^ Wong, T. Y.; Mitchell, P. (2004). „Hypertensive retinopathy”. New England Journal of Medicine. 351 (22): 2310—2317. PMID 15564546. doi:10.1056/NEJMra032865..
- ^ Balashov NA, Bernstein PS. Purification and identification of the components of the human macular carotenoid metabolism pathways. Invest Ophthal Vis Sci.1998;39:s38.
- ^ Susan Standring, ur. (2009) [1858]. Gray's anatomy: The Anatomical Basis of Clinical Practice, Expert Consult. illustrated by Richard E. M. Moore (40 izd.). Churchill Livingstone. ISBN 978-0-443-06684-9.
- ^ Siege, Allan (2006). Essential Neuroscience. Baltimore, Maryland: Lippincott Williams & Wilkins. ISBN 978-0-7813-9121-2 Proverite vrednost parametra
|isbn=: checksum (pomoć). - ^ Rodieck RW. The vertebrate retina: principles of structure and function. San Francisco: W.H. Freeman and Company; 1973.
- ^ Hageman GS, Johnson LV. The photoreceptor-retinal pigmented epithelium interface. In: Heckenlively JR, Arden GB, editors. Principles and practice of clinical electrophysiology of vision. St. Louis: Mosby Year Book; 1991. pp. 53-68.
- ^ Wilkinson, C. P.; Ferris Fl, 3rd; Klein, R. E.; Lee, P. P.; Agardh, C. D.; Davis, M.; Dills, D.; Kampik, A.; Pararajasegaram, R.; Verdaguer, J. T.; Global Diabetic Retinopathy Project Group (2003). „Proposed international clinical diabetic retinopathy and diabetic macular edema disease severity scales”. Ophthalmology. 110 (9): 1677—1682. PMID 13129861. doi:10.1016/S0161-6420(03)00475-5.
- ^ Early Treatment Diabetic Retinopathy Study Research Group. Early photocoagulation for diabetic retinopathy: ETDRS report number 9. Ophthalmology 1991;98(Suppl):766-785.
- ^ Wild S, Roglic G, Green A, Global Prevalence of Diabetes, estimates for the year 2000 and projections for 2030“. Diabetic Care 2004; 27: 1047- 1053
- ^ Teruel, M.C., Fernández-Real, J.M., Ricart, W., Valent, F.R., Vallés, P.M. (2005). „Prevalence of diabetic retinopathy in the region of Girona”. Study of related factors. Archivos de la Sociedad Española de Oftalmología. 80 (2): 85—91.
- ^ Scanlon, Peter H.; Aldington, Stephen; Wilkinson, Charles; Matthews, David (12. 3. 2009). A Practical Manual of Diabetic Retinopathy Management. John Wiley & Sons. ISBN 978-1-4443-0818-1.
- ^ World Health Organisation, fact sheet “ Magnitude and causes of visual impairment” Nov. 2005.
- ^ Vision 2020, The Right to Sight, Global Initiative for the Elimination of Avoidable Blindness: action plan 2006-2011. World Health Organization Geneva 2007
- ^ Fong DS, Aiello L, Gardner TW, et al; American Diabetes Association. Diabetic retinopathy. Diabetes Care. 2003;26:(suppl 10) S99-S102
- ^ The Wisconsin Epidemiologic Study of Diabetic Retinopathy XXIII: the twenty-five-year incidence of macular edema in persons with type 1 diabetes. Klein R, Knudtson MD, Lee KE, Gangnon R, Klein BE. (mart 2009). „Diabetic Retinopathy Medication: Corticosteroids, Ophthalmics, VEGF Inhibitors”. Ophthalmology. 116 (3): 497—503. PMC 2693093
 . PMID 19167079. doi:10.1016/j.ophtha.2008.10.016.
. PMID 19167079. doi:10.1016/j.ophtha.2008.10.016.
- ^ „Photocoagulation for diabetic macular edema: Early Treatment Diabetic Retinopathy Study Report no. 4. The Early Treatment Diabetic Retinopathy Study Research Group”. Int Ophthalmol Clin. 27 (4): 265—272. 1987. PMID 3692708. S2CID 9733059. doi:10.1097/00004397-198702740-00006..
- ^ Morello, Candis M. (2007). „Etiology and natural history of diabetic retinopathy: an overview”. Am J Health Syst Pharm. 64 (17): S3—S7. PMID 17720892. doi:10.2146/ajhp070330.
- ^ Klein, R.; Klein, B. E.; Moss, S. E.; Davis, M. D.; Demets, D. L. (1984). „Prevalence and risk of diabetic retinopathy when age at diagnosis is less than 30 years”. Arch Ophthalmol. 102 (4): 520—526. PMID 6367724. doi:10.1001/archopht.1984.01040030398010..
- ^ Klein, R.; Klein, B. E.; Moss, S. E.; Davis, M. D.; Demets, D. L. (1989). „Four-year incidence and progression of diabetic retinopathy when age at diagnosis is less than 30 years”. Arch Ophthalmol. 107 (2): 237—243. PMID 2916977. doi:10.1001/archopht.1989.01070010243030..
- ^ Klein, R.; Klein, B. E.; Moss, S. E.; Davis, M. D.; Demets, D. L. (1989). „Four-year incidence and progression of diabetic retinopathy when age at diagnosis is 30 years or more”. Arch Ophthalmol. 107 (2): 244—249. PMID 2644929. doi:10.1001/archopht.1989.01070010250031..
- ^ Klein, R.; Klein, B. E.; Moss, S. E.; Cruickshanks, K. J. (1994). „Ten-year incidence and progression of diabetic retinopathy”. Arch Ophthalmol. 112 (9): 1217—1228. PMID 7619101. doi:10.1001/archopht.1994.01090210105023.
- ^ Harris, M. I.; Klein, R.; Welborn, T. A.; Knuiman, M. W. (1992). „Onset of NIDDM occurs at least 4-7 yr before clinical diagnosis”. Diabetes Care. 15 (7): 815—819. PMID 1516497. S2CID 34366464. doi:10.2337/diacare.15.7.815..
- ^ Yu, T.; Mitchell, P.; Berry, G.; Li, W.; Wang, J. J. (1998). „Retinopathy in older persons without diabetes and its relationship to hypertension”. Arch Ophthalmol. 116 (1): 83—89. PMID 9445212. doi:10.1001/archopht.116.1.83..
- ^ Colwell, J. A. (1966). „Effect of diabetic control on retinopathy”. Diabetes. 15 (7): 497—499. PMID 5329504. S2CID 5310155. doi:10.2337/diab.15.7.497..
- ^ Miki, E.; Fukuda, M.; Kuzuya, T.; Kosaka, K.; Nakao, K. (1969). „Relation of the course of retinopathy to control of diabetes, age, and therapeutic agents in diabetic Japanese patients”. Diabetes. 18 (11): 773—780. PMID 5348519. S2CID 39860810. doi:10.2337/diab.18.11.773..
- ^ Doft, B. H.; Kingsley, L. A.; Orchard, T. J.; Kuller, L.; Drash, A.; Becker, D. (1984). „The association between long-term diabetic control and early retinopathy”. Ophthalmology. 91 (7): 763—769. PMID 6472813. doi:10.1016/S0161-6420(84)34235-X..
- ^ Friberg, T. R.; Rosenstock, J.; Sanborn, G.; Vaghefi, A.; Raskin, P. (1985). „The effect of long-term near normal glycemic control on mild diabetic retinopathy”. Ophthalmology. 92 (8): 1051—1058. PMID 4047600. doi:10.1016/S0161-6420(85)33903-9..
- ^ Kroc Collaborative Study Group (1984). „Blood glucose control and the evolution of diabetic retinopathy and albuminuria. A preliminary multicenter trial”. New England Journal of Medicine. 311 (6): 365—372. PMID 6377076. doi:10.1056/NEJM198408093110604..
- ^ Lauritzen, T.; Frost-Larsen, K.; Larsen, H. W.; Deckert, T. (1983). „Effect of 1 year of near-normal blood glucose levels on retinopathy in insulin-dependent diabetics”. Lancet. 1 (8318): 200—204. PMID 6130243. S2CID 32140907. doi:10.1016/s0140-6736(83)92585-0..
- ^ a b Klein, R.; Klein, B. E.; Moss, S. E.; Davis, M. D.; Demets, D. L. (1988). „Glycosylated hemoglobin predicts the incidence and progression of diabetic retinopathy”. JAMA. 260 (19): 2864—2871. PMID 3184351. doi:10.1001/jama.1988.03410190112033..
- ^ „The Kroc Collaborative Study Group”. New England Journal of Medicine. 311 (6): 365—372. 1984..
- ^ Klein, R.; Klein, B. E.; Lee, K. E.; Cruickshanks, K. J.; Moss, S. E. (1996). „The incidence of hypertension in insulin-dependent diabetes”. Arch Intern Med. 156 (6): 622—627. PMID 8629873. doi:10.1001/archinte.1996.00440060042005..
- ^ a b Satofuka, Shingo; Ichihara, Atsuhiro; Nagai, Norihiro; Noda, Kousuke; Ozawa, Yoko; Fukamizu, Akiyoshi; Tsubota, Kazuo; Itoh, Hiroshi; Oike, Yuichi; Ishida, Susumu (jul 2009). „(Pro)renin Receptor–Mediated Signal Transduction and Tissue Renin-Angiotensin System Contribute to Diabetes-Induced Retinal Inflammation”. Diabetes. 58 (7): 1625—33. PMC 2699867
 . PMID 19389828. S2CID 8613584. doi:10.2337/db08-0254..
. PMID 19389828. S2CID 8613584. doi:10.2337/db08-0254..
- ^ Noma, H.; Funatsu, H.; Mimura, T.; Harino, S.; Hori, S. (januar 2009). „Vitreous levels of interleukin-6 and vascular endothelial growth factor in macular edema with central retinal vein occlusion”. Ophthalmology. 116 (1): 87—93. PMID 19118700. doi:10.1016/j.ophtha.2008.09.034..
- ^ Nagai, N.; Noda, K.; Urano, T.; Kubota, Y.; Shinoda, H.; Koto, T.; Shinoda, K.; Inoue, M.; Shiomi, T.; Ikeda, E.; Tsubota, K.; Suda, T.; Oike, Y.; Ishida, S. (mart 2005). „Selective suppression of pathologic, but not physiologic, retinal neovascularization by blocking the angiotensin II type 1 receptor”. Invest Ophthalmol Vis Sci. 46 (3): 1078—84. PMID 15728568. doi:10.1167/iovs.04-1101..
- ^ Otani, Atsushi; Takagi, Hitoshi; Oh, Hideyasu; Koyama, Shinji; Honda, Yoshihito (april 2001). „Angiotensin II induces expression of the Tie2 receptor ligand, angiopoietin-2, in bovine retinal endothelial cells”. Diabetes. 50 (4): 867—75. PMID 11289054. doi:10.2337/diabetes.50.4.867..
- ^ Suzuki, Y., Ruiz-Ortega, M., Lorenzo, O., Ruperez, M., Esteban, V., & Egido, J. (2003). Inflammation and angiotensin II. Int. J. Biochem. Cell Biol., 35, 881–900.
- ^ Davis, M. D.; Fisher, M. R.; Gangnon, R. E.; Barton, F.; Aiello, L. M.; Chew, E. Y.; Ferris Fl, 3rd; Knatterud, G. L. (1998). „Risk factors for high-risk proliferative diabetic retinopathy and severe visual loss: Early Treatment Diabetic Retinopathy Study Report #18”. Invest Opthalmol Vis Sci. 39 (2): 233—252. PMID 9477980..
- ^ Qiao, Q.; Keinänen-Kiukaanniemi, S.; Läärä, E. (1997). „The relationship between hemoglobin levels and diabetic retinopathy”. J Clin Epidemiol. 50 (2): 153—158. PMID 9120508. doi:10.1016/S0895-4356(96)00335-6..
- ^ Larsson, L. I.; Alm, A.; Lithner, F.; Dahlén, G.; Bergström, R. (oktobar 1999). „The association of hyperlipidemia with retinopathy in diabetic patients aged 15-50 years in the county of Umeå”. Acta Ophthalmol Scand. 77 (5): 585—91. PMID 10551307. doi:10.1034/j.1600-0420.1999.770522.x..
- ^ „Hronične komplikacije dijabetesa”. Arhivirano iz originala 13. 11. 2007. g. Pristupljeno 25. 9. 2007.
- ^ S. Stefanović i saradnici: Specijalna klinička fiziologija, III izdanje ("Medicinska knjiga“ Beograd-Zagreb, 1980)
- ^ Loukovaara, Sirpa; Immonen, Ilkka J.; Yandle, Tim G.; Nicholls, Gary; Hiilesmaa, Vilho K.; Kaaja, Risto J. (februar 2005). „Vasoactive mediators and retinopathy during type 1 diabetic pregnancy”. Acta Ophthalmol Scand. 83 (1): 57—62. PMID 15715558. doi:10.1111/j.1600-0420.2005.00384.x..
- ^ Frank NR (1995). „Diabetic retinopathy”. Progress in Retinal and Eye Research. 14: 362—388..
- ^ H.-P. Hammes; M. Porta (2010). Experimental Approaches to Diabetic Retinopathy. Karger Medical and Scientific Publishers. ISBN 978-3-8055-9275-8.
- ^ a b v g Joyce Tombran-Tink; Barnstable, Colin J. (2007). Ocular Angiogenesis: Diseases, Mechanisms, and Therapeutics. Springer. ISBN 978-1-59745-047-8.
- ^ Barchetta, I.; Riccieri, V.; Vasile, M.; Stefanantoni, K.; Comberiati, P.; Taverniti, L.; Cavallo, M. G.; et al. (septembar 2011). „High prevalence of capillary abnormalities in patients with diabetes and association with retinopathy”. Diabet Med. 28 (9): 1039—44. PMID 21517956. S2CID 7718851. doi:10.1111/j.1464-5491.2011.03325.x. Pronađeni su suvišni parametri:
|author=i|last1=(pomoć) - ^ Shiba, T.; Takahashi, M.; Hori, Y.; Saishin, Y.; Sato, Y.; Maeno, T. (april 2011). „Relationship between sleep-disordered breathing and iris and/Or angle neovascularization in proliferative diabetic retinopathy cases”. Am J Ophthalmol. 151 (4): 604—9. PMID 21257149. doi:10.1016/j.ajo.2010.10.002.
- ^ Andou, N. (1988). „Clinical feature of central-type diabetic retinopathy and its management”. Rinshou Ganka. 42: 763—766.
- ^ Henkind, P. (1969). „Microcirculation of the peripapillary retina”. Trans Am Acad Ophthalmol Otolaryngol. 73 (5): 890—897. PMID 5357346.
- ^ Valsania P, Warram JH, Rand LI, Krolewski AS. (1993). „Different determinants of neovascularization on the optic disc and on the retina in patients with severe nonproliferative diabetic retinopathy.”. Arch Ophthalmol. 111 (2): 203—206. PMID 7679270. doi:10.1001/archopht.1993.01090020056023.
- ^ Frank, R. N. (2004). „Diabetic retinopathy”. NEJM. 350 (1): 48—58. PMID 14702427. doi:10.1056/NEJMra021678..
- ^ Klein, R.; Klein, B. E.; Moss, S. E.; Davis, M. D.; Demets, D. L. (1988). „Glycosylated hemoglobin predicts the incidence and progression of diabetic retinopathy”. JAMA. 260 (19): 2864—2871. PMID 3184351. doi:10.1001/jama.1988.03410190112033..
- ^ Klein, R.; Klein, B. E.; Moss, S. E.; Cruickshanks, K. J. (1998). „The Wisconsin Epidemiologic Study of Diabetic Retinopathy: XVII. The 14-year incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes”. Ophthalmology. 105 (10): 1801—1815. PMID 9787347. doi:10.1016/S0161-6420(98)91020-X..
- ^ Ferris FL III, Patz A. Macular edema: a complication of diabetic retinopathy. Surv Ophthalmol 1984; 28(Suppl.):452–461.
- ^ Antcliff, R. J.; Marshall, J. (1999). „The pathogenesis of edema in diabetic maculopathy”. Semin Ophthalmol. 14 (4): 223—232. PMID 10758223. doi:10.3109/08820539909069541..
- ^ Ciulla, T. A.; Amador, A. G.; Zinman, B. (2003). „Diabetic retinopathy and diabetic macular edema: Pathophysiology, screening, and novel therapies”. Diabetes Care. 26 (9): 2653—2664. PMID 12941734. doi:10.2337/diacare.26.9.2653.
- ^ a b Frank RN. Etiologic mechanisms in diabetic retinopathy. In: Ryan SJ, Schachat AP, eds. Retina, Vol. 2, Medical Retina. St. Louis: Mosby; (2001), str. 1259–1294.
- ^ Lorenzi, M. (2007). „The polyol pathway as a mechanism for diabetic retinopathy: Attractive, elusive, and resilient”. Experimental Diabetes Research. 2007: 61038. PMC 1950230
 . PMID 18224243. doi:10.1155/2007/61038
. PMID 18224243. doi:10.1155/2007/61038  .
.
- ^ Ross, R. (1999). „Atherosclerosis--an inflammatory disease”. New England Journal of Medicine. 340 (2): 115—26. PMID 9887164. doi:10.1056/NEJM199901143400207..
- ^ Lee, A. Y.; Chung, S. S. (1999). „Contributions of polyol pathway to oxidative stress in diabetic cataract”. FASEB J. 13 (1): 23—30. PMID 9872926. S2CID 624220. doi:10.1096/fasebj.13.1.23..
- ^ Tesfamariam, B. (1994). „Free radicals in diabetic endothelial cell dysfunction”. Free Radic Biol Med. 16 (3): 383—91. PMID 8063201. doi:10.1016/0891-5849(94)90040-X..
- ^ Greene DA, Stevens MJ. The sorbitol-osmotic and sor- bitol redox hypotheses. In: Le Roith D, Taylor SI, Olef- sky JM, eds. Diabetes Mellitus. Philadelphia: Lippincott- -Raven Publishers 1996.
- ^ Mizutani, M.; Kern, T. S.; Lorenzi, M. (1996). „Accelerated death of retinal microvascular cells in human and experimental diabetic retinopathy”. J Clin Inves. 97 (12): 2883—2890. PMC 507384
 . PMID 8675702. doi:10.1172/JCI118746..
. PMID 8675702. doi:10.1172/JCI118746..
- ^ Kern, T. S.; Engerman, R. L. (1981). „Distribution of aldose reductase in ocular tissues”. Exp Eye Res. 33 (2): 175—182. PMID 6791951. doi:10.1016/S0014-4835(81)80066-8..
- ^ Tilton, R. G.; Hoffmann, P. L.; Kilo, C.; Williamson, J. R. (1981). „Pericyte degeneration and basement membrane thickening in skeletal muscle capillaries of human diabetics”. Diabetes. 30 (4): 326—334. PMID 7202865. S2CID 45048301. doi:10.2337/diab.30.4.326..
- ^ Sorbinil Retinopathy Trail Research Group. A randomized trial of sorbinil, an aldose reductase inhibitor, in diabetic retinopathy. „A randomized trial of sorbinil, an aldose reductase inhibitor, in diabetic retinopathy. Sorbinil Retinopathy Trial Research Group”. Arch Ophthalmol. 108 (9): 1234—1244. 1990. PMID 2119168. doi:10.1001/archopht.1990.01070110050024..
- ^ Buzney SM, Frank RN, Varma SD,; et al. (1977). „Aldose reductase in retinal mural cells”. Invest Ophthal Visual Sci. 16: 392—396..
- ^ Kinoshita, J. H. (1986). „Aldose reductase in the diabetic eye. XLIII Edward Jackson memorial lecture”. Am J Ophthal. 102 (6): 685—692. PMID 3098107. doi:10.1016/0002-9394(86)90394-6..
- ^ Tanaka, S.; Avigad, G.; Brodsky, B.; Eikenberry, E. F. (1988). „Glycation induces expansion of the molecular packing of collagen”. J Mol Biol. 203 (2): 495—505. PMID 3143838. doi:10.1016/0022-2836(88)90015-0..
- ^ Charonis, A. S.; Reger, L. A.; Dege, J. E.; Kouzi-Koliakos, K.; Furcht, L. T.; Wohlhueter, R. M.; Tsilibary, E. C. (1990). „Laminin alterations after in vitro nonenzymatic glycosylation”. Diabetes. 39 (7): 807—814. PMID 2113013. S2CID 10939325. doi:10.2337/diab.39.7.807..
- ^ Vlassara, H.; Brownlee, M.; Cerami, A. (1985). „High-affinity-receptor-mediated uptake and degradation of glucose-modified proteins: A potential mechanism for the removal of senescent macromolecules”. Proc Natl Acad Sci USA. 82 (17): 5588—5592. Bibcode:1985PNAS...82.5588V. PMC 390596
 . PMID 2994035. doi:10.1073/pnas.82.17.5588
. PMID 2994035. doi:10.1073/pnas.82.17.5588  ..
..
- ^ a b v Esposito, C.; Gerlach, H.; Brett, J.; Stern, D.; Vlassara, H. (1989). „Endothelial receptor-mediated binding of glucose-modified albumin is associated with increased monolayer permeability and modulation of cell surface coagulant properties”. J Exp Med. 170 (4): 1387—1407. PMC 2189465
 . PMID 2551990. doi:10.1084/jem.170.4.1387..
. PMID 2551990. doi:10.1084/jem.170.4.1387..
- ^ Schiekofer, S.; Balletshofer, B.; Andrassy, M.; Bierhaus, A.; Nawroth, P. P. (2000). „Endothelial dysfunction in diabetes mellitus”. Semin Thromb Hemost. 26 (5): 503—511. PMID 11129406. S2CID 36815062. doi:10.1055/s-2000-13206..
- ^ Bucala, R.; Model, P.; Russel, M.; Cerami, A. (1985). „Modification of DNA by glucose 6-phosphate induces DNA rearrangements in an Escherichia coli plasmid”. Proc Natl Acad Sci USA. 82 (24): 8439—8442. Bibcode:1985PNAS...82.8439B. PMC 390931
 . PMID 3866232. doi:10.1073/pnas.82.24.8439
. PMID 3866232. doi:10.1073/pnas.82.24.8439  ..
..
- ^ Brownlee, M.; Vlassara, H.; Cerami, A. (1985). „Nonenzymatic glycosylation products on collagen covalently trap low-density lipoproteins”. Diabetes. 34 (9): 938—941. PMID 4029512. S2CID 22034243. doi:10.2337/diab.34.9.938..
- ^ Sensi, M.; Tanzi, P.; Bruno, M. R.; Mancuso, M.; Andreani, D. (1986). „Human Glomerular Basement Membrane: Altered Binding Characteristics following in Vitro Non-enzymatic Glycosylation”. Ann NY Acad Sci. 488 (1): 549—552. Bibcode:1986NYASA.488..549S. doi:10.1111/j.1749-6632.1986.tb46598.x..
- ^ Brownlee, M.; Vlassara, H.; Cerami, A. (1985). „Nonenzymatic glycosylation products on collagen covalently trap low-density lipoprotein”. Diabetes. 34 (9): 938—941. PMID 4029512. S2CID 22034243. doi:10.2337/diab.34.9.938..
- ^ Inoguchi T, Xia P, Kunisaki M, Higashi S, Feener EP, King GL. Insulin’s effect on protein kinase C and diacylglycerol induced by diabetes and glucose in vascular tissues. Am J Physiol 1994;267:E369–79.
- ^ Geraldes, P.; King, G. L. (2010). „Activation of protein kinase C isoforms and its impact on diabetic complications”. Circ Res. 106 (8): 1319—1331. PMC 2877591
 . PMID 20431074. doi:10.1161/CIRCRESAHA.110.217117..
. PMID 20431074. doi:10.1161/CIRCRESAHA.110.217117..
- ^ PKC-DRS2 Group; Aiello, L. P.; Davis, M. D.; Girach, A.; Kles, K. A.; Milton, R. C.; Sheetz, M. J.; Vignati, L.; Zhi, X. E. (decembar 2006). „Effect of ruboxistaurin on visual loss in patients with diabetic retinopathy”. Ophthalmology. 113 (12): 2221—30. PMID 16989901. doi:10.1016/j.ophtha.2006.07.032..
- ^ Avignon, A.; Sultan, A. (jun 2006). „PKC-B inhibition: A new therapeutic approach for diabetic complications?”. Diabetes Metab. 32 (3): 205—13. PMID 16799396. doi:10.1016/S1262-3636(07)70270-7..
- ^ Ishii, H.; Koya, D.; King, G. L. (1998). „Protein kinase C activation and its role in the development of vascular complications in diabetes mellitus”. J Mol Med. 76 (1): 21—31. PMID 9462865. doi:10.1007/s109-1998-8101-y..
- ^ Nagpala, P. G.; Malik, A. B.; Vuong, P. T.; Lum, H. (1996). „Protein kinase C B1 overexpression augments phorbol ester-induced increase in endothelial permeability”. J Cell Physiol. 166 (2): 249—255. PMID 8591984. S2CID 10077219. doi:10.1002/(SICI)1097-4652(199602)166:2<249::AID-JCP2>3.0.CO;2-P..
- ^ Williams, B.; Gallacher, B.; Patel, H.; Orme, C. (1997). „Glucose-induced protein kinase C activation regulates vascular permeability factor mRNA expression and peptide production by human vascular smooth muscle cells in vitro”. Diabetes. 46 (9): 1497—1503. PMID 9287052. S2CID 20037917. doi:10.2337/diab.46.9.1497..
- ^ Aiello LP, Bursell SE, Clermont A,; et al. (1997). „Vascular endothelial growth factor-induced retinal permeability is mediated by protein kinase C in vivo and suppressed by an orally effective B-isoform-selective inhibitor”. Diabetes. 43: 1473—1480..
- ^ Nishikawa, T.; Edelstein, D.; Du, X. L.; Yamagishi, S.; Matsumura, T.; Kaneda, Y.; Yorek, M. A.; Beebe, D.; Oates, P. J.; Hammes, H. P.; Giardino, I.; Brownlee, M. (2000). „Normalizing mitochondrial superoxide production blocks three pathways of hyperglycaemic damage”. Nature. 404 (6779): 787—790. Bibcode:2000Natur.404..787N. PMID 10783895. S2CID 4426750. doi:10.1038/35008121..
- ^ Suzuki, S.; Hinokio, Y.; Komatu, K.; Ohtomo, M.; Onoda, M.; Hirai, S.; Hirai, M.; Hirai, A.; Chiba, M.; Kasuga, S.; Akai, H.; Toyota, T. (1999). „Oxidative damage to mitochondrial DNA and its relationship to diabetic complications”. Diabetes Research and Clinical Practice. 45 (2–3): 161—168. PMID 10588369. doi:10.1016/S0168-8227(99)00046-7..
- ^ Giugliano, D.; Ceriello, A.; Paolisso, G. (1996). „Oxidative stress and diabetic vascular complications”. Diabetes Care. 19 (3): 257—267. PMID 8742574. S2CID 13639649. doi:10.2337/diacare.19.3.257..
- ^ Baynes JW. (1991). „Role of oxidative stress in development of complications in diabetes.”. Diabetes. 40: 405—412..
- ^ Anderson, H. R.; Stitt, A. W.; Gardiner, T. A.; Archer, D. B. (1995). „Diabetic retinopathy: Morphometric analysis of basement membrane thickening of capillaries in different retinal layers within arterial and venous environments”. Brit J Ophthal. 79 (12): 1120—1123. PMC 505353
 . PMID 8562548. doi:10.1136/bjo.79.12.1120..
. PMID 8562548. doi:10.1136/bjo.79.12.1120..
- ^ Ferrara N, Gerber HP (2002). „The role of vascular endothelial growth factor in angiogenesis”. Acta Haematol. 106 (4): 148—56. PMID 11815711. S2CID 46785882. doi:10.1159/000046610.
- ^ Aiello, L. P.; Avery, R. L.; Arrigg, P. G.; Keyt, B. A.; Jampel, H. D.; Shah, S. T.; Pasquale, L. R.; Thieme, H.; Iwamoto, M. A.; Park, J. E. (1994). „Vascular endothelial growth factor in ocular fluid of patients with diabetic retinopathy and other retinal disorders”. New England Journal of Medicine. 331 (22): 1480—1487. PMID 7526212. doi:10.1056/NEJM199412013312203.
- ^ Miller, J. W.; Adamis, A. P.; Aiello, L. P. (1997). „Vascular endothelial growth factor in ocular neovascularization and proliferative diabetic retinopathy”. Diabetes Metab Rev. 13 (1): 37—50. PMID 9134347. doi:10.1002/(SICI)1099-0895(199703)13:1<37::AID-DMR174>3.0.CO;2-K..
- ^ American Academy of Ophtalmology. Fundamentals and Principles of Ophtalmology, 2004-2005. San Francisco, California ;2004.
- ^ Cvetković D, Kontić Đ, Hentova-Senćanić P. Glaukom. Beograd. Zavod za udžbenike i nastavna sredstva; 1996.
- ^ Jurecka, T.; Bátková, Z.; Ventruba, J.; Synek, S. (2007). „Macular edema after cataract surgery in diabetic patients without retinopathy”. Cesk Slov Oftalmol. 63 (4): 274—84. PMID 17682607..
- ^ The United Kingdom Prospective Diabetes Study Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). „Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). UK Prospective Diabetes Study (UKPDS) Group”. Lancet. 352 (9131): 837—853. 1998. PMID 9742976. S2CID 7019505. doi:10.1016/S0140-6736(98)07019-6..
- ^ Chew, E. Y.; Klein, M. L.; Ferris Fl, 3rd; Remaley, N. A.; Murphy, R. P.; Chantry, K.; Hoogwerf, B. J.; Miller, D. (1996). „Association of elevated serum lipid levels with retinal hard exudate in diabetic retinopathy. Early Treatment Diabetic Retinopathy Study (ETDRS) Report 22”. Arch Ophthalmol. 114 (9): 1079—1084. PMID 8790092. doi:10.1001/archopht.1996.01100140281004..
- ^ Lyons, T. J.; Jenkins, A. J.; Zheng, D.; Lackland, D. T.; McGee, D.; Garvey, W. T.; Klein, R. L. (2004). „Diabetic retinopathy and serum lipoprotein subclasses in the DCCT/EDIC cohort”. Invest Ophthalm Vis Sci. 45 (3): 910—918. PMID 14985310. doi:10.1167/iovs.02-0648..
- ^ Miljanovic, B.; Glynn, R. J.; Nathan, D. M.; Manson, J. E.; Schaumberg, D. A. (2004). „A prospective study of serum lipids and risk of diabetic macular edema in type 1 diabetes”. Diabetes. 53 (11): 2883—2892. PMID 15504969. doi:10.2337/diabetes.53.11.2883..
- ^ Cusick, Michael; Chew, Emily Y.; Chan, Chi-Chao; Kruth, Howard S.; Murphy, Robert P.; Ferris, Frederick L. (2003). „Histopathology and Regression of Retinal Hard Exudates in Diabetic Retinopathy After Reduction of Elevated Serum Lipid Levels”. Ophthalmology. 110 (11): 2126—2133. PMID 14597519. doi:10.1016/j.ophtha.2003.01.001.
- ^ Uk Prospective Diabetes Study Group (1998). „Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38”. BMJ. 317 (7160): 703—713. S2CID 21224126. doi:10.1136/bmj.317.7160.703..
- ^ Misita RV. Dijabetička retinopatija. Zavod za udžbenike i nastavna sredstva Beograd 2000;21-38.
- ^ a b Nikolić Lj. Laseri u lečenju očnih bolesti. Naučna knjiga Beograd 1991;27-32
- ^ Vladislav Džinić, Ana Oros, Panretinalna laserfotokoagulacija u terapijskom pristupu dijabetesne retinopatije, Medicina danas 2010;9(1-3):45-50, UDC 617.73:616.379-008.64
- ^ Pavlović S. Laserfotokoagulacija u lečenju lezija makualrne regije. Doktorska disertacija. Novi Sad 1998.
- ^ a b Diabetic Retinopathy Clinical Research Network (septembar 2008). „A Randomized Trial Comparing Intravitreal Triamcinolone Acetonide and Focal/Grid Photocoagulation for Diabetic Macular Edema”. Ophthalmology. 115 (9): 1447—9. PMC 2748264
 . PMID 18662829. doi:10.1016/j.ophtha.2008.06.015.
. PMID 18662829. doi:10.1016/j.ophtha.2008.06.015.
- ^ Avitabile, T.; Longo, A.; Reibaldi, A. (2005). „Intravitreal triamcinolone compared with macular laser grid photocoagulation for the treatment of cystoid macular edema”. Am J Ophthalmol. 140 (4): 695—702. PMID 16226521. doi:10.1016/j.ajo.2005.05.021..
- ^ Manzano, R. P.; Peyman, G. A.; Khan, P.; Kivilcim, M. (mart 2006). „Testing intravitreal toxicity of bevacizumab (Avastin)”. Retina. 26 (3): 257—261. PMID 16508423. S2CID 7598237. doi:10.1097/00006982-200603000-00001..
- ^ Patel, P. J.; Zaheer, I.; Karia, N. (2008). „Intravitreal triamcinolone acetonide for macular oedema owing to retinal vein occlusion”. 2002. 109 (1): 920—7. PMID 16902493. S2CID 20717757. doi:10.1038/sj.eye.6702518.
- ^ Wingate RJ; Beaumont PE (januar 1999). „Intravitreal triamcinolone and elevated intraocular pressure”. Aust N Z J Ophthalmol. 27 (6): 431—432. PMID 10641903. doi:10.1046/j.1440-1606.1999.00238.x..
- ^ Jonas, J. B.; Kreissig, I.; Degenring, R. (februar 2003). „Intraocular pressure after intravitreal injection of triamcinolone acetonide”. Br J Ophthalmol. 87 (1): 24—27. PMC 1771462
 . PMID 12488256. doi:10.1136/bjo.87.1.24..
. PMID 12488256. doi:10.1136/bjo.87.1.24..
- ^ Bakri, S. J.; Beer, P. M. (oktobar 2003). „The effect of intravitreal triamcinolone acetonide on intraocular pressure”. Ophthalmic Surg Lasers Imaging. 34 (5): 386—390. PMID 14509462. doi:10.3928/1542-8877-20030901-08..
- ^ Jager, R. D.; Aiello, L. P.; Patel, S. C.; Cunningham Jr, E. T. (2004). „Risks of intravitreous injection: A comprehensive review”. Retina. 24 (5): 676—698. PMID 15492621. doi:10.1097/00006982-200410000-00002.
- ^ Diabetic Retinopathy Clinical Research Network (2005). „A Randomized Trial Comparing Intravitreal Triamcinolone Acetonide and Focal/Grid Photocoagulation for Diabetic Macular Edema”. Eur J Ophthalmol. 15 (9): 462—4. PMC 2748264
 . PMID 18662829. doi:10.1016/j.ophtha.2008.06.015.
. PMID 18662829. doi:10.1016/j.ophtha.2008.06.015.
- ^ Benz, M. S.; Murray, T. G.; Dubovy, S. R.; Katz, R. S.; Eifrig, C. W. (2003). „Endophthalmitis caused by Mycobacterium chelonae abscessus after intravitreal injection of triamcinolone”. Arch Ophthalmol. 121 (2): 271—273. PMID 12583797. doi:10.1001/archopht.121.2.271.
- ^ Rosenfeld, Philip J.; Moshfeghi, Andrew A.; Puliafito, Carmen A. (jul 2005). „Optical coherence tomography fi ndings after an intravitreal injection of bevacizumab (avastin) for neovascular age-related macular degeneration”. Ophthalmic Surg Lasers Imaging. 36 (4): 331—335. PMID 16156152. doi:10.3928/1542-8877-20050701-14..
- ^ Bakri, S. J.; Cameron, J. D.; McCannel, C. A.; Pulido, J. S.; Marler, R. J. (2006). „Absence of histologic retinal toxicity of intravitreal bevacizumab in a rabbit model”. Am J Ophthalmol. 142 (1): 162—164. PMID 16815270. doi:10.1016/j.ajo.2006.03.058..
Literatura[uredi | uredi izvor]
- Browning, David J. (2010). Diabetic Retinopathy: Evidence-Based Management. Springer. str. 1—10. ISBN 978-0-387-85900-2.
- Duh, Elia (2008). Diabetic Retinopathy. Springer. ISBN 978-1-59745-563-3.
- Joyce Tombran-Tink; Barnstable, Colin J. (2007). Ocular Angiogenesis: Diseases, Mechanisms, and Therapeutics. Springer. ISBN 978-1-59745-047-8.
- H.-P. Hammes; M. Porta (2010). Experimental Approaches to Diabetic Retinopathy. Karger Medical and Scientific Publishers. ISBN 978-3-8055-9275-8.
- Duh, Elia (2008). Diabetic Retinopathy. Springer. ISBN 978-1-59745-563-3.
- Jose Cunha-vaz (2011). Diabetic Retinopathy. World Scientific. ISBN 978-981-4304-43-6.
- Korobelnik JF, Do DV, Schmidt-Erfurth U, Boyer DS, Holz FG, Heier JS; et al. (novembar 2014). „Intravitreal aflibercept for diabetic macular edema”. Ophthalmology. 121 (11): 2247—54..
- Arevalo JF, Garcia-Amaris RA (februar 2009). „Intravitreal bevacizumab for diabetic retinopathy”. Curr Diabetes Rev. 5 (1): 39—46.. .
- Rodriguez-Fontal M, Alfaro V, Kerrison JB, Jablon EP (februar 2009). „Ranibizumab for diabetic retinopathy”. Curr Diabetes Rev. 5 (1): 47—51..
- FDA Drug and Safety Alerts. FDA Alerts Health Care Professionals of Infection Risk from Repackaged Avastin Intravitreal Injections. August 30, 2011. Available at [1]
- Meredith TA. Clinical Trials in Ophthalmology-A Summary and Practice Guide. Kertes C, ed. The diabetic vitrectomy study. 1998. 37-48.
- [Guideline] American Diabetes Association. 10. Microvascular Complications and Foot Care: Standards of Medical Care in Diabetes-2018. Diabetes Care. 2018 Jan. 41 (Suppl 1):S105-18.
- Lu L, Jiang Y, Jaganathan R, Hao Y. Current Advances in Pharmacotherapy and Technology for Diabetic Retinopathy: A Systematic Review. J Ophthalmol. 2018. 2018:1694187.
- Baker CW, Jiang Y, Stone T (maj 2016). „Recent advancements in diabetic retinopathy treatment from the Diabetic Retinopathy Clinical Research Network”. Curr Opin Ophthalmol. 27 (3): 210—6..
Spoljašnje veze[uredi | uredi izvor]
| Klasifikacija | |
|---|---|
| Spoljašnji resursi |
- „Bolest malih krvnih sudova – dijabetesna mikroangiopatija”. Arhivirano iz originala 06. 01. 2014. g.
- Simple Anatomy of the Retina. Webvision, The Organization of the Retina and Visual System (jezik: engleski)
- „Diabetic Retinopathy”. Arhivirano iz originala 12. 05. 2014. g. Resource Guide from the National Eye Institute (NEI). (jezik: engleski)
- „National Diabetes Information Clearinghouse”. Arhivirano iz originala 21. 02. 2010. g. (jezik: engleski)
- NHS Diabetic Eye Screening Programme (jezik: engleski)
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |








