Oksidativni stres
| Oksidativni stres | |
|---|---|
| Klasifikacija i spoljašnji resursi |
Oksidativni stres je stanje u organizmu u kome postoji neravnoteža između stvaranja slobodnih radikala i njihovog neutralisanja od strane antioksidativne zaštite organizma, odnosno kada prooksidansi (slobodni radikali) nadvladaju mehanizme antioksidativne zaštite organizma. Najčešće nastaje u uslovima kada u organizmu postoji povećana produkcija slobodnih radikala i smanjena sposobnost organizma za njihovu neutralizaciju, odnosno kada je stanje ravnoteže između prooksidanas i antioksidanasa pomomereno u pravcu prooksidanasa.
Za oksidativni stres se može reći da je on normalna pojava, odnosno da je prisutan i kod zdravih osoba jer je usko povezan sa starenjem. [1]. Proces oksidacije je deo regulatornog biohemijskog funkcionisanja naših tela u procesu stvaranja energije koja nam je neophodna za život. Tokom ovih procesa stvaraju se slobodni radikali koji imaju svoje fiziološke pozitivne funkcije [2][3] .
Problem nastaje kada se poremeti fina ravnoteža i kada otkažu prirodni mehanizmi odbrane pa nivo slobodnih radikala počne da prevazilazi kapacitet organizma da ih neutrališe, što menja oksidativni status i telo ulazi u zonu povećanog oksidativnog stresa, ili stanje visokog rizika za nastajanje najrazličitijih poremećaja i bolesti.
Štetno dejstvo slobodnih radikala u oksidativnom stresu, prema shvatanju savremene medicine, ogleda se u nastanku mnogih akutnih i hroničnih bolesti koji se klinički manifestuju kao akutni i hronični zapaljenjski procesi (reumatoidni artritis, vaskulitis), neurološki poremećaji (Alchajmerova bolest, Parkinsonova bolest, cerebrovaskularna oštećenja, mišićna distrofija), kardiovaskularni poremećaji (hipertenzija i hipertenzivna bolest srca, ateroskleroza), fibroza pluća, katarakta, maligne bolesti, ali i mnoga druga stanja koja se nazivaju prerano starenje [3].
Osnovni pojmovi[uredi | uredi izvor]
Slobodni radikali su nestabilni molekuli, velike reaktivnosti, koji u organizmu stupaju u hemijske reakcije sa delovima ćelije (proteinima, lipidima, ugljenim hidratima, molekulima DNK) pri čemu dovode do biohemijskih, strukturnih, funkcionalnih poremećaja.
Antioksidansi su materije koje pomažu organizmu da smanjenji oštećenja nastala dejstvom slobodnih radikala.
U unutrašnje (endogene) izvore odnosno unutrašnje uticaje koji izazivaju povećano stvaranje slobodnih radikala u organizmu spadaju; stres, imunska odbrana, zapaljenja, povrede, veliko fizičko opterećenje. Glavni izvori endogenih radikala u navedenim uticajima dele se na enzimske i neenzimske;
| Enzimski izvori | Nenzimski izvori |
|---|---|
|
|
Egzogeni izvori radikala
U spoljne (egzogene) izvore odnosno spoljne uticaje koji izazivaju povećano stvaranje slobodnih radikala u organizmu spadaju; duvanski dim, lekovi, način ishrane, neka terapijska i okolna zračenja [4] pa čak i fizička aktivnost .

- ENDOGENI I EGZOGENI IZVORI RADIKALA
Ova bolest podrazumeva poremaćaj u organizmu u čijoj etiologiji primarnu ulogu imaju slobodni radikali, a za koju postoji obilje okolnosti i dokaza. Najverovatnije da slobodni radikali delujući kao posredne supstance u inflamatorni procesima, možda čak i kao neuromodulatori, utiču na pojavu bolesti [5].
Ipak, postoje i zaštitni mehanizmi koji su dovoljni da aktivne vrste radikala koriste za neke normalne fiziološke procese. Skoro sigurno je da tu spada i antimikrobna odbrane i ksenobiotički metabolizam.
Posledice i uzroci oksidativnog stresa[uredi | uredi izvor]
| Uzroci oksidativnog stresa | Posledice oksidativnog stresa |
|---|---|
|
|
Efekti oksidanasa na makromolekule[uredi | uredi izvor]
Belančevine[uredi | uredi izvor]
Belančevine imaju mnogo reaktivnih mesta gde se mogu javiti oštećenja oksidativnim stresom[6];
- Prvo, agresivni radikali kao što je hidroksil radikal mogu razgraditi belančevine u plazmi, i tada se razgrađeni proizvodi specifičnih belančevine mogu detektovati, ako su poznati, što se zasniva na udruženim reakcijama na specificnim amino kiselinama kao što je prolin i histidin.
- Drugo, belančevine mogu sadržati mesta sa vezanim metalom koja su posebno osetljiva na oksidativne reakcije kroz interakciju sa metalima, što obično dovode do ireverzibilne modifikacije amino kiselina koje su uključene u vezivanje metalnih jona, na primer histidina.
Navedene modifikacije mogu stvoriti signalne sekvence koje prepoznaju specifične ćelijske proteaze koje degradiraju takve belančevine. Konačno, mnoge intraćelijske belančevine imaju reaktivne sulfhidrilne grupe na specifičnim ostacima cisteina koje mogu biti modifikovane (oksidovani) do specifičnih formi (disulfida) koji opet mogu biti redukovani u metaboličkim procesima. Takođe neke belančevine imaju reaktivni metionin koji može da podlegne reverzibilnoj modifikaciji do metionin sulfoksid. Reverzibilna priroda modifikacije cisteina i metionina ukazuje da oksidativna modifikacija ovog tipa može imati ulogu u regulatornim metaboličkim događajima u ćeliji u oksidativnom stresu [6].
Nukleinske kiseline[uredi | uredi izvor]
Nukleinske kiseline su pentoze-fosfatni polimeri koji mogu podleći reakciji sa hidroksil radikalom. Ove osnovne modifikacije mogu biti odgovorne za genetske defekte produkovane oksidativnim stresom. Oštećenje DNK se takođe može proceniti pomoću kidanja lanaca i modifikacije baza u ćelijama u kulturi koje su pod oksidativnim stresom. Važan metabolički efekat oštećenja DNK je brza indukcija poliadenozin-difosfat-riboza-sintaze u jedru, rezultujući izrazitim trošenjem ćelijskih rezervi NADH.
Lipidi[uredi | uredi izvor]
Lipidna peroksidacija polinezasićenih lipida je proces gde nezasićen lipid stupa u reakciju sa hidroksilnim radikalom pri čemu se izdvaja voda i nastaje lipidni radikal koji potom u reakciji sa kiseonikom daje lipidni peroksil radikal, a on sa novim nezasićenim lipidima daje lipidni peroksid. Ova oksidacija pogađa lipide koji ulaze u sastav namirnica ozbiljno narušavajući miris hrane. Peroksidacija membranskih lipida uglavnom se javlja kao posledica oksidativnog stresa u intaktnoj ćeliji, ali i neki sastojci ishrane mogu direktno biti ugrađeni u ćelijske strukture.
| „ | Lipidna peroksidacija je radikalski inicirana lančana reakcija koja je samopropagirajuća u ćelijskoj membrani. Kao posledica, izolovane oksidativne reakcije mogu imati duboke efekte na funkciju membrane. Proizvodi lipidne peroksidacija se lako detektuju u krvnoj plazmi i koriste se za merenje oksidativnog stresa. Najčešće se određuje koncetracija malonaldehida koji nastaje iz lipidnih peroksida u procesu lipidne peroksidacija. | ” |
Patogeneza[uredi | uredi izvor]
Na osnovu mnogobrojnih istraživanjlja smatra se da su slobodni radikali odgovorni za nastanak akutnih i hroničnih poremećaja koji se manifestuju kao zapaljenjijski procesi, neurološki poremećaji, kardiovaskularni poremećaji, maligne bolesti.
Slobodni radikali ili reaktivna jedinjenja kiseonika (ROS) i reaktivna jedinjenja azota (RNS) su izrazito reaktivni molekuli koji se prirodno javljaju kao produkti normalnih ćelijskih oksidativnih procesa. Koncetracije reaktivnih jedinjenja kiseonika se može povećati do visokih nivoa u nekim patološkim procesima ali tamo gde postoji deficit antioksidanasa, i mogu reagovati sa ćelijskim konstituentima i izazvati ostećenje, poremećaj funkcija ili propadanje ćelija.
Brojni dokazi povezuju reaktivna jedinjenja kiseonika sa patološkim oštećenjima koja se viđaju u bolestima kao sto su kancer, ateroskleroza, koje mogu nastati od oštećenja DNK, oksidativne modifikacije proteina i izmene lipidne strukture. Delovanjem slobodnih radikala aktiviraju se mnogobrojne strukture u ćeliji pri cemu nastaje čitav niz kaskadnih reakcija, što za posledicu ima i generisanje novih količina slobodnih radikala (nastaje tzv sindrom "začaranog kruga").
Aktivacijom lipida, dolazi do aktiviranja transkripcionog faktora-NFkB, što posledično dovodi do rasta nivoa hemokina i citokina kao medijatora zapaljenja. Ove signalne molekule dovode do povećane ekspresije adhezionih molekula (ushodna regulacija), kako na površini ćelija endotela (selektini), tako i na površini samih inflamatornih ćelija (integrini). Time je omogućen direkten kontakt i vezivanje ćelija imunskog sistema za povrsšinu endotela. Nakon toga, ćelije imunog odgovora prodiru u subendotelni prostor. Imune ćelije kao što su: neutrofili, eozinofili i makrofage, poseduju na svojoj membrani NADPH oksidazu. Ovaj enzim u kontaktu sa kiseonikom doprinosi stvaranju superoksidnog anjona. Nastali slobodni radikal biva uklonjen dejstvom superoksid-dizmutaze tokom vrlo kratkog vremenskog perioda. To je razlog što on ne penetrira kroz ćelijsku membranu. Međutim, nastali vodonik-peroksid lako difunduje u okolne ćelijske strukture. Time dovodi do aktiviranja intraćelijskih signalnih puteva, kao i do generisanja reaktivnih vrsta kiseonika. Time se na primarnu fazu generisanja oksidativnog stresa od strane slobodnih radikala, nadovezuje sekundarna faza-zapaljenja, koja nastali stres samo produbljuje. Oksidativna oštećenja lipoproteina male gustine (LDL) reaktivnim jedinjenjima kiseonika su između ostalog i jedan od uzroka ateroskleroze.
Reaktivne vrste kiseonika[uredi | uredi izvor]
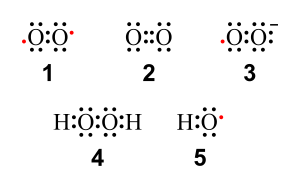
1 - tripletni kiseonik;
2 - singletni kiseonik;
3 - superoksid;
4 - vodonik peroksid;
5 - hidroksilni radikal
Među reaktivnim vrstama kiseonika (ROS), u biološkom smislu, posebno su značajne sledeće vrste reaktivnih jedinjenja kiseonika; [7]
- O2•— - superoksid ili superoksidni anjonski radikal,
- H2O2 - vodonik-peroksid,
- OH•— - hidroksilni radikal,
- RO2• - peroksilni-radikal,
- RO2• - perhidroksilradikal,
- RO-• - aloksilni radikal,
- ROOH• - hidroperoksid,
- HClO- - hipohloritna kiselina,
- O3 - ozon,
- 1ΔgO2 - singlentni kiseonik.
Superoksidni anjon radikal nastaje u mitohondrijama redukcijom kiseonika jednim elektronom. Ovaj radikal ima dominatno štetno dejstvo: indukuje lipidnu peroksidaciju i oštećuje ćelijske membrane. U fiziološkim uslovima ne izaziva toksične efekte jer ga enzim superoksid - dismutaza (SOD) transformiše u manje aktivan vodonik-peroksid [8].
Vodonik-peroksid se u ćelijama obrazuje redukcijom molekula kiseonika sa dva elektrona, pri čemu je reakcija katalizovana brojnim oksidazama. Iako se ne može definisati kao slobodni radikal jer nema nesparenih elektrona, i predstavlja najstabilniji intermedijarni produkt redukcije kiseonika, vodonik-peroksid ipak ispoljava neke toksične efekte. To se pre svega odnosi na poremećaj u deponovanju kalcijuma u mitohondrijama, sa konsekutivnim nagomilavanjem kalcijuma u citosolu i gubitkom sulfhidrilnih grupa belančevina: ovo je kritičan događaj u genezi ćelijskih oštećenja u oksidativnom stresu. Relativno visoke koncentracije vodonik-peroksida koje se oslobađaju na mestu bilo kog zapaljenja ali i u različitim nezapaljenjskim ćelijama (fibroblasti, hondrociti, endotel) pod dejstvom citokina kakvi su npr IL-1 ili TNF-α. Ćelije takođe imaju mogućnosti i da se štite od vodonik-peroksida snažnim enzimskim sistemima: katalazom u peroksizomima i glutation-peroksidazom u mitohondrijama [9].
Hidroksilni radikal je najreaktivniji intermedijarni produkt delimične redukcije kiseonika. Ako se vodonik-peroksid ne ukloni katalaza, može da reaguje sa fero jonima i formira potentnije KSR, kakav je hidroksilni radikal (Fenton reakcija). On, in situ, oštećuje mitohondrijalnu membranu (izazivajući gubitak produkcije ATP i energije), oštećuje DNK, oštećuje membranu ćelije modifikujući membranske belančevine i izaziva lipidnu peroksidaciju - što je dovoljno za ireverzibilno uništenje ćelije [10].
Singletni kiseonik nastaje dovođenjem energije u kiseonik s ciljem menjanja spina jednog od elektrona, što značajno uvećava njegovu reaktivnost. Takođe može da iskaže značajnu toksičnost u različitim biološkim sistemima [11].
Reaktivna jedinjenja azota[uredi | uredi izvor]
Ovo jedinjenje je univerzalni regulator metabolizma, koje učestvuje u mnogobrojnim funkcijama, a pored regulatorne funkcije učestvuje u imunskom odgovoru ćelije. Funkcija NO je zavisna od redoks forme. Redoks ravnoteža u zidu krvnoih sudova održava se zahvaljujući istovremenom prisustvu oksidanasa i antioksidanasa.
U glatkim mišićnim ćelijama i makrofagima stvaraju se superoksidni anjoni vodonik-peroksid koji oksiduje LDL i aktiviraju faktore transkripcije NF-kB koji je osetljiv na oksidaciju. Iz vode u prisustvu jona metala stvaraju se hidroksilni radikali.
Ćelijski antioksidativni mehanizmi uključuju aktivnost sledećih jedinjenja: azot-monoksida, glutantiona, superoksiddizmutaze i katalaze. Dakle u zavisnosti od okruženja NO se može naći na različitim stranama reakcije.
Peroksinitrit je jak oksidans koji napada cistein i metionin u proteinima. On takođe reaguje sa tirozin iz proteina adicijom NO2 u prsten ove aminokiseline. Pored toga NO se adira i formira S-nitrozo tiole. Sulfhidrilna grupa se u ovoj reakciji obično oksidiše jednim elektronom i naredna reakcija sa redukovanim tiolom vodi stvaranju disulfida [12].
Oksidativni stres u pojavi bolesti[uredi | uredi izvor]
Brz tempo života, kao i veliki stresni uticaji koji su sve više zastupljeni u svakodnevom životu, dovode do sve veće propagacije oksidativnog stresa, a samim tim i do pojave; srčanih oboljenja, neurodegenerativnih oboljenja, respiratornih oboljenja, oboljenja lokomotornog aparata, i pojave tumora, u čijoj osnovi može biti oksidativni stres.
Iako još uvek nemamo dovoljno dokaza na koji se način se može kontrolisati oksidativni stres, o tome postoji veći broj teorija.
| „ | Delovanje oksidativnog stresa lako se može porediti sa pritiskom vode koja protiče niz pukotinu na zidu; polako ali sigurno napraviće veća oštećenja ukoliko se na vreme ne sanira pukotina. Zato razlika u tretmanu oksidativnog stresa zavisi od toga koliko i gde treba delovati, da bi sanacija „pukotine“ bila efektivna i blagovremena. | ” |
Prema brojnim naučnim saznanjima, pojava oksidativnog stresa dovodi do trajnog oštećenja delova ćelija, što ima za posledicu pojavu najrazličitijih hroničnih bolesti ili razvoj tumora. Smatra se da su mitohondrije (ćelijske organele odgovorne za disajne procese ćelija) izvor, a ujedno i cilj stvorenih reaktivnih vrsta kiseonika (slobodnih radikala).
Zajednička pitanja o ulozi oksidativnog stresa u patogenezi pojedinih oboljenja su očigledna, ali nameću se i brojna druga pitanja pa i dileme [13] [14][15];
- Prvo pitanje je, da li je oksidativni stres uzrok ili posledica bolesti? To je složeno akademsko pitanje, jer ako je oksidativni stres samo posledica, postavlja se pitanje da li oksidativni stres može biti terapijski cilj kod ovih oboljenja.
- Drugo pitanje je koja je etiologija oksidativnog stresa? Zajedničko za ova oboljenja su poremećaji mitohondrija i narušavanje homeostaze redoks-aktivnih metala.
- Treće pitanje, je, kakav je odnos između oksidativnog stresa i drugih aspekata patogeneze osksidativnim stresom izazvanih oboljenja? Za većinu ovih bolesti pitanja su složena i uglavnom nerešena, etiologija multifaktorijalna, a oksidativni stres se prepliće sa drugim mehanizmima bolesti.
Oksidativni stres u pojavi tumora[uredi | uredi izvor]
Poznato je da je oksidativni stres široko rasprostranjen u ćelijama tumora koji potiču od različitih tipova tkiva. Ispitivanja su pokazala da postoji direktna povezanost između stvaranja reaktivnih vrsta kiseonika (engl. Reactive oxygen species) (ROS), ROS-signalizacije i sa ROS-om izazvanim stresom i karcinogenezom. Pod uticajem određenih onkogenih signala, ćelije povećavaju stvaranje ROS-a, što se delimično odnosi na aktivne metaboličke aktivnosti povezane sa nekontrolisanim rastom ćelija i proliferacijom. Egzogeni izvori ROS-a, kao što su na primer zračenje i određeni tipovi hemikalija, isto tako mogu da povećaju oksidativni stres u ćelijama.
Oksidativni stres može da dovede do trošenja ćeliskih antioksidansa i redoks disbalansa. Uvećanje ćelijskih ROS-a mogu doprineti pojavi, promociji i progresiji tumora na više nivoa. Na primer, ROS može da stimuliše ćelisku proliferacija i da aktivira puteve preživljavanja preko signalnih mehanizama.
ROS može, isto tako da direktno izazove oštećenja DNK, što dovodi do njene mutacije. Oksidacija gvanina na poziciji C8, što dovodi do stvaranja 8-hidroksiguanozina, verovatno je najčešće mutageno oštećenje. Ovo oksidativno DNK oštećenje može da izazove promenu, koja se često nalazi u mutiranim onkogenima i tumor supresornim genima. Za ova mutacijski oštećenja zna se da učestvuju u mehanizmima stvaranja tumora, genetske nestabilnosti i napredovanja bolesti.
Mitohondrije predstavljaju glavni endogeni izvor ROS-a, zbog elektronskog dvojnog deljenja u kompleksima 1 i 3 respiratornog lanca. Pošto mitohondrijalna DNK (mtDNK) kodira 13 proteinskih komponenata respiratornog lanca i fizički je u neposrednoj blizini mestu stvaranja ROS -a, oštećenje mtDNK od ROS-a može da izazove defekte na respiratornom lancu, proticanje elektrona više i dalje povećanje stvaranja ROS-a. Ovaj čvor koji dovodi do povećanja stvaranja ROS-a može da odigra značajnu ulogu u izazivanju endogenog stresa (ROS) i da doprinese genetskoj nestabilnosti i progresiji tumora. Uvećanje ćelijinih nivoa ROS-a i njihova povezanost sa mutacijom mitohondrialni DNK, zabeleženi su u primarnim ćelijama tumora izolovani kod pacijenata koji boluju od leukemije.
Uvećanje oksidativnog stresa u područjima sa tumorima, može da ima značajne terapijske implikacije:
- Sa jedne strane, genetska nestabilnost povezana sa ROS posredovano oštećenje DNK, može da obezbedi mehanizam za razvoj subklonova tumorskih ćelija koji su otporni na delovanje lekova.
- Sa druge strane, uvećani ROS stres u tumorskim ćelijama, može da ih napravi podložnijim za dalje oksidativno oštećenje od strane egzogeno izazvanog stvaranja ROS-a.
Ovo može da obezbedi biohemiski osnovu za razvoj novih terapeutskih strategija sa kojima bi se omogućilo potpuno uništenje na tumorskih ćelija. Razumljivo je da postojano uvećanje ROS-a pod dejstvom stresa u velikoj meri može da iscrpi ćelijski antioksidantni kapacitet u tumorskim ćelijama, tako da bilo kakvo dalje stvaranje ROS-a pod dejstvom spoljašnjih protivtumorskih agensa izazvaće programiranu ćelijsku smrt tumorske ćelije.
Oksidativni stres u pojavi autoimunih oboljenja[uredi | uredi izvor]
Isto tako, oksidativni stres igra značajnu ulogu u pojavi autoimunih oboljenja. Kao što je poznato, u razvoju autoimunih oboljenja značajni doprinos imaju kako genetska osnova, tako i uslovi spoljašnje sredine. Infekcije, UV zračenje, temperaturne promene, kao i emocionalni stres, predstavljaju deo faktora koji dovode do pojave autoimunih bolesti.
Uopšteno, oksidativni stres deluje direktno na imune ćelije. Na individualnom nivou, različiti tipovi stresa utiču na neuro-endokrino-imonološku osu. Infekcije ili zapaljenja aktiviraju monocite i neutrofile, koji stvaraju veliku količinu ROS-a, koji pak sa svoje strane dovode do narušuvanja homeostaze imunskog sistema. Oksidativni stres igra važnu ulogu u patogenezi autoimunih bolesti, preko ponovnog aktiviranja procesa zapaljenja, programirana ćelijska smrt, modifikacija sopstvenih protivgena i narušvanje imunološke tolerancije.
Oksidativni stres u pojavi programirane ćelijske smrti (apoptoza)[uredi | uredi izvor]
Oksidativni stres isto tako aktivira i programiranu ćelijsku smrt (apoptoza) kao rezultat UV zračenja, tumora, nekrotiziranog faktora alfa (TNF-α) i virusnih infekcija. Isto tako, DNK molekul, može da pretrpi velika oštećenja u svojoj strukturi, kao rezultat oksidativnog stresa. Održavanje pravilnog redoks balansa ćelije (redukcija — oksidacija) e od presudne važnosti za normalni rad ćelije, koja obuhvata ćelijsku varijabilnost, signalizaciju, aktivaciju i proliferaciju.
Zaštitni mehanizmi od oksidativnog stresa[uredi | uredi izvor]
Kako smo onda živi i što nas čuva od oksidativnog stresa i slobodnih radikala ili ROS-a? Za svaki onaj sistem koji neutrališe slobodne radikale ili sprečava njihovo nastajanje, kažemo da deluje kao antioksidantni sistem ili antioksidans.
U nekom smislu možemo reći da su antioksidansi i slobodni radikali u oksidativnom stresu kao „lice i naličje“, na način na koji povezujemo vatru i vatrogasce.
Štetni efekti oksidativnog stresa su uravnoteženi od strane kompleksnih antioksidantnih sistema, u koje spadaju;
Enzimski antioksidansi[uredi | uredi izvor]
U enzimske antioksidanse spadaju u celularni antioksidansi. Nalaze se u zdravima arterijama, u ćelijama arterijskih zidova, dok je ekstracelularne tečnosti siromašna enzimskim antioksidansima;
- Superoksid dizmutaza (SOD)
- Katalaza
- Glutation peroksidaza
- Glutation reduktaze i transferaze
- Tiol-disulfid oksidoreduktaze
- Peroksiredoksini
Neenzimska antioksidativna zaštita[uredi | uredi izvor]
U neenzimske antioksidanse spadaju i antioksidansi koji primarno zadržavaju potencijalno opasne jone gvožđa i bakra u svojoj neaktivnoj formi, i na taj način onemogućavaju njihovo učešće u produkciji slobodnih radikala;
- Transferin
- Feritin
- Laktoferin
- Hematoglobin i hemopeksin
- Albumin
- Glutation
- Askorbinska kiselina
- Α-tokoferol
- Ubihinon CoQ10H2
- β-karoten
- Mokraćna kiselina
- Bilirubin
Ojačani lipidi[uredi | uredi izvor]
Ojačani lipidi su lipidni molekuli u kojima neke od masnih kiselina sadrže deuterijum umesto vodonika. Mogu se koristiti za zaštitu živih ćelija usporavanjem lančane reakcije zbog izotopskog dejstva na peroksidaciju lipida.[16]
Izvori[uredi | uredi izvor]
- ^ a b Živković.M, izdavač. Hiperbarična i podvodna medicina.Beograd: HBO medical center ; Nauka, 1998. 251 str. ID=55440652
- ^ (jezik: engleski) Ferreira AR, Bonatto F, Pasquali MA, Polydor M, et al. Oxidative stress effects on the central nervous system of rats after acute exposure to ultra-high frequency electromagnetic fields.Bioelectromagnetics 27:487-493.(2006)
- ^ a b (jezik: engleski)Halliwell B. Oxydants and human disease: some mew consepts FFASEBJ.1 358-364;1987
- ^ (jezik: engleski)Hoyt A, Luukkonen J, Juutilainen J, Naarala J. (2008) Title Proliferation, Oxidative Stress and Cell Death in Cells Exposed to 872 MHz Radiofrequency Radiation and Oxidants. Journal Radiat Res. 170 (2) :235-243.
- ^ Huber, W., Future trends in radical studies, in Inflammation — Mechanisms and Treatment, Willoughby, P. A. and Giroud, J. P., Eds., University Park Press, Baltimore, 1980, 27.
- ^ a b Saltman B Oxidative stress: a radical view, Seninars Hematol. 26, 249-256, 1989
- ^ (jezik: hrvatski)Marijan K. ,i Marta K. Djelovanje gemfibrozila na oksidativni stres u tkivima srca i jetre Wistar i Fischer štakora, Sveučilište u Zagrebu Medicinski fakultet, Zagreb, 2009.
- ^ Gucrnouri L. Artur Y, Hcrbcth B. et al. Biological variability of superoxide dismutase, glutathione peroxidase and catalase in blood. Clin Chern 1991:37: 1932-7
- ^ Koračevic D. Dijagnostički važni enzimi. U: Koračеvic D i sar. Biohemija. Beograd: Savremena adirnistracija: 1996:96-157
- ^ Pavlovic D. Bioloska oksidacija. U: Koračеvic D i sar. Biohemija. Beograd: Savremena adimistracija; 1996:678-705
- ^ Živić S, i sar. ZNAčAJ OKSIDATIVNOG STRESA U NASTANKU DIJABETESA TIPA 1 - ODREĐIVANJE AKTIVNOSTI KATALAZE U LIMFOCITIMA OBOLELIH, Med Pregl 2008; LXI (9-10): 458-463. Novi Sad: septembar-oktobar. UDK 616.379-008.64-02
- ^ Slavica Spasić, Zorana Jelić-Ivanović, Vesna Spasojević-Kalimanovska Medicinska biohemija, 2003, Beograd
- ^ Freidovich I. Fundamental aspects of reactive oxygen species, or what’s the matter with oxygen? NY Acad Sci 1999;893:13
- ^ Yun-Zhong F, Sheng Y, Guoyao W. Free radicals,antioxidants, and nutrition. Nutrition 2002;18:872–9.
- ^ Forman H, Maiorino M, ursini F. Signaling Functionsof Reactive Oxygen Species. Biochemistry 2010;49(5):835–42.
- ^ Demidov, Vadim V. (2020). „Site-specifically deuterated essential lipids as new drugs against neuronal, retinal and vascular degeneration”. Drug Discovery Today. 25 (8): 1469—1476. ISSN 1359-6446. doi:10.1016/j.drudis.2020.03.014.
Спољашње везе[uredi | uredi izvor]
- Bibliography -- Free radicals and human disease, Handbook of Free Radicals and Antioxidants, vol 1 (1989)
- Free Radicals and Human Disease, Handbook of Free Radicals and Antioxidants, vol 1 (1989), pp. 209-221.
 | Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |
