Оксидо-редукција



Реакције оксидо-редукције (или редокс реакције) су реакције при којима се врши промена оксидационог броја (стања) атома елемената који улазе у састав реагујућих супстанци. Редокс реакције су електронски процес, односно процес премештања периферних електрона са једних атома (молекула или јона) ка другим атомима (молекулима или јонима), при чему долази до промене њиховог оксидационог броја (стања).[1]
Реакција оксидо-редукције састоји се из: реакције оксидације која представља процес отпуштања електрона са неког атома (молекула или јона) и реакције редукције која представља процес примања електрона од стране неког атома (молекула или јона). За атом који отпушта електроне каже се да се оксидовао - повећао свој оксидациони број (представља донор електрона ), а сам је редукционо средство. Атом (молекул или јон) који прима електроне се редуковао - смањио свој оксидациони број (представља акцептор електрона), а сам је оксидационо средство.[2][3] Иако довољни за многе намене, ови описи нису потпуно тачни. Оксидација и редукција се односе се на промену оксидационог стања, док до преноса електрона можда и неће доћи. Оксидација се прецизније дефинише као повећање оксидационог стања, и редукција као смањење оксидационог стања. У пракси ће пренос електрона увек изазвати промену оксидационог стања, али постоје многе реакције које се класификују као „редокс“ иако нема трансфера електрона (као што су оне са променама ковалентних веза).[4][5][6][7]
Оксидо-редукција може да буде било једноставни редокс процес, као што је оксидација угљеника до угљен-диоксида (CO2), или редукција угљеника водоником до метана (CH4). Она исто тако може да буде комплексан процес, као што је оксидација глукозе (C
6H
12O
6) у људском телу путем серије комплексних процеса електронског трансфера.
Редокс реакције, или оксидационо-редукционе реакције, имају низ сличности са реакцијама киселина и база. Као и кисело-базне реакције, редокс реакције су упарен сет, тако да се реакција оксидације не може одвијати а да се истовремено не одвија реакција редукције. Свака реакција сама по себи се зове „полу-реакција“, јер морају постојати две полу-реакције.
Код електрохемијских реакција уређај на коме долази до оксидо-редукције назива се електрода. Ако су две различите електроде повезане проводником, са отпорником, због разлике њихових потенцијала, кроз њега ће тећи електрична струја и на електродама ће почети спонтана реакција оксидације или редукције. Електрода на којој долази до оксидације назива се анода, а она на којој долази до редукције катода. Струја тече од електроде већег потенцијала према електроди нижег потенцијала, а разлика потенцијала једнака је електромоторној сили добијеног галванског елемента. Уопштено говорећи анода је електрода у коју улази струја а катода електрода из које излази струја.
Оксидујући и редукујући агенси
[уреди | уреди извор]Приликом реакције оксидо-редукције долази до привидног преноса електрона са атома мање електронегативности на атом веће електронегативности.
Оксидациона средства
[уреди | уреди извор]Оксидација је првобитно означавала реакцију сједињавања хемијског елемента са кисеоником при чему настају оксиди. Онда је појам проширен на сваку реакцију сједињавања са кисеоником (рецимо оксидацијом алкохола настаје алдехид а даљом оксидацијом алдехида киселина), што се изражава оксидационим бројем. Најшире схваћена оксидација представља губитак електрона. Рецимо, анодна оксидација је процес у којем се молекул (или јон) оксидује тако што (уместо кисеонику) преда електрон аноди.
Јака оксидациона средства имају изразити афинитет према електрону:
- Пероксиди
- Супероксиди
- киселине (нпр. азотна киселина)
- Озон,
- Гасовити флуор, хлор, бром и јод
Редукциона средства
[уреди | уреди извор]Редукција је супротан процес оксидацији и, најшире схваћена, представља процес примања електрона. На пример у катодној редукцији катјон примањем једног или више електрона редукује се до чистог метала. Јасно је да је питање да ли је неки процес оксидација или редукција ствар становишта (да би се нешто оксидовало нешто треба и да се редукује) па се такве реакције називају оксидо-редукционе и цео процес оксидо-редукција. Дакле, у оксидо-редукцији оксиданс оксидује, али се при томе сам редукује.
У пракси неку реакцију називамо оксидационом (посебно у органској хемији), када се структура главног реактанта и главног продукта разликују само у томе, да је једна мала група или појединачни атом услед те реакције повећао свој оксидациони број, на рачун редукције, обично неорганског, простог једињења које се у овом случају назива оксидационо средство.
На пример:
- 2 CH
3CH
2OH + O
2 → 2 CH
3COOH
(C прелази из -1 у +3, а кисеоник из 0 do -2), дакле, C се оксидовао а О редуковао.
Стандардни редукциони потенцијал
[уреди | уреди извор]Редукциони потенцијал се користи за рачунање стандардног електродног потенцијала (Eo ћелије).
Следећа једначина се најчешће налази у уџбеницима: Eoћелије = Eoред + Eoокс.
где: Eoћелије је стандардни електродни потенцијал (у волтима)
Eoред је стандардни редукциони потенцијал редукујућег агенса.
Eoокс (стандардни оксидациони потенцијал) је негативна вредност стандардног редукционог потенцијала оксидујућег агенса.
Следећа једначина генерално кориснија јер су обично дати само редукциони потенцијали, а не оксидациони потенцијали: Eoћелије = Eoред - Eoокс
или еквивалентно: Eoћелије = Eoкатода - Eoанода
где: Eoћелије је стандардни електродни потенцијал (у волтима).
Eoред (Eoкатода) је стандардни редукциони потенцијал редукујућег агенса.
Eoокс (Eoанода) је стандардни редукциони потенцијал оксидујућег агенса.
- John, Phillips; Victor, Strozak; Cheryl, Wistrom (2000). Chemistry: Concepts and Applications. Glencoe McGraw-Hill. стр. 558. ISBN 978-0028282107.
Примери редокс реакција
[уреди | уреди извор]Добар пример је реакција између водоника и флуора у којој се водоник оксидује, а флуор редукује:
- H
2 + F
2 → 2 HF
Ова реакција се може написати као две полу-реакције:
реакција оксидације:
- H
2 → 2 H+ + 2 e−
и реакција редукције:
- F
2 + 2 e− → 2 F−
Анализирајући сваку полу-реакцију у изолацији често се може појаснити свеукупни хемијски процес. Пошто нема нето промене набоја током редокс реакције, вишак електрона реакције оксидације мора бити једнак утрошку електрона реакције редукције (као што је приказано горе).
Елементи, чак и у молекулском облику, увек имају нулто оксидационо стање. У првој полу-реакцији, водоник се оксидује из оксидационог стања нула до оксидационог стања +1. У другој полу-реакцији, флуор се редукује из оксидационог стања нула до оксидационог стања −1.
Када се реакције саберу електрони се пониште:
H
2→ 2 H+ + 2 e− F
2 + 2 e−→ 2 F−
H
2 + F
2→ 2 H+ + 2 F−
И јони се комбинују да формирају водоник флуорид:
- H
2 + F
2 → 2 H+ + 2 F− → 2 HF
Реакције премештања
[уреди | уреди извор]Редокс се јавља у реакцијама премештања или супституције. Редокс компонента тих типова реакција је промена оксидационог стања (набоја) појединих атома, а не размена атома у једињењима.
На пример, у реакцији између гвожђа и раствора бакар(II) сулфата :
- Fe + CuSO
4 → FeSO
4 + Cu
Јонска једначина ове реакције је:
- Fe + Cu2+ → Fe2+ + Cu
Две полу-једначине, показују да се гвожђе оксидује:
- Fe → Fe2+ + 2 e−
и да се бакар редукује:
- Cu2+ + 2 e− → Cu
Други примери
[уреди | уреди извор]
- Оксидација гвожђа(II) до гвожђа(III) водоник пероксидом у присуству киселине:
- Fe2+ → Fe3+ + e−
- H2O2 + 2 e− → 2 OH−
- Укупна једначина:
- 2 Fe2+ + H2O2 + 2 H+ → 2 Fe3+ + 2 H2O
- Редукција нитрата до азота у присуству киселине (денитрификација):
- 2 NO3− + 10 e− + 12 H+ → N2 + 6 H2O
- Оксидација елементарног гвожђа до гвожђе(III) оксида кисеоником (позната као корозија, што је слично са потамњивањем):
- 4 Fe + 3 O2 → 2 Fe2O3
- Сагоревање угљоводоника, на пример у мотору са унутрашњим сагоревањем, које производи воду, угљен-диоксид, неке парцијално оксидоване форме као што је угљен-моноксид, и топлоту енергију. Комплетна оксидација материјала који садржи угљеник производи угљен-диоксид.
- У органској хемији, постепена оксидација угљоводоника кисеоником производи воду, и сукцесивно, алкохол, алдехид или кетон, карбоксилну киселину, и затим пероксид.
Редокс реакције у индустрији
[уреди | уреди извор]Редуковања руде је примарни металуршки процес у производњи метала.
Оксидација се користи у широком низу индустрија, као што је продукција производа за чишћење и оксидација амонијака у производњи азотне киселине, која се затим користи за прављење вештачких ђубрива.
Редокс реакције су фондација електрохемијских ћелија. Процес галванизације користи редокс реакције за облагање објеката танким слојем метала. Примери таквих процеса су хромирање аутомобилских делова, посребравање прибора за јело, и позлаћивање накита.
Редокс реакције у биологији
[уреди | уреди извор]
|
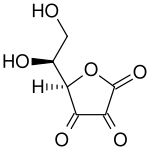
|
Доле: дехидроаскорбинска киселина (оксидована форма витамина Ц)
Многи важни биолошки процеси обухватају редокс реакције. На пример, ћелијска респирација је оксидација глукозе (C6H12O6) до CO2 и редукција кисеоника до воде. Збирна реакција ћелијске респирације је:
- C6H12O6 + 6 O2 → 6 CO2 + 6 H2O
Процес ћелијске респирације је такође у знатној мери зависан од редукције NAD+ до NADH, као и од реверзне реакције (оксидације NADH до NAD+). Фотосинтеза и ћелијска респирација су комплементарне, мада фотосинтеза није реверзна реакција ћелијске респирације:
- 6 CO2 + 6 H2O + светлосна енергија → C6H12O6 + 6 O2
Биолошка енергија се фреквентно складишти и ослобађа путем редокс реакција. Фотосинтеза обухвата редукцију угљен-диоксида у шећере и оксидацију воде у молекулски кисеоник. Супротна реакција, респирација, оксидује шећере и производи угљен-диоксид и воду. У међу корацима, редукована угљенична једињења се користе за редуковање никотинамид аденин динуклеотида (NAD+), који затим доприноси стварању протонског градијента којим се покреће синтеза аденозин-трифосфата (ATP). Он се одржава редукцијом кисеоника. У животињским ћелијама, митохондрија врши сличне функције.
Реакције слободних радикала су редокс реакције које се јављају као део хомеостазае и убијања микроорганизама. Код ових реакција један електрон се одваја од молекула. Слободни радикали могу да постану штетни за људско тело ако се не вежу за редокс молекул или антиоксиданс. Слободни радикали могу да изазову ћелијске мутације и узрокују канцер.
Термин редокс стање се често користи за означавање баланса NAD+/NADH и NADP+/NADPH у биолошким систему као што је ћелија или орган. Редокс стање се огледа у балансу неколико група метаболита (нпр., лактат и пируват, бета-хидроксибутират и ацетоацетат). Абнормално редокс стање се може развити у низ штетних ситуација, као што су хипоксија, шок, и сепса.
Редокс кружење
[уреди | уреди извор]Велики број различитих ароматичних једињења се ензиматски редукује да формира слободне радикале који садрже један електрон више него почетна једињења. У општем случају, донор електрона је било који од широког низа флавоензима и њихових коензима. Након формирања, ти анјонски слободни радикали редукују молекулски кисеоник до супероксида, и регенеришу непромењено почетно једињење. Нето реакција је оксидација флавоензимских коензима и редукција молекулског кисеоника до супероксидне форме. Овој каталитички процес се описује као бескористан циклус или редокс циркулација.
Примери молекула који индукују овој процес су хербицид паракват и други виологени, као и хинони попут менадиона.[8]
Редокс реакције у геологији
[уреди | уреди извор]
У геологији, редокс реакције су важне за формирање минерала, њихову мобилизацију, као и у неким седиментационим срединама. У општем случају, редокс стање већине стена се може видети по њиховој боји. Црвена боја се везује за оксидујуће услове формирања, док се зелена типично везује за редукујуће услове. Беле (побелеле стене) такође могу бити везане за редукујуће услове. Познати пример редокс услова са утицајем на редокс процесе су наслаге уранијума и Навахо пешчар.
Балансирање редокс реакција
[уреди | уреди извор]За описивање електрохемијске реакције редокс процеса неопходно је да се полу-реакције оксидације и редукције балансирају. У општем случају, за реакције у воденом раствору, додају се H+, OH−, H2O, и електрони да би се компензовале оксидационе промене.
Кисела средина
[уреди | уреди извор]У киселој средини, -H- јони и вода се додају полу реакцијама да би се балансилара целокупна реакција.
На пример, кад манган (II) реагује са натријум бизмутатом:
Небалансирана реакција: Mn2+
(aq) + NaBiO
3(s) → Bi3+
(aq) + MnO
4− (aq)Оксидација: 4 H
2O(l) + Mn2+
(aq) → MnO−
4(aq) + 8 H+
(aq) + 5 e−Редукција: 2 e− + 6 H+
+ BiO−
3(s) → Bi3+
(aq) + 3 H
2O(l)
Реакција се балансира скалирањем две полу реакције тако да учествује исти број електрона:
- 8 H
2O(l) + 2 Mn2+
(aq) → 2 MnO−
4(aq) + 16 H+
(aq) + 10 e− - 10 e− + 30 H+
+ 5 BiO−
3(s) → 5 Bi3+
(aq) + 15 H
2O(l)
Додавањем ове две реакције елиминишу се електронски чланови и добија се балансирана реакција:
- 14 H+
(aq) + 2 Mn2+
(aq) + 5 NaBiO
3(s) → 7 H
2O(l) + 2 MnO−
4(aq) + 5 Bi3+
(aq) + 5 Na+
(aq)
Базна средина
[уреди | уреди извор]У базној средини, додају се OH− јони и вода полу реакцијама да би се балансирала реакција.
На пример, у реакцији између калијум перманганата и натријум сулфит:
Небалансирана реакција: KMnO
4 + Na
2SO
3 + H
2O → MnO
2 + Na
2SO
4 + KOHРедукција: 3 e− + 2 H
2O + MnO
4− → MnO
2 + 4 OH−Оксидација: 2 OH− + SO
32− → SO
42− + H
2O + 2 e−
Балансирање броја електрона у две полу реакције даје:
- 6 e− + 4 H
2O + 2 MnO
4− → 2 MnO
2 + 8 OH− - 6 OH− + 3 SO
32− → 3 SO
42− + 3 H
2O + 6 e−
Додавањем те две полу реакције формира се балансирана реакција:
- 2 KMnO
4 + 3 Na
2SO
3 + H
2O → 2 MnO
2 + 3 Na
2SO
4 + 2 KOH
Види још
[уреди | уреди извор]Референце
[уреди | уреди извор]- ^ Schüring 2000, стр. 246.
- ^ Peter Atkins; Julio de Paula (2001). Physical Chemistry (7th изд.). W. H. Freeman. ISBN 0716735393.
- ^ Donald A. McQuarrie; John D. Simon (1997). Physical Chemistry: A Molecular Approach (1st изд.). University Science Books. ISBN 0935702997.
- ^ Robertson 2010, стр. 82
- ^ Phillips, Strozak & Wistrom 2000, стр. 558.
- ^ Rodgers 2012, стр. 330
- ^ Zumdahl & Zumdahl 2009, стр. 160.
- ^ „gutier.doc” (PDF). Приступљено 30. 6. 2008.
Литература
[уреди | уреди извор]- Phillips, John; Strozak, Victor; Wistrom, Cheryl (2000). Chemistry: Concepts and Applications. Glencoe McGraw-Hill. стр. 558. ISBN 978-0028282107. „Students often are confused when associating reduction with the gain of electrons.”
- Robertson, William (2010). More Chemistry Basics. National Science Teachers Association. стр. 82. ISBN 978-1-936137-74-9.
- Rodgers, Glen (2012). Descriptive Inorganic, Coordination, and Solid-State Chemistry. Brooks/Cole, Cengage Learning. стр. 330. ISBN 978-0-8400-6846-0.
- Zumdahl, Steven; Zumdahl, Susan (2009). Chemistry. Houghton Mifflin. стр. 160. ISBN 978-0-547-05405-6.
- Schüring, J. (2000). Redox: Fundamentals, Processes and Applications. Springer. ISBN 978-3-540-66528-1.
