Metaloprotein — разлика између измена
. |
(нема разлике)
|
Верзија на датум 1. новембар 2016. у 02:44
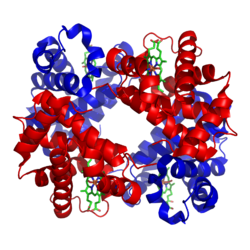
Metaloprotein je generička oznaka za protein koji sadrži metalni jon kao kofaktor.[1][2] Ovoj kategoriji pripada veliki broj proteina.
Funkcija
Procenjuje se da oko polovine svih proteina sadrži metal.[3] Prema jednoj drugoj proceni, za jednu četvrtine do jedne trećine svih proteina je neophodno prisustvo metala za obavljanje njihovih funkcija.[4] Stoga, metaloproteini imaju mnogo različitih funkcija u ćelijama, kao što su skladištenje i transport proteina, enzimi i signalizacijski proteini. Uočena je i uloga metalnih jona u zaraznim bolestima.[5]
Principi hemijske koordinacije
U metaloproteinima, metalni joni su obično koordinisani sa azotnim, kiseoničnim ili sumpornim centrima, koji pripadaju aminokiselinskim ostacima proteina. Ove donorske grupe često daju bočni ostaci lanca aminokiselina. Posebno su značajni supstituenti imidazola u ostacima histidina, tiolata u cisteinskim ostatacima i karboksilna grupa aspartata. S obzirom na raznolikost metaloproteoma, gotovo svi ostaci aminokiselina ispoljavaju afinitet vezivanja sa metanim centrima. Peptidna osnova pruža donorske grupe, gde spadaju deprotonisani amidi i amidni karbonilni centri kiseonika.
Osim grupa donora koje daju ostataci aminokiselina, veliki broj organskih kofaktora funkcionišu kao ligandi. Možda su najpoznatiji tetradentat N4 makrociklični ligandi inkorporirani u protein hema. Takođe su česti i neorganski ligandi kao što su sulfidi i oksidi.[6][7][8][9][10][11][12][13][14]
Skladištenja i transport metaloproteina
Prenosnici kiseonika
Hemoglobin, koji je glavni prenosilac kiseonika kod ljudi, ima četiri podjedinice u kojima je gvožđe(II) jon koordiniran planarnim, makrocikličnim ligandom protoporfirina IX (PIX) i imidazolskog atoma azota iz histidinskih ostataka. Šesto koordinacijako mesto sadrži molekule vode ili kiseonika. Za razliku toga proteina mioglobina, koji se nalazi u mišićnim ćelijama, ima samo jednu takvu jedinicu. Aktivno mesto se nalazi u hidrofobnom džepu. To je važno, jer bez njega gvožđe(II) će biti nepovratno oksidirano u gvožđe(III).Konstanta stabilnosti kompleksa za formiranje HBO2 je takva da se kiseonik više uzima ili otpušta, zavisno od parcijalnog pritiska kiseonika u plućima ili u mišićima. Hemoglobinske četiri podjedinice pokazuju efekt kooperativnosti koji omogućava jednostavno prenošenje kiseonika iz hemoglobina u mioglobin.[15]
Za oba, hemoglobin i mioglobin se ponekad pogrešno navodi da oksidovani oblik sadrži gvožđe(III). Sada je poznato da se dijamagnetna priroda ovih oblika javlja zato što je atom gvožđa(II) u stanju niskog spina. U oksihemoglobinu, atom gvožđa se nalazi u ravni porfirinskog prstena, ali u paramagnetnom deoksihemoglobinu, atom gvožđa je iznad ravni prstena.[15] Ova promena stanja spina je združeni efekt zbog većeg polja kristalnog cepanja i manjeg jonskog radijusa Fe2+ u polovini kiseonika.[16][17][18]
Hemeritrin je još jedan nosač kiseonika koji sadrži gvožđe. Mesto vezanja kiseonika je binuklearni centar gvožđa. Atomi gvožđa koordiniraju protein preko karboksilnih bočnih lanaca glutamata, aspartata i pet histidinskih ostataka. Uzimanje O 2 hemeritrinom je praćeno dvoelektronskom oksicijom redukovanog binuklearnog centar čime se formira vezani peroksid (OOH-). Mehanizam otpuštanja kiseonika je detaljno razrađen.[19][20]
Hemocijanini prenose kiseonik u krvi većine mekušaca i nekih zglavkara (Arthropoda), kao što su rakovi. Oni su drugi pigmenti za vezanje kiseonika, samo ih hemoglobin nadmašije po "biološkoj popularnosti" za izbor prenosnika kiseonika. Uz oksigenaciju dva atoma bakra(I) u aktivnom mestu do bakra(II), molekul kiseonika se prevodi u peroksid, O22–.[21][22]
Hlorokruorin (kao veći nosač ertrokruorin) je hemeprotein vezanja kiseonika u krvnoj plazmi mnogih Annelida (prstenastih glista), posebno određenih morskih poliheta.
Citohromi
Ostali metaloenzimi
Postoje dve vrste ugljen-monoksidne dehidrogenaze: jedan sadrži bakar i molibden, a drugi nikal i gvožđe. Paralele i razlike u katalitičkim strategije su bile u fokusu mnogih napisanih komentara. Neki drugi metaloenzimi dati su u sledećoj tabeli, u skladu sa uključenim metalima.
Vidi još
Reference
- ^ Banci, Lucia, ур. (2013). Metallomics and the Cell. Series editors Sigel, Astrid; Sigel, Helmut; Sigel, Roland K.O. Springer. ISBN 978-94-007-5560-4. electronic-book ISBN 978-94-007-5561-1 ISSN 1559-0836 electronic-ISSN 1868-0402
- ^ Shriver, D.F.; Atkins, P.W. (1999). „Chapter 19, Bioinorganic chemistry”. Inorganic chemistry (3rd. изд.). Oxford University Press. ISBN 0-19-850330-X.
- ^ Thomson, A.J.; Gray, H.B. (1998). „Bio-inorganic chemistry”. Current Opinion in Chemical Biology. 2: 155—158. doi:10.1016/S1367-5931(98)80056-2.
- ^ Waldron KJ, Robinson NJ (јануар 2009). „How do bacterial cells ensure that metalloproteins get the correct metal?”. Nat. Rev. Microbiol. 7 (1): 25—35. PMID 19079350. doi:10.1038/nrmicro2057.
- ^ Carver, Peggy L. (2013). „Chapter 1. Metal Ions and Infectious Diseases. An Overview from the Clinic”. Ур.: Astrid Sigel, Helmut Sigel and Roland K. O. Sigel. Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. 13. Springer. стр. 1—28. doi:10.1007/978-94-007-7500-8_1.
- ^ Bajrović K, Jevrić-Čaušević A., Hadžiselimović R., Ed. (2005): Uvod u genetičko inženjerstvo i biotehnologiju. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-1-8.
- ^ Kapur Pojskić L., Ed. (2014): Uvod u genetičko inženjerstvo i biotehnologiju, 2. izdanje. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 978-9958-9344-8-3.
- ^ Hall J. E., Guyton A. C. (2006): Textbook of medical physiology, 11th edition. Elsevier Saunders, St. Louis, Mo, ISBN 0-7216-0240-1.
- ^ Sofradžija A., Šoljan D., Hadžiselimović R. (2000): Biologija 1, Svjetlost, Sarajevo, ISBN 9958-10-686-8.
- ^ Međedović S., Maslić E., Hadžiselimović R. (2000): Biologija 2. Svjetlost, Sarajevo, ISBN 9958-10-222-6.
- ^ Sofradžija A., Šoljan D., Hadžiselimović R. (2000): Biologija 1, Svjetlost, Sarajevo, ISBN 9958-10-686-8.
- ^ Warrell D. A., Cox T. M., Firth J. D. (2010): The Oxford Textbook of Medicine (5th ed.). Oxford University Press.
- ^ Alberts B. (2002)ː Molecular biology of the cell. Garland Science, New York, ISBN 0-8153-3218-1.
- ^ Međedović S., Maslić E., Hadžiselimović R. (2000): Biologija 2. Svjetlost, Sarajevo, ISBN 9958-10-222-6.
- ^ а б Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (II изд.). Oxford: Butterworth-Heinemann. ISBN 0080379419. Fig.25.7, p 1100 illustrates the structure of deoxyhemoglobin
- ^ Hadžiselimović R., Pojskić N. (2005): Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-3-4.
- ^ Hadžiselimović R. (2005): Bioantropologija – Biodiverzitet recentnog čovjeka. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-2-6.
- ^ Kapur Pojskić L., Ed. (2014): Uvod u genetičko inženjerstvo i biotehnologiju, 2. izdanje. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 978-9958-9344-8-3.
- ^ Stenkamp, R. E. (1994). „Dioxygen and hemerythrin”. Chem. Rev. 94: 715—726. doi:10.1021/cr00027a008.
- ^ Wirstam, M.; Lippard, S. J.; Friesner, R. A. (2003). „Reversioble Dioxygen Binding to Hemerythrin”. J. Am. Chem. Soc. 125 (13): 3980—3987. PMID 12656634. doi:10.1021/ja017692r.
- ^ Karlin, K. D.; Cruse, R. W.; Gultneh, Y.; Farooq, A.; Hayes, J. C.; Zubieta, J. (1987). „Dioxygen–copper reactivity. Reversible binding of O2 and CO to a phenoxo-bridged dicopper(I) complex”. J. Am. Chem. Soc. 109 (9): 2668—2679. doi:10.1021/ja00243a019.
- ^ Kitajima, N.; Fujisawa, K.; Fujimoto, C.; Morooka, Y.; Hashimoto, S.; Kitagawa, T.; Toriumi, K.; Tatsumi, K.; Nakamura, A. (1992). „A new model for dioxygen binding in hemocyanin. Synthesis, characterization, and molecular structure of the μ-η2:η2-peroxo dinuclear copper(II) complexes, [Cu(Hb(3,5-R2pz)3)]2(O2) (R = isopropyl and Ph)”. J. Am. Chem. Soc. 114 (4): 1277—1291. doi:10.1021/ja00030a025.
Spoljašnje veze
- Metalloprotein на US National Library of Medicine Medical Subject Headings (MeSH)
