Угљоводоник
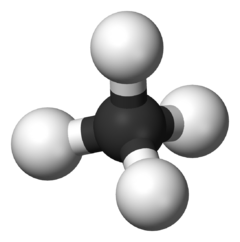
У органској хемији, угљоводоник је органско једињење која садрже само атоме угљеника и водоника.[1]:620 Угљоводоници су примери хидрида 14. групе. Угљоводоници из којих је један атом водоника био уклоњен су угљоводоничне функционалне групе.[2] Угљоводоници се састоје из основног угљениковог скелета (међусобно повезаних атома угљеника) и водоникових атома који су повезани на тај скелет.[3][4][5] Пошто угљеник има 4 електрона у својој најудаљенијој љусци (и зато што свака ковалентна веза захтева донацију једног електрона, по атому, за везу), угљеник има тачно четири везе, и стабилан је само ако се користе све ове 4 везе. Ароматични угљоводоници (арени), алкани, циклоалкани и једињења на бази алкина су различити типови угљоводоника.
Већина угљоводоника који се налазе на Земљи природно се јављају у сировој нафти, где разграђена органска материја пружа обиље угљеника и водоника који, када се вежу, могу да се катенирају тако да формирају наизглед неограничене ланце.[6][7]
Подела угљоводоника[уреди | уреди извор]
Према скелету, угљоводоници се деле на ацикличне (отворен скелет, има главу и реп) и цикличне (затворен скелет, нема ни главе ни репа). Као што је дефинисано у IUPAC номенклатури органских једињења, угљоводоници се деле према врсти везе унутар скелета на засићене, незасићене и ароматичне.
- Засићени угљоводоници су они код којих се између атома угљеника јављају само једноструке хемијске везе (нема двоструких нити троструких веза). Формула за ацикличне засићене угљоводонике (тј., алкане) је CnH2n+2.[1]:623 Најопштија форма засићених угљоводоника је CnH2n+2(1-r), где је r број прстенова. Они са тачно једним прстеном су циклоалкани. Засићени угљоводоници су основа нафтних горива и присутни су у било линеарним или разгранатим облицима. Реакција супституције је њихово карактеристично својство (попут реакције хлоринације којом се формира хлороформ). Угљоводоници са истом молекулском формулом али различитим структурним формулама се називају структурним изомерима.[1]:625 Као што се може видети на примеру 3-метилхексана и његових виших хомолога, разгранати угљоводоници могу да буду хирални.[1]:627 Хирални засићени угљоводоници сачињавају бочне ланце биомолекула као што су хлорофил и токоферол.[8]
- Незасићени угљоводоници су они код којих се између атома угљеника јављају не само једноструке, већ и двоструке и/или троструке хемијске везе. Они са двоструком везом се називају алкени, и имају формулу CnH2n (претпостављајући нецикличке структуре).[1]:628 Они који садрже троструке везе називају се алкини, и имају формулу CnH2n−2.[1]:631
- Ароматични угљоводоници, такође познати као арени, угљоводоници су који имају бар један ароматични прстен.


Према распореду угљеникових атома, угљоводоници могу бити:
- ациклични - имају линијски (разгранати или не) распоред угљеникових атома
- циклични - имају циклични распоред угљеникових атома
Према томе, постоје 4 веће групе угљоводоника:
- засићени, ациклични (парафински угљоводоници): алкани
- засићени, циклични (нафтенски угљоводоници): циклоалкани
- незасићени, ациклични (олефински угљоводоници):
- незасићени, циклични (ароматични угљоводоници): арени

Угљоводоници могу бити гасови (нпр. метан и пропан), течности (нпр. хексан и бензен), воскови или чврсте материје са ниским талиштем (нпр. парафински восак и нафтален) или полимери (нпр. полиетилен, полипропилен и полистирен).
Опште особине[уреди | уреди извор]
Због разлика у молекулској структури, емпиријске формуле угљоводоника се разликују; у линеарним или „равним” алканима, алкенима и алкинима, количина везаног водоника се смањује у алкенима и алкинима услед „самовезавања” или катенације угљеника, што спречава потпуно засићење угљоводоника формирањем двоструких или троструких веза.
Ова својствена способност угљоводоника да се вежу за себе позната је као катенација и омогућава да угљоводоници формирају сложеније молекуле, попут циклохексана, а у ретким случајевима, арене као што је бензен. Ова способност произилази из чињенице да је карактер везе између атома угљеника потпуно неполарaн, јер је расподела електрона равномерно између два елемента истих електронегативности (~0,30), а не долази до формирања електрофила.
Генерално, са катенацијом долази до губитка укупне количине везаних угљоводоника и повећања количине енергије потребне за цепање везе због напрезања молекула; у молекулима као што је циклохексан, ово се назива напрезање прстена, а јавља се због „дестабилизоване” просторне електронске конфигурације атома.
У једноставној хемији, према теорији валентне везе, атом угљеника мора да следи правило 4-водоника, који наводи да је максимални број атома расположивих за везу са угљеником једнак броју електрона који су привучени у спољну љуску угљеника. У погледу електронских шкољки, угљеник се састоји од непотпуне спољне љуске, која садржи 4 електрона и тако има на располагању 4 електрона за ковалентно или координационо везивање.
Угљоводоници су хидрофобни попут липида.
Поједини угљоводоници су изобилни у Сунчевим систему. Језера течног метана и етана пронађена су на Титану, највећем месецу Сатурна, што је потврдила мисија Касини—Хајгенс.[9] Угљоводоници су такође изобилно заступљени у маглинама у виду полицикличних ароматичних угљоводоника (PAH).[10]
Једноставни угљоводоници и њихове варијације[уреди | уреди извор]
| Број атома угљеника |
Алкан (једнострука веза) | Алкен (двострука веза) | Алкин (трострука веза) | Циклоалкан | Алкадиен |
|---|---|---|---|---|---|
| 1 | Метан | — | — | — | — |
| 2 | Етан | Етен (етилен) | Етин (ацетилен) | — | — |
| 3 | Пропан | Пропен (пропилен) | Пропин (метилацетилен) | Циклопропан | Пропадиен (ален) |
| 4 | Бутан | Бутен (бутилен) | Бутин | Циклобутан | Бутадиен |
| 5 | Пентан | Пентен | Пентин | Циклопентан | Пентадиен (пиперилен) |
| 6 | Хексан | Хексен | Хексин | Циклохексан | Хексадиен |
| 7 | Хептан | Хептен | Хептин | Циклохептан | Хептадиен |
| 8 | Октан | Октен | Октин | Циклооктан | Октадиен |
| 9 | Нонан | Нонен | Нонин | Циклононан | Нонадиен |
| 10 | Декан | Децен | Децин | Циклодекан | Декадиен |
| 11 | Ундекан | Ундекен | Ундецин | Циклоундекан | Ундекадиен |
| 12 | Додекан | Додекен | Додецин | Циклододекан | Додекадиен |
Употреба[уреди | уреди извор]


Угљоводоници су примарни извор енергије садашње цивилизације. Доминантна употреба угљоводоника је као извор горива за сагоревање. У чврстом облику угљоводоници попримају облик асфалта (битумена). Смеше испарљивих угљоводоника се преферентно користе уместо хлорофлуороугљеоника као погонско средство за аеросолно распршивање, због утицаја хлорофлуороугљоводоника на озонски омотач.
Метан (CH4) и етан (C2H6) су гасови на собној температури и не могу се лако утечнити самим притиском. Пропан (C3H8) се међутим може лако утечнити, и постоји у 'пропанским боцама' углавном као течност. Бутан (C4H10) се тако лако утечњава да то пружа безбедно, испарљиво гориво за мале џепне упаљаче. Пентан (C5H12) је безбојна течност на собној температури, која се често у користи у хемијским лабораторијама и индустрији као моћан скоро безмирисан растварач воскова и органских молекула велике молекулске тежине, укључујући мазива. Хексан (C6H14) је такође у широкој употреби као неполарни, неароматични растварач, као и значајна фракција обичног бензина. C6 до C10 алкани, алкени и изомерни циклоалкани су главне компоненте бензина, нафте, млазног горива и специјализованих индустријских растварачких мешавина. Са прогресивним додавањем угљеничних јединица, једноставни угљоводоници непрстенасте структуре имају веће вискозности, индексе подмазивања, тачке кључања, температуре очвршћавања и дубљу боју. На супротном крају од метана леже тешки катрани који остају као најнижа фракција у реторти за рафинацију сирове нафте. Они се прикупљају и широко користе као кровна једињења, за превлачење тротоара, као средства за заштиту дрвета (серија креозота) и као изузетно вискозне течности отпорне на смицање.
Употреба угљоводоника је такође распрострањена у природи. Неки еусоцијални зглавкари, попут бразилске безжаочне пчеле, Schwarziana quadripunctata, користе јединствене „мирисе” угљоводоника како би распознали сроднике од несродника. Хемијски састав угљоводоника варира у зависности од старости, пола, места гнезда и хијерархијског положаја.[11]
Тровање[уреди | уреди извор]
Тровање угљоводоником, попут бензена и дизела, обично се јавља случајно удисањем или гутањем ових цитотоксичних хемијских једињења. Интравенска или субкутана инјекција нафтних једињења са намером самоубиства или злоупотребе је ванредан догађај који може резултирати локалним оштећењем или системском токсичношћу попут некрозе ткива, стварања апсцеса, затајењем респираторног система и делимичним оштећењем бубрега, мозга и нервног система. У једном извештавају је описан случају некрозе зида грудног коша и емпиема који су последица покушаја самоубиства убризгавањем петролеја у плеуралну шупљину.[12]
Налажење и добијање угљоводоника[уреди | уреди извор]
Угљоводоници су основни састојци нафте, и земног гаса из којих се најчешће добијају.
Хемијска својства[уреди | уреди извор]
У реакцији сагоревања угљоводоника као производ увек се добија угљен-диоксид (CO2) и вода (H2O). При реакцији се ослобађа велика количина топлоте. Уколико се у реакцији не нађе довољна количина кисеоника као производ настаје још и чађ и угљен-моноксид (CO).
Супституција или замена је врста хемијске реакције карактеристична за алкане. Алкани реагују са халогеним елементима при великој количини светлости и тај процес се назива супституција. Добар пример је реакција са хлором (Cl).
- CH4 + Cl2 → CH3Cl + HCl
- CH3Cl+ Cl2 → CH2Cl2 + HCl
- CH2Cl2 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CCl4 + HCl
Када се на крају реакције нађе вода и угљен-диоксид онда је таква реакција потпуна, а ако се добије било које друго једињење онда је реакција непотпуна.
Адиција и полимеризација су врсте хемијских реакција које се јављају код незасићених ацикличних угљоводоника: алкена и алкина. Адиција'' или додавање је процес раскидања двоструке или троструке везе у алкенима и алкинима. Пример је додавање водоника на етен.
- CH2=CH2 + H2 → CH3-CH3
У наведеном примеру по један атом водоника одлази у оба једињења и раскида двоструку везу. У суштини адиција је процес преласка алкена и алкина у алкане додавањем атома неких других елемената.
Полимеризација или удруживање је процес удруживања мањих једињења у веће. Сама основна једињења се зову мономери, а удружени се називају једним именом полимери.
Референце[уреди | уреди извор]
- ^ а б в г д ђ Silberberg, Martin (2004). Chemistry: The Molecular Nature Of Matter and Change. New York: McGraw-Hill Companies. ISBN 978-0-07-310169-9.
- ^ IUPAC Goldbook hydrocarbyl groups Архивирано 2010-01-07 на сајту Wayback Machine
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ McMurry John E. (1992). Fundamentals of Organic Chemistry (3rd изд.). Belmont: Wadsworth. ISBN 0-534-16218-5.
- ^ Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th изд.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
- ^ Clayden, J., Greeves, N. (2001). Organic Chemistry Oxford. стр. 21. ISBN 978-0-19-850346-0.
- ^ McMurry, J. (2000). Organic Chemistry 5th ed. Brooks/Cole: Thomson Learning. ISBN 978-0-495-11837-4. стр. 75-81.
- ^ Meierhenrich, Uwe (2008). Amino Acids and the Asymmetry of Life: Caught in the Act of Formation. Springer. ISBN 978-3-540-76885-2.
- ^ NASA's Cassini Spacecraft Reveals Clues About Saturn Moon Архивирано 2014-09-02 на сајту Wayback Machine. NASA (12 December 2013)
- ^ Guzman-Ramirez, L.; Lagadec, E.; Jones, D.; Zijlstra, A. A.; Gesicki, K. (2014). „PAH formation in O-rich planetary nebulae”. Monthly Notices of the Royal Astronomical Society. 441 (1): 364—377. Bibcode:2014MNRAS.441..364G. arXiv:1403.1856
 . doi:10.1093/mnras/stu454.
. doi:10.1093/mnras/stu454.
- ^ Nunes, T.M.; Turatti, I.C.C.; Mateus, S.; Nascimento, F.S.; Lopes, N.P.; Zucchi, R. (2009). „Cuticular Hydrocarbons in the Stingless Bee Schwarziana quadripunctata (Hymenoptera, Apidae, Meliponini): Differences between Colonies, Castes and Age” (PDF). Genetics and Molecular Research. 8 (2): 589—595. PMID 19551647. S2CID 24411681. doi:10.4238/vol8-2kerr012. Архивирано (PDF) из оригинала 26. 9. 2015. г.
- ^ Eskandarlou, M; Moaddab, AH (август 2010). „Chest wall necrosis and empyema resulting from attempting suicide by injection of petroleum into the pleural cavity”. Emerg Med J. 27 (8): 616—8. PMID 20558490. S2CID 206938595. doi:10.1136/emj.2009.073486.
Спољашње везе[уреди | уреди извор]
- Са епруветицом кроз чаробни свет хемије Архивирано на сајту Wayback Machine (9. март 2014)
- Hydrocarbon на сајту Енциклопедија Британика
- The Methane Molecule
