Biomolekul — разлика између измена
м →top: претварање ISBN веза у шаблон |
. |
||
| Ред 1: | Ред 1: | ||
{{short description|Molekul koji je proizveo živi organizam}} |
|||
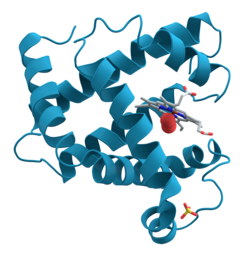
[[Датотека:Myoglobin.png|мини|мини|250px|Prikaz 3D strukture [[mioglobin]]а koja prikazuje obojane [[alfa heliks]]e. Ovo je prvi protein čiju su strukturu uz pomoć [[Rendgenska kristalografija|rendgendske kristalografije]] otkrili Maks Perutz i Džon Kendru [[1958]]. godine, i za to dostignuće dobili [[Nobelova nagrada za hemiju|Nobelovu nagradu za hemiju]].]] |
[[Датотека:Myoglobin.png|мини|мини|250px|Prikaz 3D strukture [[mioglobin]]а koja prikazuje obojane [[alfa heliks]]e. Ovo je prvi protein čiju su strukturu uz pomoć [[Rendgenska kristalografija|rendgendske kristalografije]] otkrili Maks Perutz i Džon Kendru [[1958]]. godine, i za to dostignuće dobili [[Nobelova nagrada za hemiju|Nobelovu nagradu za hemiju]].]] |
||
{{Biochemistry sidebar-lat}} |
{{Biochemistry sidebar-lat}} |
||
| ⚫ | |||
'''Biomolekul''' ili ''biološki molekul'' je svaki [[organska hemija|organski]] [[molekul]] koju proizvodi živi [[organizam]], that are essential to one or more typically [[biological process]]es, such as [[cell division]], [[morphogenesis]], or [[developmental biology|development]].<ref>Bunge, M. (1979). ''Treatise on Basic Philosophy'', vol. 4. Ontology II: A World of Systems, p. 61-2. [https://books.google.com/books?id=4hpNzUzH1E4C&lpg=PP1&hl=pt-BR&pg=PA61 link].</ref> Biomolekuli obuhvataju velike [[polimer]]ske molekule, kao što su [[protein]]i, [[polisaharidi]] i [[nukleinske kiseline]], kao i [[mali molekul|male molekuli]] poput primarnih [[metabolit]]a, [[sekundarni metabolit|sekundarnih metabolita]] i [[prirodni proizvod|prirodnih proizvoda]].<ref name=OBT6th>{{cite book |author1=Slabaugh, Michael R. |author2=Seager, Spencer L. |lastauthoramp=yes |title=Organic and Biochemistry for Today |publisher=Brooks Cole |location=Pacific Grove |year=2007 |id={{ISBN|978-0-495-11280-8}} |edition=6th}}</ref><ref>{{VoetBiochemistry3rd}}</ref> A more general name for this class of material is biological materials. Biomolecules are an important element of living organisms, those biomolecules are often [[endogeny (biology)|endogenous]],<ref>{{cite book |author1=Voon, C. H. |author2=Sam, S. T. |title=Nanobiosensors for Biomolecular Targeting |date=2019 |publisher=Elsevier |isbn=978-0-12-813900-4 |language=en |chapter=2.1 Biosensors}}</ref> produced within the organism<ref>[https://medical-dictionary.thefreedictionary.com/endogeny endogeny]. (2011) ''Segen's Medical Dictionary''. [http://www.thefreedictionary.com The Free Dictionary by Farlex.] Farlex, Inc. Accessed June 27, 2019.</ref> but organisms usually need [[exogeny|exogenous]] biomolecules, for example certain [[nutrient]]s, to survive. |
|||
[[Biology]] and its subfields of [[biochemistry]] and [[molecular biology]] study biomolecules and their [[organic reaction|reactions]]. Most biomolecules are [[organic compound]]s, and just four [[chemical element|elements]]—[[oxygen]], [[carbon]], [[hydrogen]], and [[nitrogen]]—make up 96% of the [[human body]]'s mass. But many other elements, such as the various [[biometal (biology)|biometals]], are present in small amounts. |
|||
'''Biomolekul''' je svaki [[organska hemija|organski]] [[molekul]] koju proizvodi živi [[organizam]], uključujući velike [[polimer]]ske molekule, kao što su [[protein]]i, [[polisaharidi]] i [[nukleinske kiseline]], kao i [[mali molekul|male molekuli]] poput primarnih [[metabolit]]a, [[sekundarni metabolit|sekundarnih metabolita]] i [[prirodni proizvod|prirodnih proizvoda]].<ref name=OBT6th>{{cite book |author1=Slabaugh, Michael R. |author2=Seager, Spencer L. |lastauthoramp=yes |title=Organic and Biochemistry for Today |publisher=Brooks Cole |location=Pacific Grove |year=2007 |id={{ISBN|978-0-495-11280-8}} |edition=6th}}</ref><ref>{{VoetBiochemistry3rd}}</ref> |
|||
The uniformity of both specific types of molecules (the biomolecules) and of certain [[metabolic pathway]]s are invariant features among the wide diversity of life forms; thus these biomolecules and metabolic pathways are referred to as "biochemical universals"<ref>{{cite book |last1=Green |first1=D. E. |last2=Goldberger |first2=R. |title=Molecular Insights into the Living Process |publisher=Academic Press |location=New York |year=1967 |url=https://books.google.com/books?id=xi6FAAAAIAAJ |via=[[Google Books]] }}</ref> or "theory of material unity of the living beings", a unifying concept in biology, along with [[cell theory]] and [[evolution theory]].<ref>{{cite book |last=Gayon |first=J. |chapter=La philosophie et la biologie |title=Encyclopédie philosophique universelle |volume=vol. IV, Le Discours philosophique |editor-first=J. F. |editor-last=Mattéi |publisher=Presses Universitaires de France |year=1998 |pages=2152–2171 |isbn=9782130448631 |url=https://books.google.com/books?id=CWcKAQAAMAAJ |via=Google Books }}</ref> |
|||
== Sastav biomolekula == |
== Sastav biomolekula == |
||
| Ред 11: | Ред 16: | ||
Pored ove dve grupe bioelemenata, postoji i grupa esencijalnih elemenata, koji su ništa manje važni iako se nalaze u tragovima (minimalnim količinama). Ima ih 16: [[gvožđe]], [[bakar]], [[cink]], [[mangan]], [[kobalt]], [[hrom]], [[selen]], [[molibden]], [[jod]], [[fluor]], [[bor]], [[arsen]], [[nikl]], [[kalaj]], [[vanadijum]] i [[silicijum]]. |
Pored ove dve grupe bioelemenata, postoji i grupa esencijalnih elemenata, koji su ništa manje važni iako se nalaze u tragovima (minimalnim količinama). Ima ih 16: [[gvožđe]], [[bakar]], [[cink]], [[mangan]], [[kobalt]], [[hrom]], [[selen]], [[molibden]], [[jod]], [[fluor]], [[bor]], [[arsen]], [[nikl]], [[kalaj]], [[vanadijum]] i [[silicijum]]. |
||
== Struktura i funkcija== |
|||
Tipične biomolekule, kao što su proteini, nukleinske kiseline, masti i [[šećer|karbohidarti]], su građene od specifičnih gradivnih dijelova. Funkcija svake biomolekule je posebna, ali ista u svim organizmima. Gradivni dijelovi mogu biti promijenjeni u različitim biomolekulama, kako bi doprinijeli njihovoj osnovnoj funkciji. |
|||
Na primjer, gradivni dijelovi proteina su [[aminokiselina|aminokiseline]], nukleinskih kiselina - [[nukleotid]]i, [[masti]] - [[glicerol]] i [[masna kiselina|više masne kiseline]], a [[šećer]]a - α-D-[[glukoza]].<ref>https://tkojetko.irb.hr/documents/6547_441.pdf/ {{Webarchive|url=https://web.archive.org/web/20170329051521/https://tkojetko.irb.hr/documents/6547_441.pdf |date=29 Mart 2017 }}; Miloš M. (2009): Osnove biokemije (Skripta za internu upotrebu), Split.</ref> |
|||
====Proteini (bjelančevine) ==== |
|||
'''Proteini''' su velike molekule složenog sastava koji čine osnovu strukture i organizacije živih sistema. To su polimeri dugih lanaca, izgrađeni od monomera aminokiselina, koji su povezani peptidnim vezama. Svaki protein sadrži kombinaciju 20 vrsta aminokiselina (koje nazivamo α- aminokiseline), već unaprijed određenu [[Genetički kod|genetičkim kodom]]. Različite kombinacije aminokiselina omogućavaju proteinima da budu najraznovrsnije i najrasprostranjenije biomolekule u organizmu. |
|||
''Aminokiseline'' su osnovni gradivni dijelovi proteina. Po hemijskom sastavu imaju jednu amino skupinu, karboksilnu skupinu, vodikov atom i različitu R skupinu koja je vezana za α- ugljikov atom i funkcionalnu grupu (reaktivno dio molekule). |
|||
Struktura proteina je podijeljena na više nivoa: |
|||
# '''Primarna struktura''': Različita kombinacija 20 α-aminokiselina utječe na stvaranje velikih lanaca proteina. Primarna struktura određuje funkciju i biološke osobine proteina. |
|||
# '''Sekundarna struktura''': Javlja se u polipeptidnim lancima kada se –CO i amino grupa spajaju vodikovom vezom. Tu postoje dvije strukture: α- zavojnica i β- nabrana ploča, koje su međusobno povezane vodikovom vezom. |
|||
# '''Tercijarna struktura''': To je 3D struktura proteina koja se javlja sklapanjem α i β strukture. Na osnovu ove strukture, proteini se dijele na ''fibrilarne'' i ''globularne''. |
|||
# '''Kvartarna struktura''': Kombinacijom jednostavnih proteina i različitih ili istih polipeptidnih lanaca, se stvaraju kompleksniji proteini. |
|||
Jedna od bitnih karakteristika proteina je ''[[denaturacija]]'', do koje dolazi raskidanjem vodikovih veza. Vodikove veze su jako slabe i osjetljive i lahko pucaju pri najmanjoj promjeni temperature ili [[Ph vrijednost|pH vrijednosti]] okoline. |
|||
Proteini se uglavnom vezuju u složenije molekule sa lipidima, ugljikohidratima, nukleinskim kiselinama i hem grupom. Imaju različite '''funkcije''' u organizmu: 75% [[Ćelijska masa|ćelijske mase]] je izgrađeno od proteina, a imaju veliku ulogu i kao gradivne jedinice [[Ćelijska plazma|ćelijske plazme]] i [[organela]]. Također djeluju kao biohemijski katalizatori- [[enzimi]]. Neki od najpoznatijih [[hormon]]a su proteini ([[inzulin]], [[glukagon]]). Učestvuju u rastu i obnavljanju [[tkiva]]. |
|||
=== Lipidi (masti) === |
|||
'''Lipidi''' su velika skupina masti i [[ulja]] karakteristični po netopivosti u vodi i topivosti u organskim rastvaračima (kao što su [[aceton]], [[eter]], [[karbon tetrahlorid]]). Kao i ugljikohidrati, lipidi su uglavnom sastavljeni od C, H i O atoma, a složeni mogu imati i N, P i S atome.. Nastaju u reakciji masnih kiselina sa alkoholima ili aminima. |
|||
Gradivni dijelovi lipida su ''više masne kiseline'', koje su uglavnom monokarboksilne organske kiseline sa brojem C atoma većim od četiri. Više masne kiseline mogu biti: ''zasićene'' (nerazgranate i najraširenije u prirodi) i ''nezasićene'' (sa jednom ili više dvostrukih veza). |
|||
Na osnovu njihove molekularne strukture, lipidi su podijeljeni u tri skupine: |
|||
# '''Jednostavni lipidi''': U jednostavne lipide se ubrajaju ''esteri'', koji se mogu podijeliti u dvije skupine. Po strukturi, masti i ulja su trigliceridi, koji su esteri glicerola i masnih kiselina. Njihove karakteristike zavise od vrste i količine masnih kiselina. Dugi lanci masnih kiselina mogu imati različit broj C atoma (između 12 i 24) i dvostruke veze ukoliko su nezasićeni. '''Masti''' su trigliceridi koji su na sobnoj temperaturi u čvrstom stanju, a '''ulja''' u tečnom. Dvostruka veza nezasićenih masnih kiselina lahko podliježe hidrogenizaciji, što utječe na stvaranje zasićenih triglicerida ili masti. Netopivi su u vodi. '''Voskovi''' su esteri masnih kiselina sa dugim lancima monohidroksidnih [[alkohol]]a sa 26-34 C atoma. Rašireni su u prirodi u raznim spojevima. Često su dijelom zaštitnih slojeva na površinama životinja i biljaka, a neki [[insekti]] i luče vosak (kao [[pčele]]). Trigliceridi podliježu procesu ''[[saponifikacija|saponifikacije]]'' i imaju veliku primjenu u [[Kozmetička industrija|kozmetičkoj industriji]]. |
|||
# '''Složeni lipidi''': Složeni lipidi su esteri masnih kiselina i alkohola, sa različitim primjesama proteina, fosfornih kiselina, šećera itd. Postoji više skupina ovih lipida, a najpoznatiji su fosfolipidi i glikolipidi. Složeni lipidi u svojoj hemijskoj strukturi imaju polarni i nepolarni dio. Najvažniju funkciju imaju u ''izgradnji bioloških membrana''. |
|||
# '''Dobijeni lipidi''': ''[[Steroidi]]'' su posebna grupa lipida koji se stvaraju u tijelu tokom metabolizma. Ne ubrajaju se u grupu estera. [[Holesterol]] je jedan od najpoznatijih steroida u ljudskom i životinjskom tkivu. |
|||
Osnovna '''funkcija''' lipida je učestvovanje u izgradnji svih ćelijskih membrana, kao i rezerva hranjivih sastojaka (u [[trigliceridi]]ma) za energetske potrebe organizma. |
|||
===Ugljenohidrati=== |
|||
'''Ugljenohidrati''' formiraju veliku skupinu organskih jedinjenja, koji imaju važnu ulogu u svakodnevnom životu. Nastaju u biljkama kao produkt procesa ''[[Fotosinteza|fotosinteze]].'' Najrasprostranjeniji ugljikohidrati su [[glukoza]], [[fruktoza]], [[saharoza]], [[škrob]] i [[celuloza]]. Mnogi ugljikohidrati su slatkastog okusa i zato se nazivaju '''šećerima'''. |
|||
Svi ugljikohidrati imaju zajedničku formulu '''Cx(H2O)y'''. Osnovni gradivni dijelovi njihovih lanaca se nazivaju '''monosaharidi''' (jednostavni šećeri). Lanac je nerazgranat i svaki C atom nosi –OH grupu, a po jedan aldehidnu ili keto skupinu. |
|||
Na osnovu ponašanja pri hidrolizi, ugljikohidrati se mogu podijeliti u tri skupine: |
|||
# '''[[Monosaharidi]]''' su jednostavni ugljikohidrati koji se ne mogu hidrolizom rastaviti na jednostavnije jedinice ketona. Poznato je 20 vrsta monosaharida koji se nalaze u prirodi. Oni su dalje podijeljeni na osnovu broja C atoma i funkcionalne grupe. Ako sadrže aldehidnu grupu, nazivaju se aldozama, a ako sadrže keto grupu- ketozama. Svi imaju bijelu boju i topivi su u vodi. Imaju slatkast okus. |
|||
# '''[[Oligosaharidi]]''' su ugljikohidrati koji sadrže 2- 10 monosaharidnih jedinica dobivenih hidrolizom. Oni se mogu dalje podijeliti na disaharide, trisaharide, tetrasaharide, itd. Monosaharidne jedinice od kojih su sastavljeni kompleksniji ugljikohidrati mogu, ali i ne moraju biti iste u određenom ugljikohidratu. Na primjer, saharoza hidrolizom daje jednu molekulu glukoze i jednu molekulu fruktoze. |
|||
# '''[[Polisaharidi]]''' su dugi lanci monosaharida, koji su najrasprostranjeniji ugljikohidrati u prirodi. Služe kao rezerva hrane kod životinja (glikogen) i biljaka (škrob) i kao gradivni materijal (uglavnom kod biljaka). |
|||
Monosaharidi uglavnom imaju cikličnu strukturu, jer aldehidna i keto skupina nisu potpuno slobodne, što je dokazano ''Haworth-ovim eksperimentom''. |
|||
Ugljikohidrati imaju više '''funkcija''' od kojih su najpoznatije da služi kao gradivni materijal (celuloza) za izgradnju ćelijskih zidova [[bakterija]] i biljaka, te da su povezani sa mnogim lipidima i proteinima i grade spojeve koji imaju važnu funkciju u organizmu (kao glikolipidi i glikoproteini). |
|||
===Nukleinske kiseline === |
|||
'''Nukleinske kiseline''' su biološke molekule, esencijalne za sve oblike živih organizama. To su [[Polimeri|linearni polimeri]], koji se sastoje od različitih nukleotida, poredanih u genetski predodređenom slijedu. |
|||
'''Nukleotidi''' su osnovne gradivne jedinice (monomeri) nukleinskih kiselina i međusobno su povezani preko ''[[Fosfatna grupa|fosfatne grupe]]''. [[Kondenzacija|Kondenzacijom]] hidroksilnih skupina, dolazi do uspostavljanja 3'- 5' fosfodiesterske veze. Svaki nukleotid se sastoji od baze, petougljičnog šećera (pentoze) i fosfatne grupe. |
|||
Na osnovu različite strukture nukleotida, dolazi do stvaranja polimera sa različitom građom i funkcijom, pri čemu razlikujemo dva osnovna tipa: |
|||
# '''[[DNK]]''' - deoksiribonukleinska kiselina- koja sadrži petougljični šećer deoksiribozu. Nosilac je genetičke informacije u jedru i koda za sintezu specifičnih proteina. Sadrži i do 250 miliona nukleotidnih parova. |
|||
# '''[[RNK]]''' - ribonukleinska kiselina- sadrži petougljični šećer ribozu (koja ima jednu više –OH grupu na petougljičnom šećeru). Učestvuje u transkripciji i translaciji genetičke informacije tokom sinteze proteina. Sadrži nekoliko hiljada nukleotida. Postoje tri tipa RNK molekule: ''iRNK'' (informaciona RNK- učestvuje u transkripciji genetičkog koda u jedru), ''rRNK'' (ribosomska RNK- sa ribosomskim proteinima predstavlja gradivne komponente ribosoma) i ''tRNK'' (transportna RNK- prenosi aminokiseline do ribosoma). |
|||
Različita struktura nukleotida je uzrokovana različitim ''bazama'', kojih postoje 4 vrste: [[adenin]], [[guanin]], [[citozin]] i [[timin]] (kod RNK [[uracil]]). |
|||
====Struktura DNK i RNK==== |
|||
Nakon što su Watson i Crick otkrili ''Heliks strukturu DNK''- utvrđeno je da je to dvostruka zavojnica dva polunukleotidna lanca, čije se baze na suprotnim lancima uparaju uvijek kao [[adenin]] (A) sa [[timin]]om (T) i [[guanin]] (G) sa [[citozin]]om (C), koji su međusobno povezani slabim [[vodik]]ovim vezama. |
|||
Osnovna '''funkcija''' DNK je čuvanje informacije o genetičkom materijalu. Pri dijeljenju ćelije, sa osnovne molekule DNK dolazi do prepisivanja genetičkog koda (replikacija DNK), pri čemu se stvaraju novi lanci sa identičnim genetičkim kodom. DNK je smještena u posebno organizovanim strukturama koje se nazivaju ''[[hromosom]]i''. |
|||
== Reference == |
== Reference == |
||
{{reflist| |
{{reflist|}} |
||
== Literatura == |
|||
{{refbegin|30em}} |
|||
* {{Cite book| ref=harv|last=Voet|first=Donald|last2=Voet|first2=Judith G.|title=Biochemistry|edition=3|issue=|chapter=|publisher=Wiley|location=|year=2005|isbn=9780471193500|doi=|url=http://www.chem.upenn.edu/chem/research/faculty.php?browse=V|pages=|access-date=9. 2. 2017|archive-url=https://web.archive.org/web/20070911065858/http://www.chem.upenn.edu/chem/research/faculty.php?browse=V|archive-date=11. 9. 2007|url-status=dead}} |
|||
* {{Cite book| ref=harv|last=McNaught |first = A. D. | name-list-format = vanc | title = Compendium of Chemical Terminology | edition = 2nd |year=1997 | publisher = Blackwell Scientific Publications | location = Oxford |isbn=978-0-9678550-9-7 | url = http://goldbook.iupac.org }} |
|||
* {{Cite book| ref=harv|title=Enzyme nomenclature, 1978 recommendations of the Nomenclature Committee of the International Union of Biochemistry on the nomenclature and classification of enzymes.|year=1979|publisher=Academic Press|location=New York|isbn=9780323144605|pages=}} |
|||
* {{Cite book| ref=harv|last=Clarke|first=Jeremy M. Berg; John L. Tymoczko; Lubert Stryer. Web content by Neil D.|title=Biochemistry|year=2002|publisher=W. H. Freeman|location=New York, NY [u.a.]|isbn=978-0-7167-3051-4|edition=5. ed., 4. print.|url=https://www.ncbi.nlm.nih.gov/books/NBK21154/|chapter=Section 3.5Quaternary Structure: Polypeptide Chains Can Assemble Into Multisubunit Structures|chapter-url=https://www.ncbi.nlm.nih.gov/books/NBK22550/}} |
|||
* {{Cite book| ref=harv|author=Linderstrøm-Lang KU | title = Lane Medical Lectures: Proteins and Enzymes |year=1952 | publisher = Stanford University Press | asin = B0007J31SC|pages=115}} |
|||
* {{Cite book| ref=harv|last=Krauss|first=G.| title = Biochemistry of Signal Transduction and Regulation |year=2003| publisher = Wiley-VCH | location = Weinheim |isbn=9783527605767 | edition = 3rd | chapter = The Regulations of Enzyme Activity | chapterurl = https://books.google.com/books?id=iAvu2XRLnfYC&pg=PA91&dq=enzyme+metabolic+pathways+feedback+regulation&hl=en&redir_esc=y|pages=89–114}} |
|||
* {{Cite book| ref=harv|last=Fersht|first=A.| title = Enzyme Structure and Mechanism | url=https://archive.org/details/enzymestructurem0000fers_k2m7| publisher = W.H. Freeman | location = San Francisco |year=1985 |isbn=978-0-7167-1615-0|pages=[https://archive.org/details/enzymestructurem0000fers_k2m7/page/50 50]–2}} |
|||
* {{Cite book| ref=harv|last=Costanzo|first=Linda S.|title=Physiology |publisher=Lippincott Williams & Wilkins |location=Hagerstwon, MD |year=2007 |isbn=978-0781773119|pages=}} |
|||
* {{Cite book| ref=harv|last=Maton |first = Anthea |last2=Hopkins|first2=Jean|last3=McLaughlin|first3=Charles William|last4=Johnson|first4=Susan|last5=Warner|first5=Maryanna Quon|last6=LaHart|first6=David|last7=Wright|first7=Jill D.| title = Human Biology and Health | publisher = Prentice Hall |year=1993 | location = Englewood Cliffs, New Jersey, US |isbn=978-0139811760|pages=}} |
|||
* {{Cite book| ref=harv|last=Campbell |first = Neil A. |authorlink= |last2=Williamson|first2=Brad|last3=Heyden|first3=Robin J.| title = Biology: Exploring Life | publisher = Pearson Prentice Hall |year=2006 | location = Boston, Massachusetts | url = http://www.phschool.com/el_marketing.html | doi = |id=|isbn=978-0-13-250882-7|pages=}} |
|||
* {{Cite book| ref=harv|title=Becker's World of the Cell |last=Hardin|first=Jeff |last2=Bertoni|first2=Gregory|last3=Kleinsmith|first3=Lewis J.|year=2015|publisher=Pearson |isbn=978013399939-6 |edition=8th |location=New York|pages=422–446}} |
|||
* {{Cite book| ref=harv|vauthors=Evert RF, Eichhorn SE |year=2006 | title = Esau's Plant Anatomy: Meristems, Cells, and Tissues of the Plant Body: Their Structure, Function, and Development|publisher=John Wiley & Sons|isbn=9780471738435|pages=}} |
|||
* {{Cite book| ref=harv|url=https://books.google.com/books?id=31nEAgAAQBAJ&dq|title=Lynn Margulis: The Life and Legacy of a Scientific Rebel |publisher=Chelsea Green|year=2012|isbn=978-1603584470|editor-last=Sagan|editor-first=Dorion|location=White River Junction}} |
|||
* {{Cite book| ref=harv|last=Campbell |first=Neil A. |first2 = Brad |last2=Williamson |first3 = Robin J. |last3=Heyden | name-list-format = vanc |title=Biology: Exploring Life |publisher=Pearson Prentice Hall |year=2006 |location=Boston, Massachusetts|url=http://www.phschool.com/el_marketing.html |isbn=978-0-13-250882-7|pages=}} |
|||
* {{Cite book| ref=harv|url=https://books.google.com/books/about/The_Golgi_Apparatus.html?id=JqIQEFCLVqsC&redir_esc=y|title=The Golgi Apparatus: State of the art 110 years after Camillo Golgi's discovery |vauthors=Pavelk M, Mironov AA|publisher=Springer|year=2008|isbn=978-3-211-76310-0|location=Berlin|pages=580}} |
|||
* {{Cite book| ref=harv|chapter=Ch. 1: Section: Electron Microscopy |chapterurl=https://www.ncbi.nlm.nih.gov/books/NBK9941/#A139 |last=Cooper|first=Geoffrey M.|title=The Cell — A Molecular Approach |publisher=Sinauer Associates |location=Sunderland MA |year=2000 |isbn=978-0-87893-106-4 |edition=2nd |url=https://www.ncbi.nlm.nih.gov/books/NBK9839/ }} |
|||
* {{Cite book| ref=harv|last=Marsh|first=Mark| title = Endocytosis| publisher = Oxford University Press|year=2001|isbn=978-0-19-963851-2|pages=vii}} |
|||
* {{Cite book| ref=harv|last=Schoener|first=Thomas W|chapter=§I.1 Ecological niche |url=https://books.google.com/books?id=4MS-vfT89QMC&pg=PA3 |title=The Princeton Guide to Ecology |editor1-last=Levin|editor1-first=Simon A.|editor2-last=Carpenter|editor2-first=Stephen R.|editor3 =H. Charles J. Godfray |editor4-last=Kinzig|editor4-first=Ann P.|editor5-last=Loreau|editor5-first=Michel|editor6-last=Losos|editor6-first=Jonathan B.|editor7-last=Walker|editor7-first=Brian|editor8-last=Wilcove|editor8-first=David S.|isbn=9781400833023 |publisher=Princeton University Press |year=2009|pages=3}} |
|||
* {{Cite book| ref=harv|title=Biodiversity and ecosystem function|url=https://books.google.com/books?id=j8OmrBY-6JAC&pg=PA88&lpg=PA88&dq=desulfurication&source=bl&ots=Bs_gVLZkxl&sig=96Dwvm4v-evvt-Aq_pBqrAYQ6Jc&hl=en&ei=_lbTS62JB8KB8gbS0LzkDw&sa=X&oi=book_result&ct=result&resnum=3&ved=0CBwQ6AEwAg#v=onepage&q=desulfurication&f=false|year=1993 |first=Ernst-Detlef|last=Schulze |last2=Mooney|first2=Harold A.|publisher=Springer-Verlag|pages=88–90}} |
|||
* {{Cite book| ref=harv|last=Oparin|first=A. I.|editor-last=Bernal|editor-first=John Desmond|title=The origin of life|url=https://books.google.com/books?id=ob6PhrWXZ4gC|year=1967|publisher=World Pub. Co.|pages=199–234}} |
|||
{{refend}} |
|||
== Spoljašnje veze == |
|||
{{Commons category-lat|Biomolecule}} |
|||
* -{[https://web.archive.org/web/20170120182246/http://www.bioexpoonline.com/companies/SBS Society for Biomolecular Sciences] provider of a forum for education and information exchange among professionals within drug discovery and related disciplines.}- |
|||
| ⚫ | |||
{{Biomolekularne strukture-lat}} |
{{Biomolekularne strukture-lat}} |
||
{{Authority control-lat}} |
|||
[[Категорија:Биомолекули|*]] |
[[Категорија:Биомолекули|*]] |
||
Верзија на датум 15. фебруар 2021. у 12:11
| Biohemija |
|---|
 |
| Ključne komponente |
| Istorija i teme |
| Portali: Biologija, Hemija, MCB |
Један корисник управо ради на овом чланку. Молимо остале кориснике да му допусте да заврши са радом. Ако имате коментаре и питања у вези са чланком, користите страницу за разговор.
Хвала на стрпљењу. Када радови буду завршени, овај шаблон ће бити уклоњен. Напомене
|
Biomolekul ili biološki molekul je svaki organski molekul koju proizvodi živi organizam, that are essential to one or more typically biological processes, such as cell division, morphogenesis, or development.[1] Biomolekuli obuhvataju velike polimerske molekule, kao što su proteini, polisaharidi i nukleinske kiseline, kao i male molekuli poput primarnih metabolita, sekundarnih metabolita i prirodnih proizvoda.[2][3] A more general name for this class of material is biological materials. Biomolecules are an important element of living organisms, those biomolecules are often endogenous,[4] produced within the organism[5] but organisms usually need exogenous biomolecules, for example certain nutrients, to survive.
Biology and its subfields of biochemistry and molecular biology study biomolecules and their reactions. Most biomolecules are organic compounds, and just four elements—oxygen, carbon, hydrogen, and nitrogen—make up 96% of the human body's mass. But many other elements, such as the various biometals, are present in small amounts.
The uniformity of both specific types of molecules (the biomolecules) and of certain metabolic pathways are invariant features among the wide diversity of life forms; thus these biomolecules and metabolic pathways are referred to as "biochemical universals"[6] or "theory of material unity of the living beings", a unifying concept in biology, along with cell theory and evolution theory.[7]
Sastav biomolekula
Od svih hemijskih elemenata koji se nalaze u prirodi, samo 27 ulazi u sastav hemijskih jedinjenja koja čine živi svet. Ovi elementi se nazivaju biogenim ili biomolekulskim. Najzastupljeniji bioelementi u građi organskih molekula su: C (ugljenik), H (vodonik), O (kiseonik), N (azot), P (fosfor) i S (sumpor).
Drugu grupu elemenata koja ulazi u sastav živih bića čine: Ca (kalcijum), Mg (magnezijum), Na (natrijum), K (kalijum) i Cl (hlor). Ovi elementi se u telesnim tečnostima nalaze u obliku jona, te se nazivaju elektroliti.
Pored ove dve grupe bioelemenata, postoji i grupa esencijalnih elemenata, koji su ništa manje važni iako se nalaze u tragovima (minimalnim količinama). Ima ih 16: gvožđe, bakar, cink, mangan, kobalt, hrom, selen, molibden, jod, fluor, bor, arsen, nikl, kalaj, vanadijum i silicijum.
Struktura i funkcija
Tipične biomolekule, kao što su proteini, nukleinske kiseline, masti i karbohidarti, su građene od specifičnih gradivnih dijelova. Funkcija svake biomolekule je posebna, ali ista u svim organizmima. Gradivni dijelovi mogu biti promijenjeni u različitim biomolekulama, kako bi doprinijeli njihovoj osnovnoj funkciji.
Na primjer, gradivni dijelovi proteina su aminokiseline, nukleinskih kiselina - nukleotidi, masti - glicerol i više masne kiseline, a šećera - α-D-glukoza.[8]
Proteini (bjelančevine)
Proteini su velike molekule složenog sastava koji čine osnovu strukture i organizacije živih sistema. To su polimeri dugih lanaca, izgrađeni od monomera aminokiselina, koji su povezani peptidnim vezama. Svaki protein sadrži kombinaciju 20 vrsta aminokiselina (koje nazivamo α- aminokiseline), već unaprijed određenu genetičkim kodom. Različite kombinacije aminokiselina omogućavaju proteinima da budu najraznovrsnije i najrasprostranjenije biomolekule u organizmu. Aminokiseline su osnovni gradivni dijelovi proteina. Po hemijskom sastavu imaju jednu amino skupinu, karboksilnu skupinu, vodikov atom i različitu R skupinu koja je vezana za α- ugljikov atom i funkcionalnu grupu (reaktivno dio molekule). Struktura proteina je podijeljena na više nivoa:
- Primarna struktura: Različita kombinacija 20 α-aminokiselina utječe na stvaranje velikih lanaca proteina. Primarna struktura određuje funkciju i biološke osobine proteina.
- Sekundarna struktura: Javlja se u polipeptidnim lancima kada se –CO i amino grupa spajaju vodikovom vezom. Tu postoje dvije strukture: α- zavojnica i β- nabrana ploča, koje su međusobno povezane vodikovom vezom.
- Tercijarna struktura: To je 3D struktura proteina koja se javlja sklapanjem α i β strukture. Na osnovu ove strukture, proteini se dijele na fibrilarne i globularne.
- Kvartarna struktura: Kombinacijom jednostavnih proteina i različitih ili istih polipeptidnih lanaca, se stvaraju kompleksniji proteini.
Jedna od bitnih karakteristika proteina je denaturacija, do koje dolazi raskidanjem vodikovih veza. Vodikove veze su jako slabe i osjetljive i lahko pucaju pri najmanjoj promjeni temperature ili pH vrijednosti okoline. Proteini se uglavnom vezuju u složenije molekule sa lipidima, ugljikohidratima, nukleinskim kiselinama i hem grupom. Imaju različite funkcije u organizmu: 75% ćelijske mase je izgrađeno od proteina, a imaju veliku ulogu i kao gradivne jedinice ćelijske plazme i organela. Također djeluju kao biohemijski katalizatori- enzimi. Neki od najpoznatijih hormona su proteini (inzulin, glukagon). Učestvuju u rastu i obnavljanju tkiva.
Lipidi (masti)
Lipidi su velika skupina masti i ulja karakteristični po netopivosti u vodi i topivosti u organskim rastvaračima (kao što su aceton, eter, karbon tetrahlorid). Kao i ugljikohidrati, lipidi su uglavnom sastavljeni od C, H i O atoma, a složeni mogu imati i N, P i S atome.. Nastaju u reakciji masnih kiselina sa alkoholima ili aminima.
Gradivni dijelovi lipida su više masne kiseline, koje su uglavnom monokarboksilne organske kiseline sa brojem C atoma većim od četiri. Više masne kiseline mogu biti: zasićene (nerazgranate i najraširenije u prirodi) i nezasićene (sa jednom ili više dvostrukih veza).
Na osnovu njihove molekularne strukture, lipidi su podijeljeni u tri skupine:
- Jednostavni lipidi: U jednostavne lipide se ubrajaju esteri, koji se mogu podijeliti u dvije skupine. Po strukturi, masti i ulja su trigliceridi, koji su esteri glicerola i masnih kiselina. Njihove karakteristike zavise od vrste i količine masnih kiselina. Dugi lanci masnih kiselina mogu imati različit broj C atoma (između 12 i 24) i dvostruke veze ukoliko su nezasićeni. Masti su trigliceridi koji su na sobnoj temperaturi u čvrstom stanju, a ulja u tečnom. Dvostruka veza nezasićenih masnih kiselina lahko podliježe hidrogenizaciji, što utječe na stvaranje zasićenih triglicerida ili masti. Netopivi su u vodi. Voskovi su esteri masnih kiselina sa dugim lancima monohidroksidnih alkohola sa 26-34 C atoma. Rašireni su u prirodi u raznim spojevima. Često su dijelom zaštitnih slojeva na površinama životinja i biljaka, a neki insekti i luče vosak (kao pčele). Trigliceridi podliježu procesu saponifikacije i imaju veliku primjenu u kozmetičkoj industriji.
- Složeni lipidi: Složeni lipidi su esteri masnih kiselina i alkohola, sa različitim primjesama proteina, fosfornih kiselina, šećera itd. Postoji više skupina ovih lipida, a najpoznatiji su fosfolipidi i glikolipidi. Složeni lipidi u svojoj hemijskoj strukturi imaju polarni i nepolarni dio. Najvažniju funkciju imaju u izgradnji bioloških membrana.
- Dobijeni lipidi: Steroidi su posebna grupa lipida koji se stvaraju u tijelu tokom metabolizma. Ne ubrajaju se u grupu estera. Holesterol je jedan od najpoznatijih steroida u ljudskom i životinjskom tkivu.
Osnovna funkcija lipida je učestvovanje u izgradnji svih ćelijskih membrana, kao i rezerva hranjivih sastojaka (u trigliceridima) za energetske potrebe organizma.
Ugljenohidrati
Ugljenohidrati formiraju veliku skupinu organskih jedinjenja, koji imaju važnu ulogu u svakodnevnom životu. Nastaju u biljkama kao produkt procesa fotosinteze. Najrasprostranjeniji ugljikohidrati su glukoza, fruktoza, saharoza, škrob i celuloza. Mnogi ugljikohidrati su slatkastog okusa i zato se nazivaju šećerima. Svi ugljikohidrati imaju zajedničku formulu Cx(H2O)y. Osnovni gradivni dijelovi njihovih lanaca se nazivaju monosaharidi (jednostavni šećeri). Lanac je nerazgranat i svaki C atom nosi –OH grupu, a po jedan aldehidnu ili keto skupinu.
Na osnovu ponašanja pri hidrolizi, ugljikohidrati se mogu podijeliti u tri skupine:
- Monosaharidi su jednostavni ugljikohidrati koji se ne mogu hidrolizom rastaviti na jednostavnije jedinice ketona. Poznato je 20 vrsta monosaharida koji se nalaze u prirodi. Oni su dalje podijeljeni na osnovu broja C atoma i funkcionalne grupe. Ako sadrže aldehidnu grupu, nazivaju se aldozama, a ako sadrže keto grupu- ketozama. Svi imaju bijelu boju i topivi su u vodi. Imaju slatkast okus.
- Oligosaharidi su ugljikohidrati koji sadrže 2- 10 monosaharidnih jedinica dobivenih hidrolizom. Oni se mogu dalje podijeliti na disaharide, trisaharide, tetrasaharide, itd. Monosaharidne jedinice od kojih su sastavljeni kompleksniji ugljikohidrati mogu, ali i ne moraju biti iste u određenom ugljikohidratu. Na primjer, saharoza hidrolizom daje jednu molekulu glukoze i jednu molekulu fruktoze.
- Polisaharidi su dugi lanci monosaharida, koji su najrasprostranjeniji ugljikohidrati u prirodi. Služe kao rezerva hrane kod životinja (glikogen) i biljaka (škrob) i kao gradivni materijal (uglavnom kod biljaka).
Monosaharidi uglavnom imaju cikličnu strukturu, jer aldehidna i keto skupina nisu potpuno slobodne, što je dokazano Haworth-ovim eksperimentom.
Ugljikohidrati imaju više funkcija od kojih su najpoznatije da služi kao gradivni materijal (celuloza) za izgradnju ćelijskih zidova bakterija i biljaka, te da su povezani sa mnogim lipidima i proteinima i grade spojeve koji imaju važnu funkciju u organizmu (kao glikolipidi i glikoproteini).
Nukleinske kiseline
Nukleinske kiseline su biološke molekule, esencijalne za sve oblike živih organizama. To su linearni polimeri, koji se sastoje od različitih nukleotida, poredanih u genetski predodređenom slijedu. Nukleotidi su osnovne gradivne jedinice (monomeri) nukleinskih kiselina i međusobno su povezani preko fosfatne grupe. Kondenzacijom hidroksilnih skupina, dolazi do uspostavljanja 3'- 5' fosfodiesterske veze. Svaki nukleotid se sastoji od baze, petougljičnog šećera (pentoze) i fosfatne grupe.
Na osnovu različite strukture nukleotida, dolazi do stvaranja polimera sa različitom građom i funkcijom, pri čemu razlikujemo dva osnovna tipa:
- DNK - deoksiribonukleinska kiselina- koja sadrži petougljični šećer deoksiribozu. Nosilac je genetičke informacije u jedru i koda za sintezu specifičnih proteina. Sadrži i do 250 miliona nukleotidnih parova.
- RNK - ribonukleinska kiselina- sadrži petougljični šećer ribozu (koja ima jednu više –OH grupu na petougljičnom šećeru). Učestvuje u transkripciji i translaciji genetičke informacije tokom sinteze proteina. Sadrži nekoliko hiljada nukleotida. Postoje tri tipa RNK molekule: iRNK (informaciona RNK- učestvuje u transkripciji genetičkog koda u jedru), rRNK (ribosomska RNK- sa ribosomskim proteinima predstavlja gradivne komponente ribosoma) i tRNK (transportna RNK- prenosi aminokiseline do ribosoma).
Različita struktura nukleotida je uzrokovana različitim bazama, kojih postoje 4 vrste: adenin, guanin, citozin i timin (kod RNK uracil).
Struktura DNK i RNK
Nakon što su Watson i Crick otkrili Heliks strukturu DNK- utvrđeno je da je to dvostruka zavojnica dva polunukleotidna lanca, čije se baze na suprotnim lancima uparaju uvijek kao adenin (A) sa timinom (T) i guanin (G) sa citozinom (C), koji su međusobno povezani slabim vodikovim vezama.
Osnovna funkcija DNK je čuvanje informacije o genetičkom materijalu. Pri dijeljenju ćelije, sa osnovne molekule DNK dolazi do prepisivanja genetičkog koda (replikacija DNK), pri čemu se stvaraju novi lanci sa identičnim genetičkim kodom. DNK je smještena u posebno organizovanim strukturama koje se nazivaju hromosomi.
Reference
- ^ Bunge, M. (1979). Treatise on Basic Philosophy, vol. 4. Ontology II: A World of Systems, p. 61-2. link.
- ^ Slabaugh, Michael R. & Seager, Spencer L. (2007). Organic and Biochemistry for Today (6th изд.). Pacific Grove: Brooks Cole. ISBN 978-0-495-11280-8.
- ^ Donald Voet; Judith G. Voet (2005). Biochemistry (3 изд.). Wiley. ISBN 9780471193500.
- ^ Voon, C. H.; Sam, S. T. (2019). „2.1 Biosensors”. Nanobiosensors for Biomolecular Targeting (на језику: енглески). Elsevier. ISBN 978-0-12-813900-4.
- ^ endogeny. (2011) Segen's Medical Dictionary. The Free Dictionary by Farlex. Farlex, Inc. Accessed June 27, 2019.
- ^ Green, D. E.; Goldberger, R. (1967). Molecular Insights into the Living Process. New York: Academic Press — преко Google Books.
- ^ Gayon, J. (1998). „La philosophie et la biologie”. Ур.: Mattéi, J. F. Encyclopédie philosophique universelle. vol. IV, Le Discours philosophique. Presses Universitaires de France. стр. 2152—2171. ISBN 9782130448631 — преко Google Books.
- ^ https://tkojetko.irb.hr/documents/6547_441.pdf/ Архивирано 2017-03-29 на сајту Wayback Machine; Miloš M. (2009): Osnove biokemije (Skripta za internu upotrebu), Split.
Literatura
- Voet, Donald; Voet, Judith G. (2005). Biochemistry (3 изд.). Wiley. ISBN 9780471193500. Архивирано из оригинала 11. 9. 2007. г. Приступљено 9. 2. 2017.
- McNaught AD (1997). Compendium of Chemical Terminology (2nd изд.). Oxford: Blackwell Scientific Publications. ISBN 978-0-9678550-9-7.
- Enzyme nomenclature, 1978 recommendations of the Nomenclature Committee of the International Union of Biochemistry on the nomenclature and classification of enzymes. New York: Academic Press. 1979. ISBN 9780323144605.
- Clarke, Jeremy M. Berg; John L. Tymoczko; Lubert Stryer. Web content by Neil D. (2002). „Section 3.5Quaternary Structure: Polypeptide Chains Can Assemble Into Multisubunit Structures”. Biochemistry (5. ed., 4. print. изд.). New York, NY [u.a.]: W. H. Freeman. ISBN 978-0-7167-3051-4.
- Linderstrøm-Lang KU (1952). Lane Medical Lectures: Proteins and Enzymes. Stanford University Press. стр. 115. ASIN B0007J31SC.
- Krauss, G. (2003). „The Regulations of Enzyme Activity”. Biochemistry of Signal Transduction and Regulation (3rd изд.). Weinheim: Wiley-VCH. стр. 89—114. ISBN 9783527605767.
- Fersht, A. (1985). Enzyme Structure and Mechanism. San Francisco: W.H. Freeman. стр. 50–2. ISBN 978-0-7167-1615-0.
- Costanzo, Linda S. (2007). Physiology. Hagerstwon, MD: Lippincott Williams & Wilkins. ISBN 978-0781773119.
- Maton, Anthea; Hopkins, Jean; McLaughlin, Charles William; Johnson, Susan; Warner, Maryanna Quon; LaHart, David; Wright, Jill D. (1993). Human Biology and Health. Englewood Cliffs, New Jersey, US: Prentice Hall. ISBN 978-0139811760.
- Campbell, Neil A.; Williamson, Brad; Heyden, Robin J. (2006). Biology: Exploring Life. Boston, Massachusetts: Pearson Prentice Hall. ISBN 978-0-13-250882-7.
- Hardin, Jeff; Bertoni, Gregory; Kleinsmith, Lewis J. (2015). Becker's World of the Cell (8th изд.). New York: Pearson. стр. 422—446. ISBN 978013399939-6.
- Evert RF, Eichhorn SE (2006). Esau's Plant Anatomy: Meristems, Cells, and Tissues of the Plant Body: Their Structure, Function, and Development. John Wiley & Sons. ISBN 9780471738435.
- Sagan, Dorion, ур. (2012). Lynn Margulis: The Life and Legacy of a Scientific Rebel. White River Junction: Chelsea Green. ISBN 978-1603584470.
- Campbell NA, Williamson B, Heyden RJ (2006). Biology: Exploring Life. Boston, Massachusetts: Pearson Prentice Hall. ISBN 978-0-13-250882-7.
- Pavelk M, Mironov AA (2008). The Golgi Apparatus: State of the art 110 years after Camillo Golgi's discovery. Berlin: Springer. стр. 580. ISBN 978-3-211-76310-0.
- Cooper, Geoffrey M. (2000). „Ch. 1: Section: Electron Microscopy”. The Cell — A Molecular Approach (2nd изд.). Sunderland MA: Sinauer Associates. ISBN 978-0-87893-106-4.
- Marsh, Mark (2001). Endocytosis. Oxford University Press. стр. vii. ISBN 978-0-19-963851-2.
- Schoener, Thomas W (2009). „§I.1 Ecological niche”. Ур.: Levin, Simon A.; Carpenter, Stephen R.; H. Charles J. Godfray; Kinzig, Ann P.; Loreau, Michel; Losos, Jonathan B.; Walker, Brian; Wilcove, David S. The Princeton Guide to Ecology. Princeton University Press. стр. 3. ISBN 9781400833023.
- Schulze, Ernst-Detlef; Mooney, Harold A. (1993). Biodiversity and ecosystem function. Springer-Verlag. стр. 88—90.
- Oparin, A. I. (1967). Bernal, John Desmond, ур. The origin of life. World Pub. Co. стр. 199—234.
Spoljašnje veze
- Society for Biomolecular Sciences provider of a forum for education and information exchange among professionals within drug discovery and related disciplines.
