Voda


Voda je providna tečnost koja formira reke, jezera, okeane i kišu. Ona je glavni sastojak fluida živih bića. Kao hemijsko jedinjenje, molekul vode sadrži jedan atom kiseonika i dva atoma vodonika, koji su povezani kovalentnim vezama. Voda je tečnost na standardnoj ambijentnoj temperaturi i pritisku, mada se na Zemlji često javlja zajedno sa svojim čvrstim stanjem, ledom; i u gasovitim stanju, pari (vodena para). Ona se takođe javlja u obliku snega, magle, rose i oblaka.[1]
Voda pokriva 71% Zemljine površine.[2] Ona je vitalna za sve poznate forme života. Na zemlji, 96,5% planetarne vode je u morima i okeanima, 1,7% je podzemna voda, 1,7% je u glečerima i ledenim kapama Antarktika i Grenlanda, i mala frakcija je u drugim vodenim telima, i 0,001% u vazduhu kao para, oblaci (formirani od leda i tečne vode suspendovane u vazduhu), i precipitaciji.[3][4] Samo 2,5% Zemaljske vode je slatka voda, i 98,8% te vode je u ledu (izuzev leda u oblacima) i podzemnoj vodi. Manje od 0,3% sve slatke vode je u rekama, jezerima, i atmosferi, i još manja količina Zemljine slatke vode (0,003%) je sadržana u biološkim telima i industrijskim proizvodima.[3]
Voda se na Zemlji konstantno kreće kroz hidrološki ciklus evaporacije i transpiracije (evapotranspiracija), kondenzacije, precipitacije, i oticanja, obično dosežući more. Evaporacija i transpiracija doprinose precipitaciji na zemljištu. Voda koja se koristi u proizvodnji dobara ili usluga je poznata kao virtualna voda.
Bezbedna voda za piće je esencijalna za ljude i druge životne forme, mada ona ne pruža kalorije ili organske nutrijente. Dostup bezbednoj vodi za piće je poboljšan tokom zadnjih dekada u skoro svim delovima sveta, mada približno jedna milijarda ljudi još uvek nema prisutup bezbednoj pitkoj vodi i oko 2,5 milijarde nemaju adekvatnu sanitaciju.[5] Postoji jasna korelacija između dostupa bezbedne vode i bruto domaćeg proizvoda po glavi stanovnika.[6] Međutim, pojedini posmatrači su procenili da će do 2025. više od polovine svetskog stanovništva biti ugroženo nedovoljnim pristupom bezbednoj vodi.[7] Izveštaj iz novembra 2009. sugeriše da će do 2030. u pojedinim regionima sveta koji su u razvoju potražnja za vodom premašiti ponudu za 50%.[8] Voda igra važnu ulogu u svetskoj ekonomiji, pošto ona funkcioniše kao rastvarač za širok spektar hemijskih supstanci i olakšava industrijsko hlađenje i transport. Približno 70% slatke vode koju ljudi koriste se troši na poljoprivredu.[9]
Hemijska svojstva
[uredi | uredi izvor]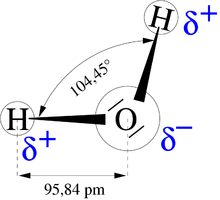





- Polarnost je neravnomjerna razdeoba naboja unutar molekula. Uzrokovana je odeljivanjem naboja usled neravnomerne raspodele elektrona u molekulu. Atom kiseonika na čelu molekula je elektronegativan (teži privlačenju elektrona), pa jedan kraj molekula ima parcijalno negativan naboj, a drugi kraj molekula, oko vodonikovih atoma, ima parcijalno pozitivan naboj. To uzrokuje asimetričnost molekula vode - dva atoma vodonika su pod uglom od 104.5° vezana za atomom kiseonika. Polarnost uveliko određuje ostala svojstva vode.
- Kohezija je svojstvo molekula vode da uspostavlja vodonične veze s bliskim molekulima. Vodonična veza nastaje međusobnim privlačenjem i spontanim usmeravanjem molekula tako da se elektronegativni atom kiseonika jednog pridružuje elektropozitivnim atomima vodonika drugih molekula vode. Vodonične veze među susednim molekulima se neprestano raskidaju i ponovno formiraju (tipična veza ima životni vek od nekoliko mikrosekundi), a svaki molekul vode je u tečnom stanju povezan s oko 3½ susednih molekula, što rezultira stvaranjem velike trodimenzionalne mreže, koja je u čvrstom stanju leda izrazito pravilna. Kohezivnost uslovljava: veliku površinsku napetost vode, kapilarnost, visoku tačku ključanja, specifičnu toplotu i toplotu isparavanja.
- Specifična toplota je količina toplote koju gram neke materije primi da bi mu se temperatura podigla za 1° C (za vodu iznosi 1.0 cal/g). Njen je visok iznos kod vode prouzrokovan širenjem vodoničnih veza. Energija, koja kod drugih tečnosti povećava kretanje među molekulima rastvarača (podiže temperaturu), se kod vode koristi za razbijanje vodoničnih veza među susednim molekulima. Vodeni rastvori su tako, zahvaljujući vodoničnim vezama, izuzeti od velikih promena u temperaturi.
- Toplota isparavanja je količina energije potrebna da se jedan gram tečnosti pretvori u paru. Ova vrednost je visoka kod vode, jer se tokom procesa moraju razložiti vodonične veze. Ovo svojstvo čini vodu izvrsnim rashlađivačem.
Molekul H2O
[uredi | uredi izvor]Voda je tečnost bez mirisa i ukusa koja je prisutna skoro svuda: u okeanima, morima, rekama, jezerima, gasovita u oblacima, zamrznuta u glečerima ili u velikim podzemnim bazenima ispod krečnjačkih stena. Vodu neprestano koristi živi svet koji bez nje ne može da živi. Ljudsko telo čini 72% vode, pri čemu ono stalno unosi i izbacuje nove količine. Voda je presudna za metabolizam u organizmu, pošto omogućuje varenje i kasnije rastvaranje hrane u ćelijama, ali i čišćenje ćelija od otpada. Smatra se da bi svakog dana u telo trebalo uneti oko osam čaša vode, ali to nije naučno potkrepljeno pošto mnogi ljudi piju znatno manje vode. Kako bi zadovoljila svoje ogromne potrebe za vodom, ljudska civilizacija vodu crpi ispod zemlje, iz reka, ili iz mora, a potom je vodovodima dovodi u gradove, do stanova i česmi. Sva voda, hemijski posmatrana sačinjena je od istog molekula H2O. Ovo nam govori da je voda sastavljena od dva atoma vodonika (H) i jednog atoma kiseonika (O). Električne karakteristike i prostorni izgled ovog molekula su zaista specifične, pa određuju mnoge od dobro poznatih svojstava vode.
Agregatna stanja
[uredi | uredi izvor]U zavisnosti od temperature i pritiska, rastojanja između molekula vode su manja ili veća, a veze među njima jače ili slabije pa se voda javlja u više stanja: čvrsto, tečno i gasovito. Prelazak vode iz jednog agregatnog stanja u drugo postiže se povećanjem ili smanjenjem temperature. Voda prelazi u gasovito agregatno stanje zagrejavanjem do temperature od 100 °C. U gasovitom agregatnom stanju molekuli vode su dovoljno međusobno udaljeni da se mogu haotično kretati bez mnogo sudaranja. Prelazak vode iz tečnog u gasovito agregatno stanje se naziva isparavanje. U tečnom agregatnom stanju molekuli vode su više približeni i oni poprimaju oblik suda u kome se nalaze. Čvrsto agregatno stanje se postiže hlađenjem do temperature od 0 °C. U čvrstom agregatnom stanju molekuli vode skoro da se i ne pomeraju i grade čvrstu kristalnu rešetku. Za razliku od tečnog i gasovitog stanja, čvrsto stanje ne mora da poprima oblik suda u kome se nalazi, već je u obliku kristala. Manje je poznato da voda delimično isparava i na nižim temperaturama od 100 °C, ali ne u velikim količinama. Ovo isparavanje omogućuje da voda neprestano kruži u prirodi, iz zemlje ka oblacima, pa potom nazad u vidu kiše i drugih padavina. Sneg je takođe voda, pošto je svaka pahulja kristal leda malih dimenzija. Prelazak vode iz čvrstog u gasovito stanje naziva se sublimacija.
Anomalija vode
[uredi | uredi izvor]Anomalija vode je veoma važna za život svih vodenih stvorenja. To je svojstvo da voda koja je hladnija od 4 °C uvek izlazi na površinu. Led ima manju gustinu od vode u tečnom stanju pa zato pliva po površini. Voda je najgušća na temperaturi od 4 °C, tako da će se u zamrznutim rekama sva voda hladnija od 4 °C popeti ka površini. Anomalija vode omogućava da se reke i jezera nikad ne zamrzavaju do dna, tako da živa bića u rekama prezimljavaju u toploj vodi. Zbog geometrije svog molekula, voda ima niz specifičnih svojstava, kao što je površinski napon - karakteristika da na svojoj površini voda formira opnu, što omogućuje da se voda uvek drži na okupu i između ostalog, postepeno formira vodene kapi. Voda je vrlo retko čista, bez dodataka i primesa. Voda u kojoj ima samo H2O molekula, naziva se destilovana i dobija se u industrijskim pogonima i laboratorijama, procesima hemijske destilacije.
Provodnik
[uredi | uredi izvor]Voda se smatra dobrim provodnikom električne struje. To i nije sasvim tačno, pošto čista voda, H2O, obično ne provodi struju. Struja kroz vodu protiče zahvaljujući rastvorenim mineralima. Voda koja sadrži izuzetno veliki udeo minerala, naziva se mineralna voda. U njoj se nalaze pojedina jedinjenja koja su korisna za organizam. Mehurići koji se nalaze u flaširanim vodama su najčešće industrijski dodatak dodat radi dužeg trajanja i boljeg ukusa (dodat je gas ugljen-dioksid CO2 koji se dodaje u sva gazirana pića). Za razliku od slatkih, u morskoj vodi je rastvorena količina minerala natrijum-hlorida NaCl (kuhinjske soli). Voda je takođe i odličan rastvarač i to joj omogućava višestruku upotrebu. Kada je voda toplija rastvaranje je brže.
Tvrda voda
[uredi | uredi izvor]Voda može biti tvrda i meka. To je zato što se u svakoj vodi nalazi rastvoreno na stotine minerala i drugih jedinjenja. Količine ovih jedinjenja su znatno male, ali su veoma značajne za živi svet. Kada je u vodi sadržaj minerala i jedinjenja visok, za vodu se kaže da je tvrda, a kada je sadržaj nizak za vodu se kaže da je meka.
Značaj
[uredi | uredi izvor]Zbog značaja za opstanak ljudi, voda ima i značajno mesto u kulturi. Većina svetskih religija vodi pridaje simbolični značaj sredstava za pročišćenje kako od materijalnih, tako i od duhovnih prljavština. U Bibliji se voda spominje 442 puta. U politeističkim religijama, kod starih Grka i Rimljana, svaki izvor vode je imao svoga boga zaštitnika. Grčki filozof Empedokle je vodu smatrao za jedan od četiri elementa, uz vazduh, vatru i zemlju, verujući da je čitav svet sačinjen od njih. Voda obično simbolizuje ravnodušnost. Nepravilna eksploatacija i zagađivanje, ugrozilo je svetske zalihe vode. Prema podacima UNESCO-a, u narednih 20 godina rezerve pijaće vode će se smanjiti za 30%. Smatra se da čak 40% svetske populacije već sada nema dovoljno vode za svoje dnevne potrebe. Prema podacima organizacije WaterAid svakih 15 sekundi jedno dete umre od oboljenja izazvanog manjkom vode.
Vrste prirodnih voda
[uredi | uredi izvor]Voda se u prirodi ne pojavljuje u hemijski čistom obliku, jer na svom putu dolazi u dodir, rastvara i prima različite materije. Od količine i vrste ovih sastojaka zavise karakteristike vode. Prema svojoj prirodi, voda se deli na atmosfersku, površinsku i podzemnu.
- Atmosferska voda nastaje od padavina kao što su kiša, sneg i led. Ona sadrži rastvorene gasove sa kojima dolazi u dodir, poput kiseonika i ugljen-dioksida. Od čvrstih materija sadrži nešto prašine i čađi, a u blizini mora i nešto soli.
- Površinska voda je ona koja ili leži na površini tla. Ova voda nastaje od atmosferske vode, koja direktno pada na Zemljinu površinu ili one koja se sliva u nju sa površine tla.
- Podzemna voda se nalazi ispod površinske zemlje. Nastaje prodiranjem padavina od površinskih vodenih tokova ka tzv. vodonepropusnim slojevima (unutar Zemljine površine) koji se sastoje od stena sa malom efektivnom poroznošću. Ova voda spada u red čistijih, pa se zbog takvih odlika veoma često koristi za piće.[10]
Osobine i rasprostranjenost
[uredi | uredi izvor]Voda je najrasprostranjenija tečnost na Zemlji (zapremine ~1500 x 109 km³) i najvažniji (polarni) rastvarač koji rastvara tečnosti, gasove i mnogobrojne čvrste materije. Voda zbog polarnosti poseduje izvrstan kapacitet da rastvara različite vrste materija.
Voda je bitan sastojak živih organizama (maseni udeo vode do 90%) i nužna je za život svih živih organizama. Naučnici tvrde da se živa bića najvećim delom sastoje od vode i da ona čini tri četvrtine (ili više od dve trećine) ukupne površine Zemlje. Na snimcima Zemlje iz Svemira može se uočiti da je velik deo Zemljine površine pokriven vodom, oko 70%.
Pod uticajem Sunčevog zračenja površinska voda neprekidno isparava u atmosferu (tzv. kruženje vode u prirodi), gde se kondenzuje (stvarajući kišne ili snežne oblake u atmosferi) i u obliku padavina (kiša, sneg, grad, rosa, inje i magla) vraća se na Zemlju, prenoseći tako velike mase vode na kontinente. To se naziva globalnim hidrološkim ciklusom, koji umnogome utiče na klimu.
U troposferi voda čini 80% stakleničkih gasova i uzrokuje zadržavanje toplote, te porast globalne temperature.
Najjednostavnija podela vode je podela na slatke (~4% na Zemlji) i slane. Većina je voda na Zemlji slana (mora, okeani). Poznata i podela vode na tečnu (reke) i stajaću (npr. jezera, bare, močvare). Ledenjaci zauzimaju posebno mesto gde je voda u čvrsto obliku.
- Rasprostranjenost vode (zapreminski udeo)
| morska voda | 96,652% |
| polarni led i ledenjaci | 1,702% |
| podzemna voda | 1,631% |
| površinska voda (jezera i reke) | 0,013% |
| voda u tlu | 0,001% |
| voda u atmosferi | 0,001% |
Osim za piće, pripremu hrane i za pranje, voda se uveliko koristi za navodnjavanje poljoprivrednog tla. Voda kao dobar rastvarač opskrbljuje biljke mineralnim materijama i nužna je za fotosintezu, a u ljudskom organizmu kao glavni sastojak telesnih tečnosti opskrbljuje sve organe hranjivim sastojcima i uklanja otpadne materije iz organizma.
Voda je osnovni sastojak svih živih organizama. U nekih organizama čini i 99% njihove mase, a kod čoveka oko 70%. Svi biološki procesi odvijaju se isključivo u vodenoj sredini, iako postoje organizmi koji mogu dugotrajno preživeti stanje potpune dehidratacije. Metabolizam, rast i razmnožavanje takvih organizama počinju tek nakon rehidratacije. Biološki makromolekuli (belančevine, nukleinske kiseline, polisaharidi) sadrže čvrsto vezanu vodu, koja je nužna za njihovu biološki aktivnu konformaciju. Voda nije samo rastvarač u kojem funkcionišu enzimi nego i direktni metabolit; supstrat je u svim hidrolitičkim, a nusprodukt u mnogim biosintetskim reakcijama. Živi organizam neprekidno uzima i otpušta vodu, što se naziva ciklusom vode. Vodeni organizmi izmenjuju vodu difuzijom.
Kod kopnenih biljaka ta se razmena odvija pretežno fizičkim mehanizmima (kapilarne sile u korenu; transpiracija). Kopnene životinje i čovek moraju piti vodu ili je pribaviti hranom koja sadrži vodu. Vodu gube mokraćom, fekalijama, disanjem i znojenjem. Izlučivanje vode metabolički je nužno, jer ono omogućuje organizmu da se oslobodi nekorisnih i štetnih materija koje su rastvorne u vodi. Znojenje je kod mnogih organizama deo procesa termoregulacije.
Ključni je uslov održivoga razvoja je održavanje čistoće vode u prirodnim spremištima i vodotokovima. Sprečavanje zagađivanja voda najvažniji je deo zaštite životne sredine (provodi se aerobna obrada otpada i ispitivanje kakvoće vode).
Dobijanje
[uredi | uredi izvor]Voda se može dobiti direktnom sintezom iz vodonika i kiseonika, a nastaje kao produkt u mnogim drugim hemijskim reakcijama. Može se rastaviti na vodonik i kiseonik elektrolizom, uz dodatak jakoga elektrolita radi povećanja provodljivosti rastvora (čista voda provodi električnu struju, ali je vrlo slab elektrolit), ili termičkom razgradnjom na više od 1000 °C (prevođenjem vodene pare preko užarene platinske žice).
U čistoj vodi postoji ravnoteža autojonizacije vode, tj. autoprotoliza, u kojoj jedan molekul vode deluje kao kiselina, a drugi kao baza:
- H2O + H2O <--> H3O+ + OH-,
Stoga je voda amfoterna.
Voda hemijski reaguje s oksidima metala i daje baze, a s oksidima nemetala formira kiseline. Važna reakcija vode je i hidroliza. Voda se ugrađuje u kristalnu rešetku mnogih soli, dajući hidratizovane soli. Čista voda slabo je jonizovana, pa je molarna koncentracija nastalih jona vrlo mala ([H3O+]=[OH-]=10−7 mol/dm³, pri 25 °C). Čista voda je neutralna, tj. pH = 7.
Zbog polarnog karaktera svog molekula, voda je odličan rastvarač za mnoga jonska i polarna jedinjenja, tako da prirodna voda (voda u prirodi) nikada nije hemijski čista, jer rastvara mineralne materije iz tla i najčešće sadrži kalcijumove, magnezijumove i natrijumove katjone te bikarbonatne, hloridne i sulfatne anjone. Takva se voda naziva tvrdom vodom, jer se prilikom njenog vrenja stvaraju nerastvorni produkti (najčešće kalcijum karbonat, CaCO3) koji slabo prenose toplotu, pa se materijal zagrijane posude pregreva i slabe mu mehanička svojstva.
To je posebno štetno za aparate u domaćinstvu (perilice i bojlere) i parne kotlove visokog pritiska u industriji. Zbog toga se prirodna voda (osim kišnice) za tehničku primenu mora omekšati. Karbonatna (polazna) tvrdoća vode, uzrokovana kalcijumovim i magnezijumovim bikarbonatima, može se ukloniti iskuvavanjem vode ili dodatkom sode, ili smeše sode i kreča, što uzrokuje taloženje netopljivih karbonata.
Voda je homogena smeša upravo zbog rastvorenih materija koje mogu biti hemijska jedinjenja (npr. magnezijum sulfat ili magnezijum hlorid u moru) ili joni metala: katjoni (npr. Ca2+, Mg2+), anjoni (npr. CO32-), potom molekuli (npr. CO2 u mineralnoj vodi) i niz drugih materija koje nažalost u vodu dolaze kao onečišćivači (npr. fosfati).
Polarnost
[uredi | uredi izvor]Molekul vode poseduje dipolni moment, tj. molekul vode je polaran. U hemiji vredi pravilo: “Polarno se rastvara u polarnom“, što će reći da se slično rastvara u sličnome, tj. polarni će se molekuli rastvarati u vodi. Voda je najčešći rastvarač. Rastvorljivost materije u vodi nije ravnomerna, već zavisi od građe materije. Rastvorljivost se menja s promenom pritiska i temperature pri kojoj se rastvaranje odvija. Ako se uzme za primer sam natrijum hlorid koji se u vodi disocira, razlaže se na jone koji su hidratizovani: Na+(aq) i Cl-(aq), taj se proces može opisati jednačinom:
- NaCl(s) --> Na+(aq) + Cl-(aq)
Dejoniziranje vode i tvrdoća
[uredi | uredi izvor]Dejonizovana voda nastaje uklanjanjem rastvorenih soli jonskim izmjenjivačima, a koristi se kao zamena za destilovanu vodu.
Kako se nekarbonatna (stalna) tvrdoća vode, uzrokovana svim ostalim u vodi rastvorenim solima, ne može tako ukloniti. Za uklanjanje ukupne tvrdoće vode (karbonatne i nekarbonatne) sprovodi se dejonizacija vode pomoću izmjenjivača jona.
U Međunarodnom sistemu jedinica (SI) ukupna tvrdoća vode izražava se kao molarna koncentracija zemnoalkalnih jona u vodi (merna jedinica mol/L). Iako ne postoji jednoznačna tablica tvrdoće vode, uglavnom se smatra kako je voda koja sadrži manje od 1,6 mmol/L kalcijumovih jona meka (npr. kišnica), od 1,6 do 3,2 mmol/L umereno tvrda, od 3,2 do 4,6 mmol/L tvrda (npr. vodovodna voda), a uz koncentraciju kalcijumovih jona veću od 4,6 mmol/L vrlo tvrda. Tako prema količini rastvorenih materija, vode se dele na meke i tvrde vode.
Ranije se tvrdoća vode navodila u različitim jedinicama, npr. u nemačkim stupnjevima tvrdoće (°dH), pa je tako 1°dH odgovarao količini jona Ca2+, Mg2+ ili Fe2+ koja je ekvivalentna masenoj koncentraciji kalcijum oksida (CaO) od 10 mg/dm³.
Morska voda
[uredi | uredi izvor]Morskom vodom se naziva voda mora i okeana. Ona sadrži znatne količine rastopljenih soli (više od 35 g/L), a zbog prisutnosti kalcijuma i magnezijuma u obliku hlorida i sulfata, morska je voda vrlo tvrda. Nagriza metale, beton i neke vrste kamena. Izrazito je slanog ukusa, ali se može koristiti za piće nakon desalinizacije slane jezerske ili morske vode (odsoljavanje).
Destilacija vode (destilisana voda)
[uredi | uredi izvor]
Postupak odvajanja rastvorenih materija iz vode naziva se destilacija vode. Hemijski čista voda naziva se redestilisanom vodom.
Destilisana voda (od latinske riči destillare: kapati; latinski aqua destillata; demineralizovana voda, omekšana voda) je destilacijom pročišćena voda (delomično omekšana voda) koja ne sadrži rastvorene čvrste materije, tj. kojoj je uklonjena karbonatna tvrdoća. Destilisana voda još uvek nije hemijski čista voda, ali može da sadrži samo male do neznatnih količina isparljivih nečistoća.
Dobija se jednokratnom ili višekratnom destilacijom, tj. isparavanjem vode i utečnjavanjem (kondenzacijom) vodene pare, čime se voda oslobađa od rastvorenih gasova i rastvorenih ili suspendovanih čvrstih materija (najčešće raznih minerala), a kondenzuje se čista vodena para (H2O). Destilacija konvencionalnim metodama zbog velike potrošnje energije prilično je skup postupak. Korištenjem regenerativne energije kao što je na primer solarna energija troškovi su znatno niži.
Destilisana voda u slobodnoj prodaji je bitno čistija od izvorskih. Destilisana voda nije za piće, zbog svog bljutavog ukusa. Ona se upotrebljava u farmaciji, medicini, hemiji (kao rastvarač, te u tehničke svrhe), industriji (dopunjavanje akumulatorskih baterija, kao sirovina u različitim tehnološkim procesima, kao sredstvo za prenos toplote ili materije), u energetici za pretvaranje kinetičke energije u električnu, kao para u toplotno-energetskim pogonima za zagrevanje i rashlađivanje, itd.
U novije doba destilovana voda se sve više zamenjuje hemijski čistom vodom, dobijenom pročišćavanjem vode pomoću izmjenjivača jona, a takva voda se naziva dejonizovanom vodom.
Destilovana voda je u ravnoteži s ugljen-dioksidom iz vazduha i ima provodljivost od oko 0.8×10−6 S x cm−1. Ponovljenom destilacijom u vakuumu može se postići provodljivost od 0.043×10−6 S x cm−1 pri 18 °C. Ova granična provodljivost uzrokovana je jonizacijom vode.
Isparavanjem takve vode do suvog, u većini slučajeva ona ispari bez ostataka karbonata kao što je slučaj kod mineralne vode.
Pitka voda
[uredi | uredi izvor]Prirodna voda, koja sadrži kalcijum bikarbonat (Ca(HCO3)2) kalcijum hlorid i kalcijum sulfat naziva se tvrda voda.
Pitka voda, podzemna, bunarska i površinska, je bistra i potpuno prozirna voda, bez mirisa i boje, a radi dobrog ukusa treba da sadrži rastvoreni kiseonik, ugljen-dioksid i rastvorne soli (NaCl, NaHCO3) i dr.
Ako voda sadrži patogene bakterije, organske materije, nitrate, nitrite i amonijak, te soli gvožđa (koje omogućuju razvoj algi), manganove soli (daju vodi loš ukus) ili druge štetne materije, voda se mora pre upotrebe pročistiti oksidacijom kiseonikom iz vazduha i dezinfikovati hlorom ili ozonom.
Padavinska voda
[uredi | uredi izvor]Padavinska voda je deo padavina, koje se ispirajući sa površine direktno ili posredno slivaju u vodne sisteme. Zbog sve većeg zagađenja atmosfere i zemljišta dolazi do znatnog zagađenja prirodne vode. Na izgrađenim površinama prikuplja se i ispušta s otpadnim vodama ili odvojeno od njih. Takva voda sadrži prašinu i nešto rastvorenih gasova iz atmosfere, a nema rastvorenih soli, pa je bljutavog ukusa, iako se se ponegde koristi za piće.
Voda u tlu
[uredi | uredi izvor]Voda u tlu je voda koju sadrži tlo, gde je dospela proceđivanjem ili upijanjem. Može biti adehijska, kapilarna ili podzemna voda.
Adehijska voda je voda koja se nalazi u gornjem sloju tla, a zadržava se silama uzajamnog molekularnog delovanja između čestica tla i upijene vode.
Kapilarna voda je voda koja ispunjava najuže pore tla zbog delovanja površinskog napona, a pojavljuje se povećanjem vlažnosti tla.
Podzemne vode su vode koje se nalaze u tlu, tj. u šupljinama tla. Podzemna voda u stenama s međuzrnastom poroznošću naziva se temeljnicom. Podzemna voda je ona voda koja može strujati pod delovanjem gravitacione sile. U vezanim stenama, voda se nakuplja i protiče kroz pukotine. U krškom području znatne količine vode protiču podzemljem.
Arteška voda, podzemna je voda koja se pod određenim pritiskom nalazi u vodopropusnom sloju između vodonepropusnih slojeva.
Otpadna voda
[uredi | uredi izvor]Otpadne vode su vode s rastvorenim i suspendovanim otpadnim materijama iz domaćinstava, industrije i poljoprivrede. Sirove otpadne vode su zagađivači, koji u prirodne vode (reke i mora) dospevaju sistemom kanala ili s padavinskim vodama procesom ispiranja tla (raspršeni ispusti). Zbog složenog sastava otpadnih voda potreban je niz postupaka za pročišćavanje, koji omogućuju ponovnu upotrebu ili neopasno ispuštanje u prirodne vode.
Otpadna voda je voda upotrebljena u domaćinstvu ili industriji i obično je toliko zagađena da se ne sme ispuštati u vodene tokove bez pročišćavanja. Zagađivanje vode industrijskim otpacima stvara u novije doba veliku opasnost za održavanje biološke ravnoteže u rekama, jezerima i morima.
Mineralna voda
[uredi | uredi izvor]Mineralnom vodom naziva se prirodna voda koja u jednoj litri sadrži više od 1g svih rastvorenih soli. Isparavanjem takve vode do suhog, u većini slučajeva ostaju karbonati.
Na svakoj boci prirodne mineralne vode nalaze se podaci o njezinom sastavu, a time i brojnost kalcijumovih i magnezijumovih jona.
Teška voda
[uredi | uredi izvor]Teška voda u hemijskom je smislu deuterijumov oksid (D2O), a u praktičnom smislu naziv za vodu koja je tehničkim postupkom obogaćena deuterijumom (tzv. teškim vodonikom).
Vidi još
[uredi | uredi izvor]Reference
[uredi | uredi izvor]- ^ Mišić, Milan, ur. (2005). Enciklopedija Britanika. V-Đ. Beograd: Narodna knjiga : Politika. str. 68. ISBN 86-331-2112-3.
- ^ „CIA - The world factbook”. Central Intelligence Agency. Arhivirano iz originala 05. 01. 2010. g. Pristupljeno 20. 12. 2008.
- ^ a b Gleick, P.H., ur. (1993). Water in Crisis: A Guide to the World's Freshwater Resources. Oxford University Press. str. 13,Table 2.1 "Water reserves on the earth". Arhivirano iz originala 08. 04. 2013. g. Pristupljeno 09. 03. 2017.
- ^ Water Vapor in the Climate System, Special Report, [AGU], December 1995 (linked 4/2007). Vital Water Arhivirano na sajtu Wayback Machine (7. novembar 2014) UNEP.
- ^ „MDG Report 2008” (PDF). Arhivirano iz originala (PDF) 27. 08. 2010. g. Pristupljeno 25. 7. 2010.
- ^ "Public Services" Arhivirano na sajtu Wayback Machine (7. april 2012), Gapminder video
- ^ Kulshreshtha, S.N (1998). „A Global Outlook for Water Resources to the Year 2025”. Water Resources Management. 12 (3): 167—184. S2CID 152322295. doi:10.1023/A:1007957229865.
- ^ „Charting Our Water Future: Economic frameworks to inform decision-making” (PDF). Arhivirano iz originala (PDF) 5. 7. 2010. g. Pristupljeno 25. 7. 2010.
- ^ Baroni, L.; Cenci, L.; Tettamanti, M.; Berati, M. (2007). „Evaluating the environmental impact of various dietary patterns combined with different food production systems”. European Journal of Clinical Nutrition. 61 (2): 279—286. PMID 17035955. S2CID 16387344. doi:10.1038/sj.ejcn.1602522.
- ^ Voda; Vladimir Stojanović;pp. 5; Gornji Milanovac 2005.
Literatura
[uredi | uredi izvor]- Gleick, P.H., ur. (1993). Water in Crisis: A Guide to the World's Freshwater Resources. Oxford University Press. str. 13,Table 2.1 "Water reserves on the earth". Arhivirano iz originala 08. 04. 2013. g. Pristupljeno 09. 03. 2017.
- Debenedetti, PG., and HE Stanley, . „Supercooled and Glassy Water”. Physics Today. 56 (6).. pp. 40–46 (2003). Downloadable PDF (1.9 MB)
- Franks, F (Ed), Water, A comprehensive treatise, Plenum Press, New York, 1972–1982
- Gleick, PH., (editor), The World's Water: The Biennial Report on Freshwater Resources. Island Press, Washington, D.C. (published every two years, beginning in 1998) The World's Water, Island Press
- Jones, OA., JN Lester and N Voulvoulis, Pharmaceuticals: a threat to drinking water? TRENDS in Biotechnology. 23 (4): 163. Недостаје или је празан параметар
|title=(помоћ), 2005 - -last1= -
- Postel,S., Last Oasis: Facing Water Scarcity. W.W. Norton and Company, New York. 1992
- Reisner,M., Cadillac Desert: The American West and Its Disappearing Water. Penguin Books, New York. 1986.
- United Nations World Water Development Report. Produced every three years. UN World Water Development Report
- Pollem, Ole (2009). Regulierungsbehörden für den Wassersektor in Low-Income Countries. Eine vergleichende Untersuchung der Regulierungsbehörden in Ghana, Sambia, Mosambik und Mali. Hamburg: Verlag Dr. Kovac. ISBN 978-3-8300-4473-4.
- Sibylle Selbmann: Mythos Wasser, Symbolik und Kulturgeschichte, Badenia Verlag Karlsruhe. . 1995. ISBN 978-3-7617-0309-0. Nedostaje ili je prazan parametar
|title=(pomoć) - Bol, Filip (2013). Biografija vode. Smederevo-Beograd: Heliks-Centar za promociju nauke. ISBN 978-86-88767-11-8.-
- Siegfried Dyck, Gerd Peschke: Grundlagen der Hydrologie. 3. izdanje, Verlag für Bauwesen. . Berlin. 1995. ISBN 978-3-345-00586-2.
- Vollrath Hopp: Wasser-Krise? Wasser, Natur, Mensch, Technik und Wirtschaft. Wiley-VCH, Weinheim. . 2004. ISBN 978-3-527-31193-4. Nedostaje ili je prazan parametar
|title=(pomoć) - Ernst Schmidt (ed): Properties of Water and Steam in SI-Units („Thermodynamische Eigenschaften von Wasser und Wasserdampf, 0–800 °C, 0–1000 bar“). Springer-Verlag. . Berlin. 1981. ISBN 978-3-540-09601-6.
- Helmut Lehn, Oliver Parodi: Wasser – elementare und strategische Ressource des 21. Jahrhunderts. I. Eine Bestandsaufnahme. Umweltwissenschaften und Schadstoff-Forschung 21(3), S. 272–281 (2009), ISSN 0934-3504.
- Wolfram Mauser: Wie lange reicht die Ressource Wasser? : vom Umgang mit dem blauen Gold. Fischer-Taschenbuch-Verlag, Frankfurt. . 2007. ISBN 978-3-596-17273-3. Nedostaje ili je prazan parametar
|title=(pomoć) - Erik Orsenna: Die Zukunft des Wassers : eine Reise um unsere Welt. C.H. Beck, München: 2010.
- Heinrich Sontheimer, Paul Spindler, Ulrich Rohmann: Wasserchemie für Ingenieure. DVGW-Forschungsstelle am Engler-Bunte-Institut der Uni Karlsruhe ZfGW-Verlag Frankfurt. . 1980. ISBN 978-3-922671-00-8. Nedostaje ili je prazan parametar
|title=(pomoć) - Bernd Naumann: Chemische Untersuchungen der Lebensgrundlage Wasser. Landesinstitut für Lehrerfortbildung, Lehrerweiterbildung und Unterrichtsforschung von Sachsen-Anhalt (LISA), Halle 1994, (Anregungen zur ökologischen Bildung; Bd. 2).
- Günter Wieland: Wasserchemie. 12. izdanje, Vulkan-Verlag, Essen. . 1999. ISBN 978-3-8027-2542-5. Nedostaje ili je prazan parametar
|title=(pomoć) - Karl Höll, Andreas Grohmann u. a.: Wasser. Nutzung im Kreislauf. Hygiene, Analyse und Bewertung. 8. izdanje. Walter de Gruyter. . Berlin. 2002. ISBN 978-3-11-012931-1. (Standardwerk der Wasseruntersuchung).
- Leonhard A. Hütter: Wasser und Wasseruntersuchung – Methodik, Theorie u. Praxis chemischer, chemisch-physikalischer, biologischer u. bakteriologischer Untersuchungsverfahren. Sauerländer, Frankfurt/M. . 1994. ISBN 978-3-7935-5075-4. Nedostaje ili je prazan parametar
|title=(pomoć) - Christian Opp (ed): Wasserressourcen. Nutzung und Schutz; Beiträge zum Internationalen Jahr des Süßwassers 2003. Marburger Geographische Gesellschaft, Marburg/Lahn. . 2004. ISBN 978-3-88353-049-9. Nedostaje ili je prazan parametar
|title=(pomoć) - Christian Leibundgut, Franz-Josef Kern: Wasser in Deutschland – Mangel oder Überfluss? Geographische Rundschau 58(2), S. 12–19 (2006), ISSN 0016-7460.
- Athie, Aboubacry (2002). Die politischen Implikationen der Wasserverfügbarkeit in Afrika südlich der Sahara dargestellt am Beispiel der Sahelländer Westafrikas. Berlin: Wissenschaftlicher Verlag. ISBN 978-3-936846-05-8.
- Hans Huber Abendroth: Der „Wasserkrieg“ von Cochabamba. Zur Auseinandersetzung um die Privatisierung einer Wasserversorgung in Bolivien. Bundeskammer für Arbeiter und Angestellte. . 2004. ISBN 978-3-7062-0081-3. Nedostaje ili je prazan parametar
|title=(pomoć) - Detlef Müller-Mahn: Wasserkonflikte im Nahen Osten – eine Machtfrage. Geographische Rundschau 58(2), S. 40–48 (2006), ISSN 0016-7460.
- Lisa Stadler und Uwe Hoering: Das Wasser-Monopoly. Von einem Allgemeingut und seiner Privatisierung. Rotpunktverlag, Zürich. . 2003. ISBN 978-3-85869-264-1. Nedostaje ili je prazan parametar
|title=(pomoć) - Karo Katzmann: Schwarzbuch Wasser – Verschwendung, Verschmutzung, bedrohte Zukunft. Molden, Wien. . 2007. ISBN 978-3-85485-196-7. Nedostaje ili je prazan parametar
|title=(pomoć) - Andreas Hoppe: Wasser im Nahen Osten – ein Kriegsgrund? Naturwissenschaftliche Rundschau 59(5), S. 241–247 (2006), ISSN 0028-1050.
Spoljašnje veze
[uredi | uredi izvor]- Njeno veličanstvo voda - izvor života i sukoba, specijalni prilog br.161 magazina Odbrana, Zvonimir Pešić, 1. i 15. januar 2015.
- Voda, RTS Kvadratura kruga - Zvanični kanal
- Scientific Facts on Water disinfectants A faithful summary by GreenFacts of a leading scientific consensus report on Drinking Water Disinfectants published by the International Programme on Chemical Safety of the WHO.
- World Water Forum
- World Water Assessment Program
- United Nations' World Water Development Report
- United Nations GEMS/Water Programme
- Water Structure and Behaviour
- Stockholm International Water Institute (SIWI)
- BBC: The water debate
- Voda - najveća tajna našeg doba („Večernje novosti“, feljton, jun 2015) Arhivirano na sajtu Wayback Machine (31. oktobar 2015)

