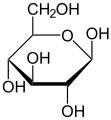
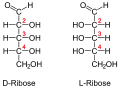Monosaharid

Monosaharid (od grčkog monos: jedan, sacchar: šećer) ugljeni hidrat je (šećer) sa najprostijom strukturom.[1][2] On se ne može hidrolizom razložiti na prostija jedinjenja šećernog karaktera.[3][4] Prema broju ugljenikovih atoma razlikuju se: trioze koje su najprostiji monosaharidi sa tri C atoma,[5][6] tetroza,[7] pentoza,[8] heksoze itd. Poznat je veliki broj monosaharida. Oni su veoma retko javljaju u prirodi u slobodnom obliku (samo oko dvadeset tipova monosaharida). Njihova jedinjenja su, međutim, veoma rasprostranjena. Opšta formula je C
nH
2nO
n. Oni su obično bezbojni, rastvorni u vodi, i kristalne materije. Neki monosaharidi imaju sladak ukus.
Primeri monosaharida su glukoza (dekstroza), fruktoza (levuloza), i galaktoza. Monosaharidi su gradivni blokovi disaharida (kao što je saharoza i laktoza) i polisaharida (kao što su celuloza i skrob). Svaki atom ugljenika koji ima hidroksilnu grupu (što su skoro svi ugljenici izuzev primarnog i krajnjeg ugljenika) je hiralan, te je prisutan znatan broj izomernih formi, sve od kojih imaju istu hemijsku formulu. Na primer, galaktoza i glukoza su obe aldoheksoze, ali imaju različite fizičke strukture i hemijska svojstava.
Podela monosaharida
[уреди | уреди извор]Monosaharid se dele u dve grupe u zavisnosti od toga da li njihov aciklični oblik poseduje aldehidnu ili keto grupu na: aldoze i ketoze.
Druga podela se vrši na osnovu broja ugljikovih atoma u lancu molekula monosaharida na: trioze, tetroze, pentoze, heksoze
-
Glicerolaldehid (primer trioze)
-
Eritroza (primer tetroze)
-
Riboza (primer pentoze)
-
Glukoza (primer heksoze)

Monosaharidi su često prisutni u cikličnom obliku (hemiacetal). Na osnovu broja atoma u prstenu dele sa na:
- Furanoze (petočlani prsten – 4 atoma ugljika i jedan atom kiseonika)
- Piranoze (šestočlani prsten – 5 atoma ugljika i jedan atom kiseonika)[9]
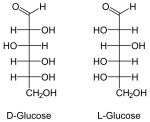
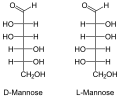
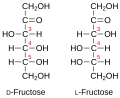
Pripadnost nekog monosaharida L ili D-seriji je određena položajem OH-grupe na pretposlednjem ugljikovom atomu, gde numerisanje počinje od aldehidne, odnosno keto grupe. Monosaharidi, koji na pretposlednjem ugljikovom atomu imaju OH-grupu s desne strane, pripadaju D-seriji optičkih izomera, bez obzira da li polarizovanu svetlost zakreću udesno ili ulevo, a ako se ta OH-grupa nalazi na levoj strani, monosaharid pripada L-seriji. Zakretanje ravni polarizovane svetlosti označava s (+) u desno i (-) u levo. Npr. D(-) fruktoza znači da D-fruktoza zakreće ravan polarizovane svetlosti ulevo, a po konfiguraciji pripada D-seriji.
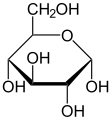
Havortove formule
[уреди | уреди извор]-
Fišerova i Havortova formula na primeru glukoze
-
α-D-glukopiranoza (Havortova formula)
-
β-D-glukopiranoza (Havortova formula)
Ciklična struktura monosaharida se često predstavlja Havortovim formulama. Intermolekularnim formiranjem hemiacetala nastaju optički izomeri koji se označavaju kao α i β. α izomer ima glikozidnu OH-grupu na desnoj strani, a u Havortovoj formuli ispod piranoznog prstena, dok β izomer ima tu OH- grupu iznad prstena.
Pregled
[уреди | уреди извор]Monosaharidi su jednostavni šećeri koji se hidrolizom ne mogu razgraditi na prostija jedinjenja koji bi imali svojstva ugljenih hidrata.[10][11] Najčešće su: heksoze (sa 6 atoma C) i pentoze (sa 5 atoma C). U heksoze spadaju: glukoza, fruktoza, maltoza, laktoza, galaktoza i manoza, a u pentoze: riboza i dezoksiriboza.
Glukoza (glikoza ili grožđani šećer) najčešće se susreće u plodovima (posebno u grožđu), hemolimfi, krvi i drugim biljnim i životinjskim organima i tečnostima. Ulazi u sastav oligosaharida i polisaharida biljnog i životinjskog porijekla, kao što su saharoza, skrob, celuloza, glikogen i dr.
Fruktoza (voćni šećer) u slobodnom stanju najraširenija je u medu i plodovima, a kod disaharida ulazi u sastav složenih molekula saharoze, rafinoze i inulina.
Galaktoza kod biljaka ulazi u sastav polisaharida galaktana, a kod životinja i čoveka sastojak je mlečnog šećera (laktoza).
Manoza se uglavnom susreće kod biljaka, kao monomer u molekulima složenih ugljenih hidrata - polisaharida.[12]
Pentoze su uglavnom sastojci složenih makromolekula nukleinskih kiselina, odnosno nukleoproteida.
Osim samostalnih jedinjenja monosaharidi mogu učestvovati u građi ostalih složenih ugljenih hidrata (oligosaharida i polisaharida). U zavisnosti o prisustvu aldehidne i keto grupe, dele se na aldoze i ketoze. Slatkog su okusa i rastvorni u vodi.
Od monosaharida, kao osnovni energent, u živom svetu najčešće se sreće glukoza (sa 6 atoma ugljenika), koja ulazi i u sastav: skroba, glikogena, celuloze i drugih jedinjenja šećera. U strukturi molekula glukoze, na ugljenikovim atomima koji nose oznaku 1 i 4, OH grupa može biti levo i desno od ravni polarizirane svjetlosti.
Delovanjem mineralnih kiselina (HCl, HN03, H2 S04) monosaharidi mogu se prevoditi u estre. Među najbitnijim estrima za živi svet su glukoza-6-fosfat i glukoza-1, 6- fosfat, preko kojih se odvija metabolizam šećera.
Spajanjem 2-10 molekula monosaharida, uz izdvajanje odgovarajućeg broja oligosaharida (grč. oligoi = malo njih).[12]
Hemijske osobine
[уреди | уреди извор]Redukcija
[уреди | уреди извор]Monosaharidi podliježu reakciji redukcije analogno aldehidima pri čemu nastaju polihidroksilni alkoholi. Npr. redukcijom D-glukoze nastaje alkohol sorbitol.
Oksidacija
[уреди | уреди извор]Oksidacijom aldehidne grupe iz monosaharida nastaju kiseline. Produkt oksidacije monosaharida zavisi od jačine oksidansa. Blagim oksidacijskim sredstvima se oksidira aldehidna grupa (nastaju polihidroksi-monokarboksilne kiseline), dok jača oksidacijska sredstva oksidiraju i primarnu OH-grupu na poslednjem ugljikovom atomu. Npr. oksidacijom glukoze nastaje glukonska kiselina, a daljom oksidacijom glukuronska kiselina.
Kvalitativne reakcije
[уреди | уреди извор]Redukcione osobine monosaharida se dokazuju sledećim reakcijama:
- Redukcija Felingovog reagensa: [Cu(NH3)4](OH)2 pomešan s rastvorom K, Na-tartarata u prisustvu reducirajućih monosaharida nastaje crveni talog bakar(I) oksida
- Redukcija Benediktovog reagensa: Rastvor Cu2+ jona kompleksiran natrijum citratom u prisustvu reducirajućih monosaharida daje crveni talog bakar(I) oksida
- Redukcija Tolensovog reagensa: [Ag(NH3)2](OH) - u prisustvu reducirajućih monosaharida redukuje se Ag+ jon do elementarnog srebra, koje se istaloži na zidovima posude (reakcija srebrnog ogledala).
Vidi još
[уреди | уреди извор]Reference
[уреди | уреди извор]- ^ „Carbohydrates”. Chemistry for Biologists. Royal Society of Chemistry. Приступљено 10. 3. 2017.
- ^ Collins, Peter M.; Ferrier, Robert J. (1995). Monosaccharides : their chemistry and their roles in natural products (на језику: енглески). Robert J. Ferrier. Chichester: Wiley & Sons. стр. 4. ISBN 0-471-95343-1. OCLC 30894482.
- ^ „Definition of Saccharification”. www.merriam-webster.com (на језику: енглески). Архивирано из оригинала 7. 1. 2021. г. Приступљено 8. 9. 2020.
- ^ Steane, Richard. „Condensation and Hydrolysis”. www.biotopics.co.uk. Архивирано из оригинала 2020-11-27. г. Приступљено 2020-11-13.
- ^ „Trioses - Three Carbon Sugars”. Oxford University Press. Приступљено 2011-07-10.
- ^ „Glycolysis in Detail”. Ohio State University at Mansfield. Приступљено 2011-07-10.
- ^ Batt RD, Dickens F, Williamson DH (новембар 1960). „Tetrose metabolism. 2. The utilization of tetroses and tetritols by rat tissues”. The Biochemical Journal. 77 (2): 281—94. PMC 1204983
 . PMID 13687765. doi:10.1042/bj0770281.
. PMID 13687765. doi:10.1042/bj0770281.
- ^ "D-Ribose". PubChem compound webpage, accessed on 2010-02-06.
- ^ Robert Meyers (Editor): Encyclopedia of physical science and technology, Third edition, Ramtech Limited, Kalifornija. 2001. ISBN 978-0-12-227410-7.
- ^ Lindhorst, Thisbe K. (2007). Essentials of Carbohydrate Chemistry and Biochemistry (1st изд.). Wiley-VCH. ISBN 978-3-527-31528-4.
- ^ Robyt, John F. (1997). Essentials of Carbohydrate Chemistry (1 изд.). Springer. ISBN 0-387-94951-8.
- ^ а б Međedović S.; Maslić E.; Hadžiselimović R. (2002). Biologija 2. Sarajevo: Svjetlost. ISBN 978-9958-10-222-6.
Literatura
[уреди | уреди извор]- Garrett, Reginald H; Grisham, Charles M (2017). Biochemistry. Boston, MA: Cengage Learning. стр. 755—794. ISBN 978-1-305-57720-6.
- McMurry, John. Organic Chemistry. 7th ed. Belmont, CA: Thomson Brooks/Cole, 2008. Print.
- Pigman, Ward; Anet, E.F.L.J. (1972). „Chapter 4: Mutarotations and Actions of Acids and Bases”. Ур.: Pigman and Horton. The Carbohydrates: Chemistry and Biochemistry Vol 1A (2nd изд.). San Diego: Academic Press. стр. 165—194.
- Pigman, Ward; Horton, D. (1972). „Chapter 1: Stereochemistry of the Monosaccharides”. Ур.: Pigman and Horton. The Carbohydrates: Chemistry and Biochemistry Vol 1A (2nd изд.). San Diego: Academic Press. стр. 1—67.
- Campbell, Neil A.; Williamson, Brad; Heyden, Robin J. (2006). Biology: Exploring Life. Boston, Massachusetts: Pearson Prentice Hall. ISBN 978-0-13-250882-7.
- Ahern, K. G.; K. E. Van Holde; Matthews, C. E. (1999). Biochemistry (3rd изд.). Benjamin Cummings. ISBN 978-0-8053-3066-3.
- Burtis, Carl A.; Ashwood, Edward R.; (PhD.), Barbara Border; Tietz, Norbert W. (2001). Tietz Fundamentals of Clinical Chemistry. Palme yayıncılık. ISBN 978-0-7216-8634-9.
- Coulter, John Merle; Barnes, Charler Reid; Cowles, Henry Chandler (2009). A Textbook of Botany for Colleges and Universities. BiblioBazaar. стр. 375. ISBN 978-1-113-90995-4.
- Maton, Anthea; Hopkins, Jean; McLaughlin, Charles William; Johnson, Susan; Warner, Maryanna Quon; LaHart, David; Wright, Jill D. (1993). Human Biology and Health. Englewood Cliffs, New Jersey, USA: Prentice Hall. стр. 52-59. ISBN 978-0-13-981176-0.
- Solomon, Eldra Pearl; Berg, Linda R.; Martin, Diana W. (2004). Biology. Cengage Learning. стр. 52. ISBN 978-0534278281 — преко google.books.com.
- „Compolition of foods raw, processed, prepared” (PDF). www.ars.usda.giv. 2015. Приступљено 30. 10. 2016.
- Alfarouk KO, Verduzco D, Rauch C, Muddathir AK, Adil HH, Elhassan GO, et al. (18. 12. 2014). „Glycolysis, tumor metabolism, cancer growth and dissemination. A new pH-based etiopathogenic perspective and therapeutic approach to an old cancer question”. Oncoscience. 1 (12): 777—802. PMC 4303887
 . PMID 25621294. doi:10.18632/oncoscience.109.
. PMID 25621294. doi:10.18632/oncoscience.109. - Romano AH, Conway T (1996). „Evolution of carbohydrate metabolic pathways”. Research in Microbiology. 147 (6–7): 448—455. PMID 9084754. doi:10.1016/0923-2508(96)83998-2.
- Keller MA, Turchyn AV, Ralser M (април 2014). „Non-enzymatic glycolysis and pentose phosphate pathway-like reactions in a plausible Archean ocean”. Molecular Systems Biology. 10 (4): 725. PMC 4023395
 . PMID 24771084. doi:10.1002/msb.20145228.
. PMID 24771084. doi:10.1002/msb.20145228. - Oshima, Kintaro; Tollens, B. (мај 1901). „Ueber Spectral‐Reactionen des Methylfurfurols”. Berichte der Deutschen Chemischen Gesellschaft (на језику: енглески). 34 (2): 1425—1426. ISSN 0365-9496. doi:10.1002/cber.19010340212.
- Seager, Spencer L.; Slabaugh, Michael R.; Hansen, Maren S. (2016-12-05). Safety Scale Laboratory Experiments (на језику: енглески). Cengage Learning. стр. 358. ISBN 9781337517140.
- Pavia, Donald L. (2005). Introduction to Organic Laboratory Techniques: A Small Scale Approach (на језику: енглески). Cengage Learning. стр. 447. ISBN 0534408338.