Радиоизотоп




Радиоизотоп (радиоактивни нуклид, радионуклид или радиоактивни изотоп) радиоактивни је изотоп једног хемијског елемента (супротан стабилном изотопу). Атомска језгра се јављају у два типа, стабилан и нестабилан. За она која припадају нестабилном типу, каже се да су радиоактивна. Нестабилна језгра се преко радиоактивног распада евентуално могу трансформисати у стабилна. Појам радиоизотоп се такође користи за било који тип радиоактивних атома. Док је само дванаестак радиоизотопа пронађено у природи у значајним количинама, на стотине других је вештачки створено бомбардовањем стабилних атомских језгара атомским пројектилима.
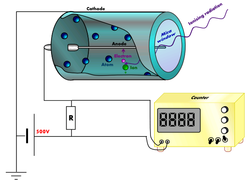
Радиоизотоп има вишак нуклеарне енергије, што га чини нестабилним. Овај вишак енергије може се користити на један од три начина: емитује се из језгра као гама зрачење; преноси се на један од његових електрона да би га ослободио као конверзијски електрон;[1][2] или се користи за стварање и емитовање нове честице (алфа честица или бета честица) из језгра. Током тих процеса, за радионуклид се каже да се радиоактивно распада.[3] Ове емисије се сматрају јонизујућим зрачењем, јер су довољно снажне да ослобађају електрон из другог атома. Радиоактивни распад може произвести стабилан нуклид или ће понекад произвести нови нестабилни радионуклид који може проћи кроз даље распадање. Радиоактивни распад је случајан процес на нивоу појединачних атома: немогуће је предвидети када ће се поједини атом распасти.[4][5][6][7] Међутим, за колекцију атома једног елемента, брзина распадања, а тиме и време полураспада (t1/2) за ту колекцију, може се израчунати из њихове измерене константе распадања. Распон времена полураспада радиоактивних атома нема позната ограничења и обухвата временски распон од преко 55 редова величине.
Радионуклиди се јављају природно или се вештачки производе у нуклеарним реакторима, циклотронима, акцелераторима честица или генераторима радионуклида. Постоји око 730 радионуклида са периодима полураспада дужим од 60 минута (погледајте списак нуклида). Тридесет и два су исконски радионуклиди који су створени пре формирања земље. У природи је могуће открити још најмање 60 радионуклида, било као ћерке исконских радионуклида, било као радионуклиде произведене природном производњом на Земљи космичким зрачењем. Више од 2400 радионуклида има време полураспада мање од 60 минута. Већина се производи само вештачки и имају врло кратак полуживот. Поређења ради, постоји око 252 стабилна нуклида. (У теорији, само њих 146 је стабилно, а за осталих 106 се верује да пропадају алфа распадом, бета распадом, двоструким бета распадом, хватањем електрона или двоструким хватањем електрона.)
Подела радионуклида
[уреди | уреди извор]Преко 60 радиоактивних елемената или радионуклида се може наћи у природи и они се могу сврстати у три категорије:[8]
- Праисконски радионуклиди - радиоактивни елементи који постоје од настанка Земље;
- Космогени радионуклиди - настали као последица космичког зрачења;[9]
- Радионуклиди настали људском активношћу. Радиоактивни елементи се често називају радиоактивни изотопи, радионуклиди или једноставно нуклиди. Постоји преко 1500 различитих радиоактивних нуклида. Они се означавају помоћу хемијског симбола и атомске масе. Радионуклиди се налазе у ваздуху, води, тлу и у живим бићима, и они су производ људских активности и природне околине. Сваки дан људи уносе у своје тело нуклиде путем ваздуха, хране и воде. Не постоји место на земљи где нема природне радиоактивности.[10][11]
Просечна еквивалентна доза износи око 3 mSv по особи годишње. Око 82% од укупне примљене апсорбоване дозе узрокују природни извори зрачења, од којега је највећи део од радона. Остатак од 18% зрачења долази од вештачких извора. То су пре свега медицинске дијагнозе и третмани.[12]
Праисконски радионуклиди
[уреди | уреди извор]Праисконски радионуклиди постоје од постанка света. Они су дугоживући радионуклиди са временом полураспада реда величине 100 милиона година. Активност радионуклида који постоје дуже од 30 времена властитих полуживота је немерљива. Потомци и продукти распада праисконских нуклида такође спадају у праисконске нуклиде. Примери праисконских радионуклида су:
- уранијум-235 (време полураспада је 7,04 x 108 година): има га у просеку око 0,72% од укупне количине природног уранијума (у налазиштима и рудницима уранијума);[13]
- уранијум-238 (време полураспада је 4,47 x 109 година): има га у просеку око 99,27% од укупне количине природног уранијума (у налазиштима и рудницима уранијума); има га 0,00005% до 0,00047% у уобичајеним врстама стена;
- торијум-232 (време полураспада је 1,41 x 1010 година): има га од 0,00016 до 0,002% у уобичајеним врстама стена са уобичајеним просеком од 0,00107%;
- радијум-226 (време полураспада је 1,6 x 103 година): има га око 16 Bq/kg у кречњаку и 48 Bq/kg у вулканским стенама;
- радон-222 (време полураспада је 3,82 дана): то је племенити гас, а годишњи просек концентрације у ваздуху 0,6 Bq/m3 до 28 Bq/m3;
- калијум-40 (време полураспада је 1,28 x 109 година): има га у тлу од 0,037 до 1,1 Bq/g. Просечна еквивалентна доза због природне радиоактивности (калијум-40, угљеник-14) људског тела је 0,40 mSv/годину.
Неки нуклиди имају више корака при распадању тако да од њих кроз време настају многи други нуклиди. На примеру торијума се види временски редослед распадања, односно промене нуклида једног у други: Th-232 --> Ra-228 --> Ac-228 --> Th-228 --> Ra-224 --> Rn-220 --> Po-216 --> Pb-212 --> Bi-212 --> Po-212 --> Pb-208 (стабилан). Неки од таквих нуклида су: V-50, Rb-87, Cd-113, In-115, Te-123, La-138, Ce-142Ce, Nd-144, Sm-147, Gd-152, Hf-174, Lu-176, Re-187, Pt-190, Pt-192, Bi-209.
Космогени радионуклиди
[уреди | уреди извор]Космичко зрачење испуњава цели свемир, а потиче углавном изван Сунчевог система. Зрачење се јавља у више облика, од брзих тешких честица па до високоенергетских фотона и миона. На горње слојеве атмосфере делују различите врсте зрачења, где се стварају козмогенички радиоактивни нуклиди. Они могу бити дугоживући, али су углавном краћег полуживота од праисконских нуклида. Примери учесталијих козмогеничких радионуклида су:[14]
- угљеник-14 (време полураспада је 5730 година): настаје међуделовањем космичких зрака, а природна радиоактивност је око 0,22 Bq/g. Користи се често у археологији за одређивање старости органских материја методом датирања угљеником-14;
- трицијум или H-3 (време полураспада је 12,3 година): настаје међуделовањем космичких зрака с азотом и кисеоником; има га у ручним сатовима за гледање бројчаника по ноћи (бета светлост); природна радиоактивност је око 1,2 x 10-3 Bq/kg;
- берилијум-7 (време полураспада је 53,28 дана): настаје међуделовањем космичких зрака с азотом и кисеоником; природна радиоактивност је око 0,01 Bq/kg.
Постоје још многи космички радионуклиди, неки од њих су: Be-10, Al-26, Cl-36, Kr-80, Si-32, Ar-39, Na-22, S-35, Ar-37, P-33, P-32, Mg-38, Na-24, S-38, Si-31, F-18, Cl-39, Cl-38, Cl-34m (ознака m је за метастабилно стање).
Радионуклиди настали људским деловањем
[уреди | уреди извор]Људи користе радиоактивност око стотину година и кроз то време неки радионуклиди су настали људским деловањем. Количине таквих нуклида су мање него количине козмогеничких радионуклида. Они обично имају краће време полураспада од праисконских и козмогеничких нуклида. Забраном тестирања нуклеарног оружја изнад површине земље, забележен је пад тако насталих радионуклида. Неки од нуклида који су настали људским деловањем су:[15]
- трицијум или H-3 (време полураспада је 12,3 година): настао тестирањем оружја и у нуклеарним реакторима; настао производњом нуклеарног оружја;
- јод-131 (време полураспада је 8,04 дана): продукт нуклеарне фисије у реакторима и тестирању оружја; медицинско лечење болести штитне жлезде;
- јођ129 (време полураспада је 1,57 x 107 година): продукт нуклеарне фисије у реакторима и тестирању оружја;
- цезијум-137 (време полураспада је 30,17 година): продукт нуклеарне фисије у реакторима и тестирању оружја;
- стронцијум-90 (време полураспада је 28,78 година): продукт нуклеарне фисије у реакторима и тестирању оружја;
- технецијум-99м (време полураспада је 6,03 сати): продукт распада Mo-99, користи се у дијагностичке сврхе (радиологија – нуклеарна медицина);
- технецијум-99 (време полураспада је 2,11 x 105 година): продукт распада технецијума-99m
- плутонијум-239 (време полураспада је 2,41 x 104 година): настаје неутронским бомбардовањем уранијума-238 (U-238 + n--> U-239--> Np-239 +ß--> Pu-239+ß)
Попис доступних радионуклида на тржишту
[уреди | уреди извор]За добијање само гама зрачења
[уреди | уреди извор]| Радионуклид | Радиоактивност | Време полураспада | Енергија (KeV) |
|---|---|---|---|
| Баријум-133 | 1 μCi | 10,7 година | 81,0, 356,0 |
| Кадмијум-109 | 1 μCi | 453 дана | 88,0 |
| Кобалт-57 | 1 μCi | 270 дана | 122,1 |
| Кобалт-60 | 1 μCi | 5,27 година | 1173,2, 1332,5 |
| Европијум-152 | 1 μCi | 13,5 година | 121,8, 344,3, 1408,0 |
| Манган-54 | 1 μCi | 312 дана | 834,8 |
| Натријум-22 | 1 μCi | 2,6 година | 511,0, 1274,5 |
| Цинк-65 | 1 μCi | 244 дана | 511,0, 1115,5 |
| Техницијум-99m | 1 μCi | 6,01 сати | 140 |
За добивање само бета-честица
[уреди | уреди извор]| Радионуклид | Радиоактивност | Време полураспада | Енергија (KeV) |
|---|---|---|---|
| Стронцијум-90 | 0,1 μCi | 28,5 година | 546,0 |
| Талијум-204 | 1 μCi | 3,78 година | 763,4 |
| Угљеник-14 | 10 μCi | 5730 година | 49,5 (просечно) |
За добивање само алфа-честица
[уреди | уреди извор]| Радионуклид | Радиоактивност | Време полураспада | Енергија (KeV) |
|---|---|---|---|
| Полонијум-210 | 0,1 μCi | 138 дана | 5304,5 |
За добивање више различитих елементарних честица ионизирајућег зрачења
[уреди | уреди извор]| Радионуклид | Радиоактивност | Време полураспада | Енергија (KeV) | |
|---|---|---|---|---|
| Цезијум-137 | 1, 5, 10 μCi | 30,1 година | Гама и бета распад | Г: 32, 661,6 Б: 511,6, 1173,2 |
Види још
[уреди | уреди извор]Референце
[уреди | уреди извор]- ^ Loveland, Walter D. (2005). Modern Nuclear Chemistry. Wiley. стр. 232. ISBN 0471115320.
- ^ M.E. Rose: "Theory of Internal Conversion", in: Alpha-, Beta- and Gamma-Ray Spectroscopy, ed. by Kai Siegbahn, North-Holland Publishing, Amsterdam (1966), Vol. 2
- ^ R.H. Petrucci, W.S. Harwood and F.G. Herring, General Chemistry (8th ed., Prentice-Hall 2002), p.1025–26
- ^ „Decay and Half Life”. Приступљено 2009-12-14.
- ^ Stabin, Michael G. (2007). „3”. Ур.: Stabin, Michael G. Radiation Protection and Dosimetry: An Introduction to Health Physics (Submitted manuscript). Springer. ISBN 978-0387499826. doi:10.1007/978-0-387-49983-3.
- ^ Best, Lara; Rodrigues, George; Velker, Vikram (2013). „1.3”. Radiation Oncology Primer and Review. Demos Medical Publishing. ISBN 978-1620700044.
- ^ Loveland, W.; Morrissey, D.; Seaborg, G.T. (2006). Modern Nuclear Chemistry. Modern Nuclear Chemistry. Wiley-Interscience. стр. 57. Bibcode:2005mnc..book.....L. ISBN 978-0-471-11532-8.
- ^ [1] Архивирано на сајту Wayback Machine (16. јул 2011) "Radionuklid", www.zpr.fer.hr, 2001.
- ^ Eisenbud, Merril; Gesell, Thomas F (1997-02-25). Environmental Radioactivity: From Natural, Industrial, and Military Sources. стр. 134. ISBN 9780122351549.
- ^ Bagnall, K.W. (1962). The Chemistry of Polonium. Advances in Inorganic Chemistry and Radiochemistry. 4. New York: Academic Press. стр. 197—229. ISBN 0-12-023604-4. doi:10.1016/S0065-2792(08)60268-X.
- ^ Bagnall, K. W. (1962). "The Chemistry of Polonium". Advances in Inorganic Chemistry and Radiochemistry 4. New York: Academic Press, p. 198
- ^ [2] Архивирано на сајту Wayback Machine (25. новембар 2012) "Jedinica radioaktivnosti", www.radiobiologija.vef.unizg.hr, 2011.
- ^ [3][мртва веза] "Uvod u nuklearnu energetiku", Prof. dr. sc. Danilo Feretić, 2011.
- ^ [4] Архивирано на сајту Wayback Machine (5. јул 2010) "Jonizirajuće zračenje u biosferi", Nuklearna elektrana Krško, Mile Dželalija, Kemijsko-tehnološki fakultet, Sveučilište u Splitu, 2011.
- ^ [5] Архивирано на сајту Wayback Machine (6. јануар 2012) "Fizika - Slikovne dijagnostike za medicinare", Davor Eterović, 2011.
Литература
[уреди | уреди извор]- Carlsson, J.; Aronsson, Eva Forssell; Hietala, SO; Stigbrand, T; Tennvall, J (2003). „Tumour therapy with radionuclides: assessment of progress and problems”. Radiotherapy and Oncology. 66 (2): 107—117. PMID 12648782. doi:10.1016/S0167-8140(02)00374-2.
- „Radioisotopes in Industry”. World Nuclear Association. Архивирано из оригинала 27. 02. 2013. г. Приступљено 18. 05. 2012.
- Martin, James (2006). Physics for Radiation Protection: A Handbook. стр. 130. ISBN 978-3-527-40611-1.
- Luig, H.; Kellerer, A. M.; Griebel, J. R. (2011). „Radionuclides, 1. Introduction”. Ullmann's Encyclopedia of Industrial Chemistry. ISBN 978-3527306732. doi:10.1002/14356007.a22_499.pub2.
Спољашње везе
[уреди | уреди извор]- EPA – Radionuclides – EPA's Radiation Protection Program: Information.
- FDA – Radionuclides – FDA's Radiation Protection Program: Information.
- Interactive Chart of Nuclides Архивирано на сајту Wayback Machine (10. октобар 2018) – A chart of all nuclides
- National Isotope Development Center – U.S. Government source of radionuclides – production, research, development, distribution, and information
- The Live Chart of Nuclides – IAEA
- Radionuclides production simulator – IAEA
