Ванадијум
 узорак | ||||||||||||||||||||||||||||
| Општа својства | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Име, симбол | ванадијум, V | |||||||||||||||||||||||||||
| Изглед | плаво-сребрно-сиви метал | |||||||||||||||||||||||||||
| У периодном систему | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Атомски број (Z) | 23 | |||||||||||||||||||||||||||
| Група, периода | група 5, периода 4 | |||||||||||||||||||||||||||
| Блок | d-блок | |||||||||||||||||||||||||||
| Категорија | прелазни метал | |||||||||||||||||||||||||||
| Рел. ат. маса (Ar) | 50,9415(1)[1] | |||||||||||||||||||||||||||
| Ел. конфигурација | ||||||||||||||||||||||||||||
по љускама | 2, 8, 11, 2 | |||||||||||||||||||||||||||
| Физичка својства | ||||||||||||||||||||||||||||
| Тачка топљења | 2183 K (1910 °C, 3470 °F) | |||||||||||||||||||||||||||
| Тачка кључања | 3680 K (3407 °C, 6165 °F) | |||||||||||||||||||||||||||
| Густина при с.т. | 6,11 g/cm3 | |||||||||||||||||||||||||||
| течно ст., на т.т. | 5,5 g/cm3 | |||||||||||||||||||||||||||
| Топлота фузије | 21,5 kJ/mol | |||||||||||||||||||||||||||
| Топлота испаравања | 444 kJ/mol | |||||||||||||||||||||||||||
| Мол. топл. капацитет | 24,89 J/(mol·K) | |||||||||||||||||||||||||||
Напон паре
| ||||||||||||||||||||||||||||
| Атомска својства | ||||||||||||||||||||||||||||
| Електронегативност | 1,63 | |||||||||||||||||||||||||||
| Енергије јонизације | 1: 650,9 kJ/mol 2: 1414 kJ/mol 3: 2830 kJ/mol (остале) | |||||||||||||||||||||||||||
| Атомски радијус | 134 pm | |||||||||||||||||||||||||||
| Ковалентни радијус | 153±8 pm | |||||||||||||||||||||||||||
| Остало | ||||||||||||||||||||||||||||
| Кристална структура | унутрашњецентр. кубична (BCC) | |||||||||||||||||||||||||||
| Брзина звука танак штап | 4560 m/s (на 20 °C) | |||||||||||||||||||||||||||
| Топл. ширење | 8,4 µm/(m·K) (на 25 °C) | |||||||||||||||||||||||||||
| Топл. водљивост | 30,7 W/(m·K) | |||||||||||||||||||||||||||
| Електрична отпорност | 197 nΩ·m (на 20 °C) | |||||||||||||||||||||||||||
| Магнетни распоред | парамагнетичан | |||||||||||||||||||||||||||
| Магнетна сусцептибилност (χmol) | +255,0·10−6 cm3/mol (298 K)[2] | |||||||||||||||||||||||||||
| Јангов модул | 128 GPa | |||||||||||||||||||||||||||
| Модул смицања | 47 GPa | |||||||||||||||||||||||||||
| Модул стишљивости | 160 GPa | |||||||||||||||||||||||||||
| Поасонов коефицијент | 0,37 | |||||||||||||||||||||||||||
| Мосова тврдоћа | 6,7 | |||||||||||||||||||||||||||
| Викерсова тврдоћа | 628–640 MPa | |||||||||||||||||||||||||||
| Бринелова тврдоћа | 600–742 MPa | |||||||||||||||||||||||||||
| CAS број | 7440-62-2 | |||||||||||||||||||||||||||
| Историја | ||||||||||||||||||||||||||||
| Откриће | Андрес Мануел дел Рио (1801) | |||||||||||||||||||||||||||
| Прва изолација | Хенри Енфилд Роско (1867) | |||||||||||||||||||||||||||
| Именовање и епоним | Нилс Габријел Сефстрем (1830) | |||||||||||||||||||||||||||
| Главни изотопи | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
Ванадијум (V, лат. vanadium) метал је VB групе, прелазних метала.[3][4] [5] Има 11 изотопа чије се атомске масе налазе између 44-55. Постојан је само 51. Заступљен је у земљиној кори у количини од 80 ppm (енгл. parts per million) у облику минерала: патронита и ванданита. Открио га је 1801. мексички научник, Андрес Мануел дел Рио. Име је добио по скандинавској богињи Ванадис.
Ванадијум гради неколико оксида са оксидационим бројем од 1 до 5 са различитим кристалним структурама. Многи од њих су нашли примену у индустрији као катализатори оксидационих реакција у органској хемији. Ванадијум је лиснат, сребрнаст метал, лоших механичких особина. Ипак он се додаје челику да би побољшао његову отпорност на отирање и пуцање. Због малих количина његових руда и због његове војне примене он представља метал од стратешке важности.
Биолошки значај: Ванадијум се налази у човековом окружењу и у његовој исхрани. У човековом организму он се јавља у траговима. Препоручљиво га је уносити у количини од 10 микрограма. Код особа које се редовно и правилно хране не долази до недостатка ванадијума. Ванадијумом може доћи до индустријског загађења животне средине, најзначајнији ефекти су: оштећење бубрега, надражај слузокоже система за дисање и за варење. За многе живе организме ванадијум је есенцијални минерал. Тако на примјер ванадијум има одређену улогу при управљању ензимима који учествују у фосфорисању, а користе га и неке бактерије за фиксирање азота. С друге стране, за њега или његова једињења сумња се да делују као мутагени кластогени који изазивају промене на хромозомима те су проглашени отровима и карциногенима.[6] Ванадијум је елемент који се налази у ензимима који мењају глукозу и друге шећере.
Историја[уреди | уреди извор]

Метал, за који се касније испоставило да је ванадијум, открио је шпански минералог Андрес Мануел дел Рио у мексичкој руди олова, касније названој ванадинит. Нови елемент, он је назвао панхромијум због његове разноликости у погледу боја, а касније је преименован у еритронијум, јер су његове соли након закисељавања добијале црвену боју. Међутим, дел Риово откриће су оповргавали Александар фон Хумболт, те касније и француски хемичар Х.В. Колет-Десотилс због сличности ванадијума са једињењима хрома, те су сматрали да се код наводног новог елемента ради о хрому са одређеним примесама.[7]
Ванадијум је поновно открио 1830. године шведски хемичар Нилс Габриел Сефстрем. Он је испитивао жељезо из шведског рудника жељеза Таберг, тако што је руду растварао у хлороводоничној киселини. При томе је поред других познатих материјала открио и један непознати елемент, који је у неким особинама доста наликовао хрому, али је такође показивао и особине својствене уранијуму. Међутим, након каснијих испитивања, није се радило о ова два елемента. Новом елементу дали су име по Ванадису, другом имену нордијске богиње Фреје. Недуго затим Фридрих Велер, који се са Берцелијусом већ с тим бавио, пружио је доказ идентитета и повезао ванадијум са раније описаним еритронијумом.[8][9]
Ванадијум у чистом, металном облику први је сачинио Хенри Енфилд Роско 1867. путем редукције ванадијум(II) хлорида са водоником. Чисти 99,7% ванадијум добили су Џон Весли Марден и Малколм Рич 1925. године редукцијом ванадијум(V) оксида са калцијумом.[10] У Енглеској се од 1903. почео користити ванадијум за легирање челика. Већа употреба овог елемента у индустрији челика отпочела је 1905. када је Хенри Форд почео да користи ванадијумске челике у производњи својих аутомобила.[11]
Особине[уреди | уреди извор]
Физичке[уреди | уреди извор]
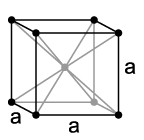
Ванадијум је немагнетични, тврди али ковни тешки метал, челично-плаве нијансе. Има густину од 6,11 g/cm3.[11] Чисти ванадијум је релативно мек, али у присуству и најмање количине примесе других елемената постаје изузетно тврд и има изузетно велику механичку чврстоћу. По већини особина, он наликује свом „комшији” из периодног система, титанијуму. Тачка топљења чистог ванадијума износи 1910 °C, а ако су присутне нечистоће, попут угљеника, она је знатно виша. Тако на пример при уделу од око 10% угљеника, тачка топљења износи око 2700 °C.[12] Ванадијум се кристализује слично као хром или ниобијум у кубној просторно-центрираној кристалној структури са Im3m и параметром решетке a = 302,4 pm као и две формулске јединице по елементарној ћелији.[13]
Испод критичне температуре од 5,13 K, ванадијум постаје суперпроводник.[14] Као и чисти ванадијум, и његове легуре са галијумом, ниобијумом и цирконијумом такође су суперпроводници. При температурама испод 5,13 K, као и метали из његове групе ниобијум и тантал, ванадијум иситњен у сићушним грудвицама од по 200 атома исказује необичну особину електричне поларизације која до данас није објашњена. Осим њега, такву особину имају и неметали.[15][16]
Хемијске[уреди | уреди извор]
Ванадијум није племенити метал и у могућности је да реагује са многим неметалима. Изложен ваздуху задржава метални сјај неколико недеља. Међутим, након дужег временског периода постаје приметан настанак зеленкасте корозије. Уколико је потребно конзервисати метални ванадијум, он се мора држати затворен у атмосфери аргона. При високој температури напада га кисеоник и оксидира у ванадијум(V) оксид. И док са угљеником и азотом реагује тек кад је загрејан до белог усијања, реакције са флуором и хлором одвијају се и у хладном стању.
Према киселинама и базама при собној температури, ванадијум је претежно стабилан због свог танког пасивизираног слоја оксида. Напада га само флуороводонична киселина, као и киселине које делују снажно оксидирајуће, попут вруће азотне киселине, концентриране сумпорне киселине и царске воде.
До температуре од око 500 °C, ванадијум може апсорбовати водоник. При томе метал постаје веома крхак и може се врло лако претворити у прах. Водоник се може ослободити из ванадијума тек при 700 °C у вакууму.[11]
Изотопи[уреди | уреди извор]
Познато је 25 изотопа ванадијума и шест нуклеарних изомера.[17] Само два изотопа се јављају у природи. То су изотоп 50V са природном распрострањеношћу од 0,25% и 51V којег има 99,75%. Изотоп 50V је благо радиоактиван. Распада се са временом полураспада од 1,5 · 1017 година тако што 83% изотопа путем електронског захвата прелази у 50Ti док 17% изотопа путем β−-распада прелази у 50Cr.[17] Оба језгра се могу користити за испитивања са НМР-спектроскопијом.
Најстабилнији вештачки изотопи су 48V са временом полураспада од 16 дана и 49V који има време полураспада од 330 дана. Ови изотопи нашли су примену у нуклеарној медицини као трасери.[12] Сви остали изотопи и нуклеарни изомери су веома нестабилни и распадају се у времену од неколико минута или секунди.
Референце[уреди | уреди извор]
- ^ Meija, J.; et al. (2016). „Atomic weights of the elements 2013 (IUPAC Technical Report)”. Pure and Applied Chemistry. 88 (3): 265—291. doi:10.1515/pac-2015-0305.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. стр. E110. ISBN 0-8493-0464-4.
- ^ Parkes, G.D. & Phil, D. (1973). Melorova moderna neorganska hemija. Beograd: Naučna knjiga.
- ^ Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. изд.). Prentice Hall. ISBN 978-0-13-175553-6.
- ^ Мишић, Милан, ур. (2005). Енциклопедија Британика. В-Ђ. Београд: Народна књига : Политика. стр. 17. ISBN 86-331-2112-3.
- ^ Juan J. Rodríguez-Mercado, Rodrigo A. Mateos-Nava, Mario A. Altamirano-Lozano: DNA damage induction in human cells exposed to vanadium oxides in vitro. u: Toxicology in Vitro 25, br. 8, 2011, str. 1996–2002, Rodríguez-Mercado, Juan J.; Mateos-Nava, Rodrigo A.; Altamirano-Lozano, Mario A. (2011). „DNA damage induction in human cells exposed to vanadium oxides in vitro”. Toxicology in Vitro. 25 (8): 1996—2002. PMID 21803147. S2CID 11236668. doi:10.1016/j.tiv.2011.07.009..
- ^ L. R. Caswell: Andres del Rio, Alexander von Humboldt, and the Twice-Discovered Element (PDF). u: Bull. Hist. Chem.. 2003, 28 (1), str. 35–41.
- ^ N. G. Sefstöm: Über das Vanadin, ein neues Metall, gefunden im Stangeneisen von Eckersholm, einer Eisenhütte, die ihr Erz von Taberg in Småland bezieht. u: Annal. d. Physik, 1831, 97 (1), str. 1–4.
- ^ Pismo Berzeliusa upućeno Wöhleru 22. januara 1831. u djelu: O. Wallach (ur.): Briefwechsel zwischen J. Berzelius und F. Wöhler. Leipzig 1901.
- ^ Vanadium. u: Encyclopædia Britannica. 2008. Encyclopædia Britannica Online, pristupljeno 6. oktobra 2008. (online).
- ^ а б в Günter Bauer et al.: Vanadium and Vanadium Compounds. u: Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim 2000, Bauer, Günter; Güther, Volker; Hess, Hans; Otto, Andreas; Roidl, Oskar; Roller, Heinz; Sattelberger, Siegfried (2000). „Vanadium and Vanadium Compounds”. Ullmann's Encyclopedia of Industrial Chemistry. ISBN 9783527303854. doi:10.1002/14356007.a27_367..
- ^ а б Arnold F. Holleman; E. Wiberg; N. Wiberg (2007). Lehrbuch der Anorganischen Chemie (102 изд.). Berlin: de Gruyter. стр. 1542-1543. ISBN 978-3-11-017770-1.
- ^ K. Schubert: Ein Modell für die Kristallstrukturen der chemischen Elemente. u: Acta Crystallographica, 1974, 30, str. 193–204, Schubert, K. (1974). „Ein Modell für die Kristallstrukturen der chemischen Elemente”. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 30: 193—204. doi:10.1107/S0567740874002469..
- ^ Aaron Waxler, William S. Corack: Superconductivity of Vanadium. u: Physical Review, 1952, 85, (1), str. 85–90, Wexler, Aaron; Corak, William S. (1952). „Superconductivity of Vanadium”. Physical Review. 85 (1): 85—90. Bibcode:1952PhRv...85...85W. doi:10.1103/PhysRev.85.85..
- ^ T. Krome: Metalle auf Abwegen. Über das ungewöhnliche Tieftemperaturverhalten winziger Metallklumpen. u: Spektrumdirekt.de od 22. maja 2003; sažetak, pristupljeno 23. oktobra 2015.
- ^ Ramiro Moro, Xiaoshan Xu, Shuangye Yin, Walt A. de Heer: Ferroelectricity in Free Niobium Clusters, u: Science, 2003, Vol. 300, br. 5623, str. 1265–1269, Moro, Ramiro; Xu, Xiaoshan; Yin, Shuangye; De Heer, Walt A. (2003). „Ferroelectricity in Free Niobium Clusters”. Science. 300 (5623): 1265—1269. Bibcode:2003Sci...300.1265M. PMID 12764191. S2CID 30993305. doi:10.1126/science.1083247..
- ^ а б G. Audi; O. Bersillon; J. Blachot; A. H. Wapstra (2003). „The NUBASE evaluation of nuclear and decay properties” (PDF). Nuclear Physics. A 729: 3—128. doi:10.1016/S0375-9474(97)00482-X. Архивирано из оригинала 24. 07. 2013. г. Приступљено 11. 01. 2021.
Литература[уреди | уреди извор]
- Slebodnick, Carla; et al. (1999). „Modeling the Biological Chemistry of Vanadium: Structural and Reactivity Studies Elucidating Biological Function”. Ур.: Hill, Hugh A.O.; et al. Metal sites in proteins and models: phosphatases, Lewis acids, and vanadium. Springer. ISBN 978-3-540-65553-4.
Спољашње везе[уреди | уреди извор]
- Vanadium at The Periodic Table of Videos (University of Nottingham)
- ATSDR – ToxFAQs: Vanadium
- Vanadium concentration in seawater and estuary environments is around 1.5-3.3 ug/kg.
- Vanadium speciation and cycling in coastal waters
- Ocean anoxia and the concentrations of Molybdenum and Vanadium in seawater


