Витамин Ц — разлика између измена
| Ред 106: | Ред 106: | ||
Губитак способности синтезе аскорбата се подудара са појавом неспособности разлагања [[уринска киселина|уринске киселине]], која је такође карактеристична за примате. Уринска киселина и аскорбат су јаки [[редукујући агенс]]и, те се претпоставља да је код виших примата, уринска киселина преузела део функција аскорбата.<ref>{{Cite journal|author=Proctor P |title=Similar functions of uric acid and ascorbate in man? |journal=Nature |volume=228 |issue=5274 |page=868 |year=1970 |pmid=5477017|doi=10.1038/228868a0}}</ref> |
Губитак способности синтезе аскорбата се подудара са појавом неспособности разлагања [[уринска киселина|уринске киселине]], која је такође карактеристична за примате. Уринска киселина и аскорбат су јаки [[редукујући агенс]]и, те се претпоставља да је код виших примата, уринска киселина преузела део функција аскорбата.<ref>{{Cite journal|author=Proctor P |title=Similar functions of uric acid and ascorbate in man? |journal=Nature |volume=228 |issue=5274 |page=868 |year=1970 |pmid=5477017|doi=10.1038/228868a0}}</ref> |
||
===Апсорпција, транспорт, и уклањање=== |
|||
Аскорбинска киселина се апсорбује у телу путем активног транспорта и једноставне дифузије. Котранспортери од натријума зависног активног транспорта натријум аскорбата (-{SVC6T}-) и хексозни транспортери (-{GLUT}-) су два транспортера неопходна за апсорпцију. -{SVCT}- су предоминантни систем за транспорт витамина Ц у телу. -{SVCT1}- и -{SVCT2}- уносе редуковану форму аскорбата кроз ћелијску мембрану.<ref name="ReferenceA">{{cite journal |author=Savini I., Rossi A., Pierro C., Avigliano L., Catani M. V. |title=SVCT1 and SVCT2: key proteins for vitamin C uptake |journal=Amino Acids |volume=34 |issue=3 |pages=347–55 |year=2007 |pmid=17541511 |doi=10.1007/s00726-007-0555-7}}</ref> -{GLUT1}- и -{GLUT3}- су два глукозна транспортера. Они преносе витамин Ц у облику дехидроаскорбинске киселине.<ref>{{cite journal |doi=10.1074/jbc.272.30.18982 |author=Rumsey SC, Kwon O, Xu GW, Burant CF, Simpson I, Levine M |title=Glucose transporter isoforms GLUT1 and GLUT3 transport dehydroascorbic acid |journal=The Journal of biological chemistry |volume=272 |issue=30 |pages=18982–9 |year=1997 |pmid=9228080}}</ref> Мада се дехидроаскорбинска киселина апсорбује брже од аскорбата, количина дехидроаскорбинске киселине у плазми и ткивима под нормалним условима је ниска, јер ћелије брзо редукују дехидроаскорбинску киселину до аскорбата.<ref>{{cite journal |author=May J, Qu Zhi-Chao, Neel Dustin R., Li Xia |title=Recycling of vitamin C from its oxidized forms by human endothelial cells |journal=Biochimica et Biophysica Acta (BBA) - Molecular Cell Research |volume=1640 |pages=153–61 |year=2003 |doi=10.1016/S0167-4889(03)00043-0 |issue=2–3}}</ref><ref>{{cite book |author=Packer, L. |year=1997 |chapter=Vitamin C and redox cycling antioxidants. |editor=Packer L, F. J.(ed). |title=Vitamin C in health and disease |publisher=Marcel Dekker Inc |location=New York}}</ref> |
|||
==Литература== |
==Литература== |
||
Верзија на датум 8. фебруар 2012. у 05:10
Један корисник управо ради на овом чланку. Молимо остале кориснике да му допусте да заврши са радом. Ако имате коментаре и питања у вези са чланком, користите страницу за разговор.
Хвала на стрпљењу. Када радови буду завршени, овај шаблон ће бити уклоњен. Напомене
|
 | |
 | |
| IUPAC име | |
|---|---|
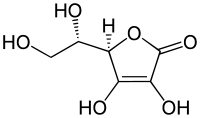
2-Оксо-L-трео-хексоно-1,4-лактон-2,3-енедиол или (R)-3,4-дихидрокси-5-((S)- 1,2-дихидроксиетил)фуран-2(5H)-он | |
| Клинички подаци | |
| Drugs.com | Мултум, информације за потрошаче |
| Категорија трудноће |
|
| Начин примене | орално |
| Правни статус | |
| Правни статус |
|
| Фармакокинетички подаци | |
| Биорасположивост | брза & комплетна |
| Везивање протеина | незнатно |
| Полувреме елиминације | варира у зависности концентрације плазме |
| Излучивање | ренално |
| Идентификатори | |
| CAS број | 50-81-7 |
| ATC код | A11G (WHO) |
| PubChem | CID 5785 |
| DrugBank | DB00126 |
| ChemSpider | 10189562 |
| UNII | PQ6CK8PD0R |
| KEGG | D00018 |
| ChEBI | CHEBI:29073 |
| ChEMBL | CHEMBL196 |
| Синоними | L-аскорбинска киселина |
| Хемијски подаци | |
| Формула | C6H8O6 |
| Моларна маса | g/mol |
| |
| |
| Физички подаци | |
| Густина | 1.694 g/cm3 |
| Тачка топљења | 190 °C (374 °F) |
| Тачка кључања | 553 °C (1.027 °F) |

Витамин Ц (L-аскорбинска киселина, L-аскорбат) је витамин код људи и више животињских врста. У живим организмима аскорбат делује као антиоксиданс, те штити тело од оксидатовног стреса.[1] Он је исто тако кофактор у најмање шест ензимских реакција, међу којима је неколико реакција колагенске синтезе, чија дисфункционалност се манифестује симптомима скорбута.[2] Код животиња су ове реакције посебно важне у зарастању рана и спречавању крварења из капилара.
Аскорбат (јон аскорбинске киселине) је неопходан у низу есенцијалних метаболичких реакција код свих животиња и биљки. Њега формира велика већина живих организама, са приметним изузетаком групе сисара, међу којима је ред слепих мишева, заморци, капибаре, и један од два главна подреда примата, антропоиди (сувоносни мајмуни) (тарсијери, мајмуни, човеколики мајмуни, и људи). Аскорбинску киселину исто тако не синтетишу поједине врсте птица и риба. Свим врстама које немају способност синтезе витамина Ц, неопходан је његов унос путем исхране. Дуготрани дефицит овог витамина се манифестује развојем скорбута.[2][3][4] Витамин Ц је један од најшире коришћених прехрамбених адитива.
Ширина опсега његовог дејства, као и препоручљива дневна доза су тема текућих дебата. Препоручене дозе се крећу у опсегу 45 до 400 mg на дан.
Биолошки значај
Витамин Ц ис чист L-енантиомер аскорбата, док супротни D-енантиомер нема физиолошког значаја. Кад L-аскорбат, који је јак редукујући агенс, обавља своје редукујуће функције, он се конвертује у оксидовани облик, L-дехидроаскорбат.[2] L-дехидроаскорбат се може затим редуковати назад у активну L-аскорбатну форму дејством ензима и глутатиона у телу.[5] Током овог процеса формира се радикал семидехидроаскорбинске киселине. Слободни радикал аскорбата слабо реагује са кисеоником, тако да се не формира супероксид. Уместо тога два радикала семидехидроаскорбата реагују и формирају један аскорбат и један дехидроаскорбат. Уз помоћ глутатиона, дехидроксиаскорбат се конвертује назад у аскорбат.[6] Присуство глутатиона је есенцијално, јер он омогућава обнављање аскорбата и побољшава антиоксидансни капацитет крви.[7] Без њега не би долазило до конверзије дехидроксиаскорбата назад у аскорбат.
L-аскорбат је слаба шећерна киселина. Он је структурно сродан са глукозом. Аскорбат се природно јавља везан било за водонични јон, дајући аскорбинску киселину, или за метални јон, формирајући минерални аскорбат.
Биосинтеза
Биосинтеза код различитих врста
Велика већина биљки и животиња има способност синтезе витамина Ц. Овај процес се одвија путем секвенце од четири трансформације које су посредоване ензимима, при чему долази до конверзије глукозе у витамин Ц.[2] Глукоза за формирање аскорбата се издваја из гликогена у јетри код сисара и врапчарки. Синтеза аскорбата је процес који је завистан од гликогенолизе.[8] Код рептила и птица биосинтеза се одвија у бубрезима.
Међу животињама које су изгубиле способност синтезе витамина Ц су симијани и тарзијери, који заједно сачињавају један од подредова примата, anthropoidea или haplorrhini. Ова група обухвата људе. Други примитивни примати (strepsirrhini) су задржали способност формирања витамина Ц. Синтеза се не јавља код бројних (можда и код свих) врста из фамилије малих глодара caviidae у којој су морско прасе и капибари, али је присутна код других глодара (на пример пацовима и мишевима није потребан витамин Ц у исхрани). Бројне врсте птица врапчарки такође не синтетишу овај витамин, мада не све од њих. Врсте птица које немају способност синтезе нису јасно повезане. По једној теорији способност синтезе је независно изгубљена више пута код птица.[9]
Све тестиране фамилије слепих мишева, што обухвата главне фамилије које се хране инсектима и воћем немају способност синтезе витамина Ц. Трагови GLO-а су детектовани само код једне од 34 тестиране врсте слепих мишева, из 6 фамилија.[10] Ранији извештаји да само слепи мишеви који се хране воћем немају способност синтезе су били засновани на мањем броју и мањој разноврсности узорака.
Код свих животиња које не могу да синтетишу витамин Ц, није присутан ензим L-гулонолактон оксидаза (GULO) ензим, који је неопходан у задњем степену синтезе. Те животиње имају различите несинтетичке гене тог ензима (псеудогене ΨGULO).[11] Сличан нефункционални ген је присутан у геному морског прасета и примата, укључујући човека.[12][13] Неке од тих врста (међу којима је човек) могу да се одрже са ниским нивоима доступним из хране путем рециклирања оксидованог витамина Ц.[14]
Већина симијана конзумира количине витамина које су 10 до 20 пута веће од препоручених за људе.[15] Овај раскорак је основа за контроверзна мишљења о тренутно препорученим дијетарним количинама. Супротни аргумент је да су људи веома ефективни у презервацији дијетарног витамина Ц, те да су способни да одрже крвне нивое витамина Ц упоредиве са другим симијанима уз далеко мањи дијетарни унос.
Одрасла коза је типичан пример животиње која производи витамин Ц. Она произведе више од 13 g витамина Ц на дан при нормалном здрављу, а биосинтеза се повећава неколико путе под стресним условима.[16] За трауме и повреде је показано да користе велике количине витамина Ц код људи.[17]
Неки микроорганизми као што је квасац Saccharomyces cerevisiae имају способност синтезе витамина Ц из једноставних шећера.[18][19]
Витамин Ц током еволуције
Вентури и Вентури[20][21] сугерирају да је антиоксидансно дејство аскорбинске киселине првобитно развијено у биљном царству кад су пре око 500 милиона година биљке почеле да се адаптирају на свежу воду ушћа река која је дефицитарна у антиоксидансним минералима. Неки биолози напомињу да су многи кичмењаци развили метаболичке адаптивне стратегије у окружењу које пружа ушћа река.[22] По овој теорији, кад су пре неких 400–300 милиона година, биљке и животиње су прво почеле да прелазе из мора у реке и на копно, средине дефицитарне у јоду су представљале препреку у еволуцији терестријалног живота.[23] Код биљака, животиња и риба, терестријална храна је постала дефицитарна у многим есенцијалним морским антиоксидансним микронутријентима, међу којима се јод, селен, цинк, бакар, манган, гвожђе, итд. Алге у свежој води и копнене биљке, као замену за морске антиоксидансе, временом су оптимизовале производњу других ендогених антиоксиданаса као што су аскорбинска киселина, полифеноли, каротеноиди, токофероли итд. Неки од њих су постали есенцијални “витамини” у исхрани копнених животиња (витамини Ц, А, Е, итд.).
Аскорбинска киселина или витамин Ц је чест кофактор ензима код сисара. Он учествује у синтези колагена. Аскорбат је јак редукујући агенс који има способност брзог сакуљања више реактивних врста кисеоника (ROS). Слатководним правим кошљорибама је такође потребан дијетарни витамин Ц у исхрани. Без њега би оне оболеле од скорбута. Симптоми недостатка витамина Ц који су најлакше препознатљиви код риба су сколиоза, лордоза и тамна боја коже. Слатководне пастрмке такође манифестују умањено формирање колагена, крварење на перајама, унутрашње крварење, закривљење кичме и повишени морталитет. Ако су те рибе живе у морској води са алгама и фитопланктоном, онда је витаминска суплементација мање важна. Сматра се да је разлог доступност других ефикаснијих антиоксиданаса у природном морском окружењу.[24]
Научници су изнели претпоставку да је губитак пута биосинтезе витамина Ц можда у складу са теоријом брзих еволуционих промена, која је довела до развоја хоминида и појаве људских бића.[25][26][27] Међутим, једна друга терија базирана на теорији еволуције наводи да се губитак способности прављења витамина Ц код симијана можда јавио знатно раније током еволуционе историје од појаве људи или чак и човеколиких мајмуна. Постоји евиденција да је до тога дошло ускоро након појаве првих примата, а вероватно након поделе раних примата у два главна подреда: хаплорхини (који не могу да праве витамин Ц) и његовог сестринског подреда netarsijer prosimijana, стрепсирхини (примати „влажног носа“), који је задржао способност прављења витамина Ц.[28] На основу датирања молекуларног часовника, та два подреда примата су се раздвојила пре око 63 до 60 милиона година.[29] Апроксимативно три до пет милиона година касније (пре 58 милиона година), што је кратак период у еволуционом смислу, ред Tarsiiformes, чија једина преостала фамилија је тарсијер (Tarsiidae), се одвојила од других хаплорхина.[30][31][32] Пошто тарсијери такође немају способност прављења витамина Ц, следи да је до мутације већ било дошло, те да је до ње морало доћи између те две раздвојне тачке (63 до 58 милиона година).
Губитак способности синтезе аскорбата се подудара са појавом неспособности разлагања уринске киселине, која је такође карактеристична за примате. Уринска киселина и аскорбат су јаки редукујући агенси, те се претпоставља да је код виших примата, уринска киселина преузела део функција аскорбата.[33]
Апсорпција, транспорт, и уклањање
Аскорбинска киселина се апсорбује у телу путем активног транспорта и једноставне дифузије. Котранспортери од натријума зависног активног транспорта натријум аскорбата (SVC6T) и хексозни транспортери (GLUT) су два транспортера неопходна за апсорпцију. SVCT су предоминантни систем за транспорт витамина Ц у телу. SVCT1 и SVCT2 уносе редуковану форму аскорбата кроз ћелијску мембрану.[34] GLUT1 и GLUT3 су два глукозна транспортера. Они преносе витамин Ц у облику дехидроаскорбинске киселине.[35] Мада се дехидроаскорбинска киселина апсорбује брже од аскорбата, количина дехидроаскорбинске киселине у плазми и ткивима под нормалним условима је ниска, јер ћелије брзо редукују дехидроаскорбинску киселину до аскорбата.[36][37]
Литература
- ^ Sebastian J. Padayatty, Arie Katz, Yaohui Wang, Peter Eck, Oran Kwon, Je-Hyuk Lee, Shenglin Chen, Christopher Corpe, Anand Dutta (2003). „Vitamin C as an antioxidant: evaluation of its role in disease prevention”. Journal of the kAmerican College of Nutrition. 22 (1): 18—35. PMID 12569111.
- ^ а б в г „Vitamin C”. Food Standards Agency (UK). Приступљено 2007-02-19. Грешка код цитирања: Неисправна ознака
<ref>; назив „UKFSA Risk” је дефинисано више пута с различитим садржајем - ^ „Vitamin C”. University of Maryland Medical Center. 2007. Приступљено 2008-03-31. Непознати параметар
|month=игнорисан (помоћ) - ^ Jane Higdon (2006-01-31). „Vitamin C”. Oregon State University, Micronutrient Information Center. Приступљено 2007-03-07.
- ^ Alton Meister (1994). „Glutathione-ascorbic acid antioxidant system in animals” (PDF). The Journal of biological chemistry. 269 (13): 9397—400. PMID 8144521.
- ^ Nualart FJ, Rivas CI, Montecinos VP; et al. (2003). „Recycling of vitamin C by a bystander effect”. J Biol Chem. 278: 10128—10133.
- ^ Gropper SS, Smith JL, Grodd JL (2004). Advanced Nutrition and Human Metabolism (4th изд.). Belmont, CA. USA: Thomson Wadsworth. стр. 260—275.
- ^ Bánhegyi Gábor, Mandl JóZsef (2001). „The hepatic glycogenoreticular system”. Pathology & Oncology Research. 7 (2): 107—110. doi:10.1007/BF03032575.
- ^ Martinez del Rio, Carlos (1997). „Can passerines synthesize vitamin C?”. The Auk. 114 (3): 513—16. JSTOR 4089257. Приступљено 2. 5. 2011. Непознати параметар
|month=игнорисан (помоћ) - ^ Jenness R, Birney E, Ayaz K (1980). „Variation of l-gulonolactone oxidase activity in placental mammals”. Comparative Biochemistry and Physiology Part B: Biochemistry and Molecular Biology. 67 (2): 195—204. doi:10.1016/0305-0491(80)90131-5.
- ^ James W. Harris (1996). Ascorbic acid: biochemistry and biomedical cell biology. New York: Plenum Press. стр. 35. ISBN 0-306-45148-4.
- ^ Nishikimi M, Kawai T, Yagi K (1992). „Guinea pigs possess a markedly different gene for L-gulono-gamma-lactone oxidase, the key enzyme for L-ascorbic acid biosynthesis missing in this species”. The Journal of biological chemistry. 267 (30): 21967—72. PMID 1400507. Непознати параметар
|month=игнорисан (помоћ) - ^ Ohta Y, Nishikimi M (1999). „Random nucleotide substitutions in primate nonfunctional gene for L-gulono-gamma-lactone oxidase, the missing enzyme in L-ascorbic acid biosynthesis”. Biochimica et biophysica acta. 1472 (1–2): 408—11. PMID 10572964. doi:10.1016/S0304-4165(99)00123-3. Непознати параметар
|month=игнорисан (помоћ) - ^ Montelhagen A, Kinet S, Manel N, Mongellaz C, Prohaska R, Battini JL, Delaunay J, Sitbon M, Taylor N (2008). „Erythrocyte Glut1 Triggers Dehydroascorbic Acid Uptake in Mammals Unable to Synthesize Vitamin C”. Cell. 132 (6): 1039—48. PMID 18358815. doi:10.1016/j.cell.2008.01.042. Генерални сажетак – Science Daily (21. 3. 2008).
- ^ Milton K (1999). „Nutritional characteristics of wild primate foods: do the diets of similar organisms have lessons for us?”. Nutrition. 15 (6): 488—98. PMID 10378206. doi:10.1016/S0899-9007(99)00078-7.
- '^ Stone Irwin (16. 7. 1978). „Eight Decades of Scurvy. The Case History of a Misleading Dietary Hypothesis”. Приступљено 2007-04-06. „'Биохемијска истраживања током 1950-тих су показала да је појава скорбута последица одсуства ензима, L-Гулонолактон оксидаза (GLO) у хуманој јетри (Burns, 1959). Тај ензим је задњи у серији од четири ензима који конвертују крвни шећер, глукозу, у аскорбат у јетри сисара. Овај метаболит јетре, аскорбат, се производи у кози под нормалним условима, на пример, у количини од око 13,000 mg на дан на 150 фунти телесне тежине (Chatterjee, 1973). Повратни механизам сисара многоструко повећава ову дневну производњу аскорбата под стресним условима (Subramanian et al., 1973)”
- ^ Long C, Maull KI, Krishnan RS, Laws HL, Geiger JW, Borghesi L, Franks W, Lawson TC, Sauberlich HE (2003). „Ascorbic acid dynamics in the seriously ill and injured”. Journal of Surgical Research. 109 (2): 144—8. PMID 12643856. doi:10.1016/S0022-4804(02)00083-5.
- ^ R.D. Hancock & R. Viola. „Ascorbic acid biosynthesis in higher plants and microorganisms” (PDF). Scottish Crop Research Institute. Приступљено 2007-02-20.
- ^ Hancock Robert D., Galpin John R., Viola Roberto (2000). „Biosynthesis of L-ascorbic acid (vitamin C) by Saccharomyces cerevisiae”. FEMS Microbiology Letters. 186 (2): 245—50. PMID 10802179. doi:10.1111/j.1574-6968.2000.tb09112.x.
- ^ {{cite journal |author=Venturi S, Venturi M. Evolution of Dietary Antioxidant Defences |journal=European EPI-Marker |year=2007 |volume=11 |issue=3 |pages=1–7 |url= http://www.icb-asbl.com/en/pdf/epimarker/epimarker_3_07.pdf
- ^ Venturi S, Donati FM, Venturi A, Venturi M (2000). „Environmental iodine deficiency: A challenge to the evolution of terrestrial life?”. Thyroid : official journal of the American Thyroid Association. 10 (8): 727—9. PMID 11014322. doi:10.1089/10507250050137851.
- ^ Purves WK, Sadava D, Orians GH, Heller HC (1998). „30”. Life. The Science of Biology. Part 4: The Evolution of Diversity.
- ^ Venturi S, Venturi M (1999). „Iodide, thyroid and stomach carcinogenesis: evolutionary story of a primitive antioxidant?”. European Journal of Endocrinology. 140 (4): 371—2. PMID 10097259. doi:10.1530/eje.0.1400371.
- ^ Hardie L.J., Fletcher T.C., Secombes C.J. (1991). „The effect of dietary vitamin C on the immune response of the Atlantic salmon (Salmo salar L.)”. Aquaculture. 95 (3–4): 201—14. doi:10.1016/0044-8486(91)90087-N.
- ^ Challem J, Taylor EW (1998). „Retroviruses, Ascorbate, and Mutations, in the Evolution of Homo sapiens”. Free Radical Biology and Medicine. 25 (1): 130—2. PMID 9655531. doi:10.1016/S0891-5849(98)00034-3.
- ^ Bánhegyi G, Braun L, Csala M, Puskás F, Mandl J (1997). „Ascorbate Metabolism and Its Regulation in Animals”. Free Radical Biology and Medicine. 23 (5): 793—803. PMID 9296457. doi:10.1016/S0891-5849(97)00062-2.
- ^ Stone I (1979). „Homo sapiens ascorbicus, a biochemically corrected robust human mutant”. Medical Hypotheses. 5 (6): 711—21. PMID 491997. doi:10.1016/0306-9877(79)90093-8.
- ^ Pollock J. I., Mullin R. J. (1987). „Vitamin C biosynthesis in prosimians: Evidence for the anthropoid affinity ofTarsius”. American Journal of Physical Anthropology. 73 (1): 65—70. PMID 3113259. doi:10.1002/ajpa.1330730106.
- ^ Poux C, Douzery E.J.P. (2004). „Primate phylogeny, evolutionary rate variations,and divergence times: a contribution from the nuclear gene IRBP”. American Journal of Physical Anthropology. 124 (1): 1—16. PMID 15085543. doi:10.1002/ajpa.10322.
- ^ Goodman M., Porter C.A., Czelusniak J., Page S.L., Schneider H., Shoshani J., Gunnell G., Groves C.P. (1998). „Toward a phylogenetic classification of primates based on DNA evidence complemented by fossil evidence”. Molecular Phylogenetics and Evolution. 9 (3): 585—598. PMID 9668008. doi:10.1006/mpev.1998.0495.
- ^ {{cite journal |author=Porter, C.A., Page, S.L., Czelusniak, J., Schneider, H., Schneider, M.P.C., Sampaio, I. and Goodman, M. |year=1997 |title=Phylogeny and evolution of selected primates as determined by sequences of the ?-globin locus and 5’flanking regions |journal=International Journal of Primatology |volume=18 |pages=261–295
- ^ „Refs Poux, Porter and Goodman preceding” (PDF).]
- ^ Proctor P (1970). „Similar functions of uric acid and ascorbate in man?”. Nature. 228 (5274): 868. PMID 5477017. doi:10.1038/228868a0.
- ^ Savini I., Rossi A., Pierro C., Avigliano L., Catani M. V. (2007). „SVCT1 and SVCT2: key proteins for vitamin C uptake”. Amino Acids. 34 (3): 347—55. PMID 17541511. doi:10.1007/s00726-007-0555-7.
- ^ Rumsey SC, Kwon O, Xu GW, Burant CF, Simpson I, Levine M (1997). „Glucose transporter isoforms GLUT1 and GLUT3 transport dehydroascorbic acid”. The Journal of biological chemistry. 272 (30): 18982—9. PMID 9228080. doi:10.1074/jbc.272.30.18982.
- ^ May J, Qu Zhi-Chao, Neel Dustin R., Li Xia (2003). „Recycling of vitamin C from its oxidized forms by human endothelial cells”. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1640 (2–3): 153—61. doi:10.1016/S0167-4889(03)00043-0.
- ^ Packer, L. (1997). „Vitamin C and redox cycling antioxidants.”. Ур.: Packer L, F. J.(ed). Vitamin C in health and disease. New York: Marcel Dekker Inc.
Спољашње везе
 | Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |