Ernest Raderford
| Ernest Raderford | |
|---|---|
 Ernest Raderford | |
| Lični podaci | |
| Datum rođenja | 30. avgust 1871. |
| Mesto rođenja | Nilson, Novi Zeland |
| Datum smrti | 19. oktobar 1937. (66 god.) |
| Mesto smrti | Kembridž, Ujedinjeno Kraljevstvo |
| Obrazovanje | University of Canterbury, Univerzitet u Kembridžu, Triniti koledž, Nelson College |
| Naučni rad | |
| Polje | fizika, hemija |
| Poznat po | otac nuklearne fizike Raderfordov model otkriće protona raderford (jedinica) |
| Nagrade | Ramfordova medalja (1905) Medalja Eliot Kreson (1910) Matelučijeva medalja (1913) Koplejeva medalja (1922) Medalja Frenklin (1924) |
| Potpis | |


Ernest Raderford (engl. Ernest Rutherford, 1st Baron Rutherford of Nelson; Nilson, 30. avgust 1871 — Kembridž, 19. oktobar 1937) je bio britanski fizičar koji se smatra ocem nuklernih reakcija.[2][3]
Bio je profesor na fakultetu u Montrealu; bio je profesor fizike na Univerzitetu u Mančesteru (od 1907), a od 1919. direktor Kevendišova laboratorije u Kembridžu. Godine 1903. izabran za člana (1925-30 za predsednika) Kraljevskog društva. Nobelovu nagradu za hemiju dobio je 1908. godine. U početku se bavio proučavanjem radioaktivnih raspada. Prvi je uočio da se zračenje radijuma sastoji od tri vrste, koje je nazvao α- β- i γ-zračenje.[4] Zajedno sa Frederikom Sodijem uveo je pojam vreme poluraspada i formulisao zakone radioaktivnog raspada. Proučavanjem raspadanja alfa-čestica na atomima Raderford je došao do zaključka da atom čija je veličina 10−8 cm nije kompaktan delić materije, nego složen od pozitivnog jezgra (veličine 10−12 cm) i elektrona koji kruže oko njega. Raderford je prvi upotrebio reč proton za pozitivno naelektrisanu česticu u jezgru atoma.
Od njega potiče i formula (nazvana njegovim imenom) za rasejanje alfa-čestica naj jezgrima atoma; kasnije (1925. godine), Raderford je utvrdio i odstupanje od te formule do kojeg dolazi kod vrlo bliskih sudara α-čestice i jezgra, kad nuklearno međudelovanje postaje mnogo važnije od električnog.[5]
Godine 1919. Raderford je, bombardujući azot alfa-česticama izveo prvu (transmutaciju) jednog elementa u drugi jer je iz azota uspeo da dobije kiseonik. Tako je izvršena prva nuklearna reakcija. Veštački hemijski element raderfordijum od 1997. godine po njemu nosi ime.
Biografija[uredi | uredi izvor]
Raderfordovi roditelji su bili farmeri, koji su emigrirali iz Škotske na Novi Zeland, da bi lakše podigli veliku porodicu. Ernest je završio elektrotehničku školu, a kasnije je putovao u Veliku Britaniju, da bi se usavršio u merenju i otkrivanju elektromagnetskih talasa. Bio je profesor na univerzitetu u Montrealu; načelnik odeljenja za fiziku univerziteta u Mančesteru (od 1907), a od 1919. direktor Kavendišove laboratorije u Kembridžu. Godine 1900. se oženio i imao je jednu kćer.[6]
Naučna istraživanja[uredi | uredi izvor]
Početkom 20. veka bilo je poznato 5 radioaktivnih elemenata: uranijum, torijum, polonijum, aktinijum i radijum. Među njima najviše se upotrebljavao radijum i to za lečenje raka. Iz radijuma i njegovih hemijskih jedinjenja stalno se razvijao jedan gas, koji je isto tako bio radioaktivan, a nazvan je radijumova emanacija ili radon. Osim radona nastajao je i helijum. Iz toga se zaključilo da se radijum, ali i svi ostali radioaktivni elementi, pretvaraju u druge elemente s manjom težinom i pri tom postupku zrače. Uočeno je takođe da je ta prirodna radioaktivnost svojstvena atomima s najvećim atomskim masama i da je to proces koji se dešava u unutrašnjosti atoma, znači ne zavisi od spoljnih uticaja, kao što su pritisak, temperatura ili neka hemijska reakcija.
Radioaktivno zračenje[uredi | uredi izvor]
Već 1900. bilo je poznato da jedan deo radioaktivnog zračenja može da skreće u magnetskom polju. Raderford je na osnovu ispitivanja prolaza radioaktivnih zraka kroz tanke listiće aluminijuma utvrdio da kod zračenja uranijumovih jedinjenja postoje dve vrste zraka. Onu vrstu zraka koji ne mogu da prođu kroz aluminijsku pločicu debljine 0,02 mm nazvao je alfa-česticama, a onu vrstu koja je prolazila i kroz deblje slojeve nazvao je beta-česticama. Iste godine francuski naučnik Pol Vilard je otkrio i treću vrstu radioaktivnog zračenja, za koju se utvrdilo da ima veliku prodornu moć i da ne skreće u magnetskom polju, a nazvana je gama-česticama. Na osnovu skretanja u magnetskom polju, utvrđeno je da alfa-čestice imaju pozitivni električni naboj, a beta-čestice negativan električni naboj.
Godine 1908. su Raderford i Hans Gajger merenjem utvrdili da alfa-čestice imaju dvostruki električni naboj, a da im je masa jednaka četvorostrukoj masi atoma vodonika. Kada alfa-čestica privuče dva elektrona, ona prelazi u atom helijuma.[7][8] Iz toga je Raderford zaključio da su alfa-čestice u stvari joni helijuma ili samo atomska jezgra helijuma. Za beta-čestice se utvrdilo da se u magnetnom i električnom polju ponašaju isto kao i katodni zraci ili elektroni. To znači da su beta-čestice u stvari elektroni velikih brzina, ali za razliku od elektrona u elektronskom omotaču atoma, nastaju iz atomskog jezgra.
Za gama-čestice je utvrđeno da odgovaraju tvrdim rendgenskim zrakama. To su dokazali Raderford i E. N. da Kosta Andrade 1914, difrakcijom gama-čestica kroz odgovarajuću kristalnu rešetku, pomoću koje su uspeli i da odrede i njihovu talasnu dužinu. Prema dosadašnjim merenjima utvrđeno je da su talasne dužine gama-čestica između 0,000466 nm i 0,0428 nm. Prema tome, gama-čestice odgovaraju kratkotalasnom rendgenskom zračenju, ali za razliku od rendgenskog zračenja nastaju u atomskom jezgru.
Teorija radioaktivnog raspadanja[uredi | uredi izvor]
U to vreme se nije moglo objasniti odakle potiče tako velika energija kojom zrače radioaktivne materije. Na osnovu činjenice da se atomi radioaktivnih materija zaista raspadaju i prelaze u atome drugih elemenata manje težine, tj. da se transmutiraju, Raderford i Frederik Sodi postavili su 1903. teoriju radioaktivnog raspadanja. Prema njoj atomi radioaktivnih elemenata nisu stabilni, nego se spontano raspadaju (dezintegriraju ili transmutiraju), uz zračenje radioaktivnih čestica (alfa-čestica, beta-čestica ili gama-čestica), pri čemu prelaze u atome drugih elemenata.
Nuklearna reakcija[uredi | uredi izvor]
Teorija radioaktivnog raspadanja je vrlo značajna, jer iz nje proizlazi da su atomi deljivi i da mogu prelaziti u atome drugih hemijskih elemenata. Pošto je prelaženje jednog hemijskog elementa moguće samo ako se promena događa u atomskom jezgru, može se zaključiti da je radioaktivnost u stvari raspadanje jezgra atoma nekih hemijskih elemenata. Promena stanja atomskog jezgra kod radioaktivnih elemenata se naziva nuklearna reakcija.[9]
Prema zakonu pomicanja atomi radioaktivnih elemenata koji emitiraju alfa-čestice prelaze u atome čija je atomska masa manja za 4 atomske jedinice, a atomski broj manji za 2, tj. prelaze u atome elemenata koji u periodnom sistemu zauzimaju položaj pomeren za dva mesta ulevo, a atomi koji emituju beta-čestice prelaze u atome koji uz istu atomsku masu povećavaju svoj atomski broj za 1, tj. prelaze u atome elemenata koji u periodnom sistemu zauzimaju položaj pomeren za jedno mesto udesno.
Vreme poluraspada[uredi | uredi izvor]
Godine 1904. je Raderford uvideo da vreme, u toku kojeg se raspadne polovina početne količine nekog radioaktivnog elementa, može poslužiti kao podatak o brzini njegovog raspadanja, pa je zato veličinu tog vremena uveo kao svojstvenu konstantu, koja se naziva vreme poluraspada.[10]
Scintilacija[uredi | uredi izvor]
Godine 1899. Bekerel je zapazio još jedno svojstvo radioaktivnog zračenja i to da izazivaju luminiscenciju kod mnogih hemijskih materija, kao što su na primer cinkov sulfid (ZnS), barijumov platinocijanid (Ba[Pt(CN)4]x4 H2O) i dijamant. Zapaženo je pomoću mikroskopa da se luminiscentno svetlucanje cinkovog sulfida, izazvano alfa-česticama, sastoji iz velikog broja pojedinačnih bljeskova svetlosti. Zato što ovo kratkotrajno svetlucanje ima sličan izgled svetlucanju iskri, nazvano je scintilacija (lat. scintilla znači iskra). Pošto svaka alfa-čestica svojim udarom o luminiscentni zastor izaziva jednu scintilaciju ili iskru, Raderford je predložio da je to vrlo pogodan način za brojanje radioaktivnih čestica. Na taj način je scintilacija poslužila kao prvi način za istraživanje količine alfa-čestica.
Raderford je nastavio eksperimente, te je koristio zatvorenu posudu (koja se mogla puniti različitim gasovima) s pokretnim izvorom alfa čestica koji se mogao staviti na različite udaljenosti od zastora. Na zastoru su se uz pomoć mikroskopa motrile scintilacije - udarci čestica u zastor koji su izazivali svetlucanje. Kad je u posudu stavio kiseonik broj scintilacija se smanjio zbog apsorpcije alfa čestica u sloju gasa. Kad je u uređaj stavio suvi vazduh javio se efekt suprotan očekivanom – broj scintilacija se povećao. Zatim je posudu napunio čistim azotom i broj scintilacija bio je još i veći. Na osnovu mnogobrojnih eksperimenata zaključio je da čestice koje su prodornije, prelaze veći put i izazivaju scintilacije nastaju zbog sudara alfa čestica s atomima azota, te da su te nove čestice atomi vodonika.
Eksperiment s alfa-česticama i zlatnim listićem[uredi | uredi izvor]
Eksperiment s alfa-česticama i zlatnim listićem je bio jedan od najznačajnijih eksperimenata u nuklearnoj fizici, jer je to bio prvi dokaz da u atomu postoji atomsko jezgro. Raderford okuplja plodan tim istraživača, među kojima su Hans Gajger, Ernest Marsden, Džordž Hevesi, Henri Mozli, a nekoliko je godina član tima bio i Nils Bor.
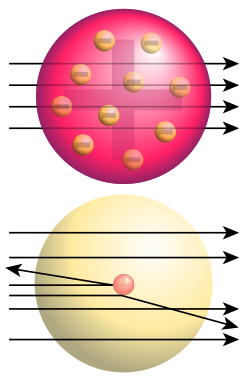
Ključni se eksperiment za to otkriće dogodio 1909. kada su naučnici vrlo tanku zlatnu foliju izložili delovanju alfa-čestica. Tompsonov model atoma je predviđao će alfa-čestice proći kroz tanki metalni film i raspršiti se pod određenim malim uglovima. Međutim, na veliko je iznenađenje istraživačkoga tima ustanovljeno raspršenje i pod velikim uglovima, a neka su se helijumska jezgra od metalne folije odbila potpuno unazad. Raderford je to uporedio s verovatnoćom da list papira odbije topovsku kuglu. Rezultat je eksperimenta vodio prema novom modelu atoma, koji je Raderford predložio 1911.: atom se sastoji od središnjeg naboja okruženoga sferičnom raspodelom naboja suprotnoga predznaka. U početku se pretpostavljalo da su i elektroni gradivne čestice atomskog jezgra, pa je u modelu za atom azot rednog broja 7 bilo pretpostavljeno da u jezgru ima 21 česticu, i to 14 protona i 7 elektrona, a u elektronskom omotaču još 7 elektrona. Otkriće je spina i spektroskopija azotnih jezgara, do čega je 1930. došao italijanski fizičar Franko Raseti, pokazalo da se azotna jezgra ponašaju kao čestice celobrojnog spina, tj. kao bozoni. To je bilo u potpunom neskladu s predloženim modelom azotnog jezgra sa 21 nukleonom, pa je to neslaganje nazvano „azotnom katastrofom“. Međutim, „katastrofa“ je razrešena otkrićem neutrona, koje je 1932. objavio Džejms Čedvik i njegovog spina 1/2. Ruski je fizičar Dmitri Ivanenko predložio današnji model atoma prema kojem su atomski nukleoni protoni i neutroni, a ne elektroni. Naziv proton za pozitivno naelektrisani nukleon prvi je upotrebio Raderford, a on je 1919. godine izveo i prvo pretvaranje (transmutaciju) jednoga elementa u drugi; toj je prvoj nuklearnoj reakciji u istoriji bombardovao azot alfa-česticama i tako dobio kiseonik.
Raderfordovo raspršenje[uredi | uredi izvor]
Raderfordovo raspršenje je pojava iz nuklearne fizike, kojom se objašnjava skretanja alfa-čestica koje udaraju u tanke listiće metala, a s njim se dokazuje postojanje pozitivno naelektrisanog atomskog jezgra, koje ima gotovo svu masu atoma.Rutherford, Ernest (1911). The scattering of alpha and beta particles by matter and the structure of the atom. Taylor & Francis. str. 688.</ref> Raderfordovo raspršenje je objašnjenje strukture atomsko jezgra, koje je nastalo nakon eksperimenta s alfa-česticama i zlatnim listićem, koji su izveli Ernest Raderford, Hans Gajger i Ernest Marsden. Rezultati tog eksperimenta su pokazali da su skretanja alfa-čestica pod velikim uglovima bila jako retka, na primer pri prolazu kroz listić platine na svakih 8000 jedna alfa-čestica bi skrenula pod uglom većim od 90º.
Raderfordov model atoma[uredi | uredi izvor]
Činjenica koju je utvrdio Raderford, da je alfa-čestica u stvari jon atoma helijuma, da je njena masa 4 puta veća od mase atoma vodonika i da njen električni naboj iznosi dva elementarna električna naboja, omogućila je određivanje električnog naboja svakog atoma.[11] Osim toga, Raderford je zapazio još jednu važnu pojavu, da se alfa-čestice raspršuju pri prolazu kroz neki materijal, na osnovu koje je zasnovao Raderfordov model atoma. On je zapazio da se uski snop alfa-čestica, nakon prolaza kroz tanki listić (foliju) metala, skreće od polaznog snopa i da se rasprši. Zapazio je i da se alfa-čestice više rasprše kod prolaza kroz metal, nego kod prolaza kroz vazduh.
Prvo nuklearno pretvaranje[uredi | uredi izvor]
Godine 1919. Raderford je bombardujući azot alfa-česticama izveo prvo pretvaranje (transmutaciju) jednog elementa u drugi. Raderford je prilikom istraživanja raspršenja alfa-čestica kroz vazduh, otkrio da prilikom bombardovanja atoma azota s alfa-česticama nastaju nova jezgra atoma kiseonika i vodonika.
Neutron[uredi | uredi izvor]
Godine 1921. Raderford je radio s Nilsom Borom i pretpostavio je postojanje neutrona, kojeg je 1932. dokazao njegov kolega Džejms Čedvik i 1935. dobio Nobelovu nagradu za fiziku za to otkriće.
Publikacije[uredi | uredi izvor]
- Radio-activity , (1905). (2nd изд.). 1904. ISBN 978-1-60355-058-1.
- Radioactive Transformations . 1906. ISBN 978-1-60355-054-3.
- Radioactive Substances and their Radiations (1913)[12]
- The Electrical Structure of Matter (1926)
- The Artificial Transmutation of the Elements (1933)
- The Newer Alchemy (1937)
Članci[uredi | uredi izvor]
- "Disintegration of the Radioactive Elements" Harper's Monthly Magazine, January 1904, pages 279 to 284.
Vidi još[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ „Ernest Rutherford – Biography”. NobelPrize.org. Arhivirano iz originala 17. 12. 2012. g. Pristupljeno 21. 02. 2013.
- ^ Eve, A. S.; Chadwick, J. (1938). „Lord Rutherford 1871–1937”. Obituary Notices of Fellows of the Royal Society. 2 (6): 394. doi:10.1098/rsbm.1938.0025.
- ^ „Ernest Rutherford, Baron Rutherford of Nelson”. Encyclopædia Britannica.
- ^ „The Discovery of Radioactivity”. lbl.gov. 09. 08. 2000. Arhivirano iz originala 15. 06. 2020. g. Pristupljeno 31. 07. 2017.
- ^ „Od rude do žutog kolača“ Arhivirano na sajtu Wayback Machine (31. jul 2017), Nuklearna elektrana Krško, 2011.
- ^ [1] Arhivirano na sajtu Wayback Machine (1. januar 2012) "Povijest fizike", Ivan Supek, 2011.
- ^ Campbell, John. „Rutherford – A Brief Biography”. Rutherford.org.nz. Pristupljeno 04. 03. 2013.
- ^ Rutherford, E.; Royds, T. (1908). „XXIV.Spectrum of the radium emanation”. Philosophical Magazine Series 6. 16 (92): 313. doi:10.1080/14786440808636511.
- ^ "Uvod u nuklearnu energetiku"[mrtva veza], Prof. dr. sc. Danilo Feretić, 2011.
- ^ "Fizika NEK-a - Fisija" Arhivirano na sajtu Wayback Machine (5. februar 2017), Nuklearna elektrana Krško, e-škola, 2011.
- ^ Longair, M. S. (2003). Theoretical concepts in physics: an alternative view of theoretical reasoning in physics. Cambridge University Press. str. 377—378. ISBN 978-0-521-52878-8.
- ^ Carmichael, R. D. (1916). „Review" Radioactive Substances and their Radiations, by E. Rutherford” (PDF). Bull. Amer. Math. Soc. 22 (4): 200. doi:10.1090/s0002-9904-1916-02762-5.
Literatura[uredi | uredi izvor]
- Longair, M. S. (2003). Theoretical concepts in physics: an alternative view of theoretical reasoning in physics. Cambridge University Press. str. 377—378. ISBN 978-0-521-52878-8.
- Badash, Lawrence (2008) [2004]. „Rutherford, Ernest”. Oxford Dictionary of National Biography (online izd.). Oxford University Press. doi:10.1093/ref:odnb/35891. (Subscription or UK public library membership required.)
- Cragg, R. H. (1971). „Lord ernest rutherford of nelson (1871?1937)”. Royal Institute of Chemistry, Reviews. 4 (2): 129—120. doi:10.1039/RR9710400129.
- Campbell, J. (1999) Rutherford: Scientist Supreme, AAS Publications, Christchurch
- Marsden, E. (1954). „The Rutherford Memorial Lecture, 1954. Rutherford-His Life and Work, 1871–1937”. Proceedings of the Royal Society A. 226 (1166): 283—226. Bibcode:1954RSPSA.226..283M. doi:10.1098/rspa.1954.0254.
- Reeves, Richard (2008). A Force of Nature: The Frontier Genius of Ernest Rutherford. New York: W. W. Norton. ISBN 978-0-393-33369-5.
- Rhodes, Richard (1986). The Making of the Atomic Bomb. New York: Simon & Schuster. ISBN 978-0-671-44133-3.
- Wilson, David (1983). Rutherford. Simple Genius. Hodder & Stoughton. ISBN 978-0-340-23805-9.
Spoljašnje veze[uredi | uredi izvor]
- Biography and web exhibit Архивирано на сајту Wayback Machine (30. јул 2016)
- Biography
- Nobel Lecture
- "Radioactive change", Rutherford & Soddy article (1903), online and analyzed on Bibnum.
- The Rutherford Museum
- Rutherford Scientist Supreme
- Profile from American Public Broadcasting Service
- Profile from The New Zealand Edge
- Annotated bibliography for Ernest Rutherford from the Alsos Digital Library for Nuclear Issues
- Biography
- Rutherford at Canterbury University College
- Rutherford's Timebomb Архивирано на сајту Wayback Machine (30. септембар 2007)
- BBC Radio 4: In Our Time – Rutherford
- The Rutherford Collection at his alma mater the University of Canterbury[мртва веза]
- Ernest Rutherford NZ Post stamp, 2008
- Kennedy, Bruce. „Rutherford Gold Foil Experiment”. Backstage Science. Brady Haran.

