Хемија


Хемија је природна и експериментална наука. Бави се проучавањем грађе, особина и промена супстанци као и закона по којима се те промене дешавају. Класично се издваја четири поља у хемији, мада постоји далеко већи број уско специјализованих грана хемије и то: општа хемија, неорганска хемија, органска хемија и биохемија. Хемија је једна од елементарних наука, поред математике блиска је и: физици, биологији, фармацији, медицини. У многим пословима као и у свакодневном животу заступљена је хемија.
Хемија заузима централно место међу природним наукама. Између осталог, бави се и молекулима, њиховом структуром, особинама и трансформацијама, и принципима на којима се особине молекула заснивају. Због ове своје свеобухватности, хемија има доста заједничких тема са другим природним наукама, као што су физика, геологија и астрономија, с једне стране, и биологија, физиологија и медицина, с друге.
Историја хемије[уреди | уреди извор]
Настанак хемије се може пратити до опажања феномена горења који је довео до појаве металургије - вештине и науке о добијању метала из руда. Међутим, због недостатка научног објашњења, ватра је остала само мистична сила која је могла трансформисати супстанцу из једног облика у други (спаљивање дрвета, кључање воде), док истовремено производи топлоту и светлост. Филозофски напори да се разуме зашто различите супстанце имају различите особине (боју, густину, мирис), постоје у различитим агрегатним стањима (гасовита, течна и чврста тела) и реагују на другачије начине када су изложене неким утицајима, попут воде, ватре или промени температуре, довели су до постављања првих теорија о природи и хемији. Једна од првих теорија је била да су вода, ватра, земља и ваздух четири главна елемента.
Грчки атомисти Демокрит и Леукип су тврдили да постоје атоми (άτομος) као најмање и недељиве честице.[1] Међутим, због недостатка научних доказа, постојање атома је било лако порећи, па се теорија о четири елемента дуго задржала, јер ју је заступао Аристотел (који је додао и пети елемент етар, као божанску силу), а Црква је касније прихватила овакво учење.
Жеља за златом је довела до процеса његове пурификације, иако тада основни принципи нису били познати - мислило се да је то пре трансформација, а не пурификација. Многи учени људи из тог периода су сматрали да је разумљиво веровати да постоји начин за претварање јефтинијих метала у злато. Ово је довело до појаве алхемије и потраге за Каменом мудрости, за који се сматрало да врши такву трансформацију обичним додиром.[2]

Неки сматрају средњовековне муслимане за прве хемичаре, који су увели прецизно посматрање и експериментисање, и који су окрили бројне супстанце. Најутицајни муслимански хемичари били су Гебер, ал-Кинди, ал-Рази и Абу Рајхан ал-Бируни. Геберови радови су постали познати у Европи кроз латинске преводе псеудо-Гебера из 14. века, који је такође написао неколико својих књига под именом Гебер. Допринос индијских алхемичара и металурга је такође значајан.[3]
Појава хемије у Европи је била првенствено због сталних појава куге и болести биљака током раног средњег века. Ово је довело до потребе за лековима. Веровало се да постоји универзални лек назван Еликсир живота, али као ни Камен мудрости, ни он никада није пронађен.
Парацелзус (1493—1541) је одбацио теорију о 4 елемента (вода, ватра, ваздух и земља) и, уз врло мало знање о својим хемикалијама и медицини, створио је хибрид алхемије и науке, што ће временом добити име јатрохемија. Такође, утицај филозофа као што су Френсис Бекон (1561—1626) и Рене Декарт (1596—1650), који су тражили више тачности у математици и другим наукама и у уклањању предрасуда из научних опсервација, довело је научне револуције, која је у хемији почела са Робертом Бојлом (1627—1691), који је добио једначину познату као Бојлов закон о особинама гасовитих тела.[4] Модерна хемија је настала када ја Лавоазјеовим (1743—1794) открићем Закона о одржању маса (1783), Прустовим открићем Закона сталних односа маса (1799) и модерном атомском теоријом Џона Далтона (око 1800). Закон о одржању маса и теорија сагоревања су реформулисали хемију. Лавоазјеови фундаментални доприноси хемији су били резултат свесних напора да резултати добијени експериментима прилагоде у једну теорију. Лавоазје је објаснио да је сагоревање у ствари реакција са кисеоником и тиме оповргнуо флогистонску теорију и развио је нови систем хемијске номенклатуре. Такође је превео архаични и технички језик хемије у нешто што су могле да разумеју необразоване масе, што је повећало интересовање јавности за хемијом. Због свих тих доприноса, Антоан Лавоазје се сматра оцем модерне хемије. Касније откриће Фридриха Велера да се многе супстанце које се налазе у природи могу добити у лабораторији је помогло даљем развоју хемије.
Откриће хемијских елемената је имало дугу историју још од времена алхемије, а кулминирало се стварањем периодног система елемената који је начинио Дмитриј Мендељејев и каснијим открићем неких синтетичких елемената.
Открића у хемији су изванредно допринела развоју модерне цивилизације. Један од најважнијих проналазака 20. века је вештачка фиксација азота (синтеза амонијака: Нобелова награда за хемију 1918, Фриц Хабер и 1931, Карл Бош) из које је израсла модерна индустрија вештачких ђубрива. Процењује се да исхрана 40% светске популације зависи од вештачких ђубрива на бази синтезе амонијака. (Nature 427, 498-499 (05 Feb 2004)) Друга важна открића везана су за молекулске основе живота где је хемија успела да продре дубоко у молекулске механизме биохемијских процеса и трансфера генетичких информација у живим системима.
Подела[уреди | уреди извор]
Аналитичка хемија[уреди | уреди извор]

Аналитичка хемија је наука која се бави проучавањем хемијских и физичких процеса на основу којих се може одредити квалитативни и квантитативни састав испитиване супстанце. Због тога се ова наука дели на две области: квалитативну и квантитативну анализу. Квалитативна анализа по правилу претходи квантитативној и њоме се утврђује из којих се елемената, јона, атомских (функционалних) група и молекула састоји испитивана супстанца. Квантитативна анализа се заснива на утврђивању или количина испитиваних супстанци или односа у коме се дате супстанце налазе. Методе којима се при томе аналитичка хемија користи се могу поделити на хемијске, физичке и физичко-хемијске.
Неорганска хемија[уреди | уреди извор]
Хемија је заправо наука која проучава састав и особине супстанци, као и појаве које се дешавају када супстанце реагују једна са другом. Неорганска хемија представља велики део хемије јер она проучава хемијска својства и реакције свих хемијских елемената и њихових једињења као и хемијске процесе који се збивају међу њима. Изузетак чине једињења (четворовалентног) угљеника које изучава органска хемија.
Органска хемија[уреди | уреди извор]
Органска хемија је, најопштије постављено, хемијска дисциплина која се бави проучавањем угљеника и његових једињења.[5] Нешто конкретније, то је наука која проучава својства, структуру и реактивност органских једињења, као и начине на који се та сазнања могу применити у синтези жељених једињења. И поред сугестивног назива, спектар структура којима се бави органска хемија нипошто није ограничен на супстанце пореклом из живог света; напротив, органска синтеза бави се добијањем нових органских једињења из најразличитијих прекурсора. Ипак, за сва једињења којима се бави органска хемија заједничко је да садрже четворовалентни угљеник.
Почетком 19. века из биљака су изоловане органске супстанце које су по својим особинама биле потпуно другачије од свих до тада познатих једињења. Доктрина витализма, коју је заступао велики број хемичара тадашњице, тврдила је да је особеност свих таквих једињења присуство „животне силе“ (лат. vis vitalis), без чијег учешћа је уједно и немогуће синтетисати органску материју. Овакав ригидан став по којем синтеза органских структура (које су тада сматране посебно сложенима) може да се одигра само у живим организмима, а никако у реакционој смеши, ефективно је закочио даљи развој органске хемије. 1828. године, међутим, немачки хемичар Фридрих Велер је сасвим случајно, у покушају да добије амонијум-цијанат из цијанатне киселине и амонијака, добио супстанцу коју је успешно идентификовао као уреју. Уреја је данас позната као значајан финални продукт метаболизма сисара, али је и у Велерово време била класификована као органско једињење, јер је раније била изолована из урина. Велеровом синтезом срушен је постулат да је немогуће добити органско једињење из неорганских прекурсора. Ово откриће представљало је прекретницу у развитку органске хемије које је довело до њене велике експанзије.
Током протекла два века научна основа органске хемије знатно је проширена, захваљујући и развоју других хемијских дисциплина. Има велике импликације у бројним другим пољима науке и привреде — петрохемији, фармацији, индустрији пластичних маса, прехрамбеној индустрији, индустрији боја и лакова...
Главни акценат у органској хемији данас је на органској и хиралној синтези, затим зеленој хемији, микроталасној хемији и хемији фулерена.
Физичка хемија[уреди | уреди извор]
Физичка хемија је настала комбиновањем знања из физике, хемије, термодинамике и квантне механике да би се опажене макроскопске појаве описале на атомском и молекулском нивоу, дакле, физичка хемија се бави везом између микроскопских и макроскопских особина материје. На пример, величина молекула у течности може да се одреди на основу мерења њеног индекса преламања и густине, или на основу топлотног капацитета и површинског напона.
Биохемија[уреди | уреди извор]

Биохемија је мост између биологије и хемије који проучава како комплексне хемијске реакције стварају живот. Биохемија је хибридни део хемије који конкретно проучава хемијске процесе у живим организмима. Овај чланак дискутује само копнену биохемију, која почива на угљенику и води. Како сви облици живота које данас имамо на планети имају заједничко порекло, према томе имају и сличне биохемије, као што су генетички код и стереохемија многих биомолекула. Непознато је да ли су наизменичне биохемије уопште и могуће.
Биохемија проучава структуру и функцију целуларних компоненти, као што су протеини, угљени хидрати, липиди, нуклеинске киселине и остали биомолекули. Иако постоји огроман број различитих биомолекула, они се често састоје од истих јединица које се понављају мономера, али који се понављају у различитим секвенцама. Недавно, биохемија је почела да се фокусира на проучавање реакција у којима су катализатори ензими, и на проучавање особина протеина.
Биохемија метаболизма ћелије и биохемија ендокриног система су два домена која су интензивно студирана. Друге области које спадају под појам биохемије су генетички код (ДНК, РНК), синтеза протеина, транспорт кроз ћелијску мембрану и трансдукција сигнала.
Теоријска хемија[уреди | уреди извор]
Теоријска хемија је подобласт хемије која користи знања из физике да се објасне или предвиде хемијски феномени. У претходним годинама чинила ју је само квантна хемија, тј. примена квантне механике да би се решили проблеми у хемији. Груба потподела теоријске хемије су електронске структуре, динамика и статистичка механика. У процесу решавања проблема, све три подгране могу бити укључене у различитом степену. Од краја Другог светског рата, развој рачунара је омогућио систематски развој рачунске хемије, вештине развијања и примене рачунарских програма за решавање хемијских проблема. Теоријска хемија се у великој мери преклапа са (теоријском или експерименталном) физиком кондензоване материје и молекуларном физиком.
Основни појмови[уреди | уреди извор]
Атом[уреди | уреди извор]

Атом (грчки άτομον (атомон) - недељив) је најмањи делић супстанце, тј. хемијског елемента који испољава све особине тог хемијског елемента. Атом се састоји из језгра и електронског омотача.
Језгро чине:
- Протони, са позитивним наелектрисањем и јединичном масом и
- Неутрони, који имају јединичну масу али нису наелектрисани.
Омотач чине:
- Електрони, који имају негативно наелектрисање и занемарљиво малу масу.
Хемијске особине атома одређује број протона у њему (редни број) и тај број је јединствен за сваки елемент, а масу број протона и број неутрона. Атом као целина је неутралан јер садржи исти број електрона и протона. Атом постаје наелектрисан тако што прими или отпусти један или више електрона и постаје јон.
Хемијске особине атома не зависе од броја неутрона, па постоје атоми истог елемента са различитим бројем неутрона - изотопи.
Молекул[уреди | уреди извор]

Молекул је најмања јединица хемијског једињења која задржава хемијски састав и својства. Молекул се састоји из више атома, истог хемијског елемента као код кисеоника, (O2), или из различитих елемената као код воде (H2O).
Молекули су сувише мали да би се видели голим оком. Димензија су од 0,1 до 100 нанометара (0,0000000001 до 0,0000001 метара) мада има и изузетака. Рецимо макромолекул ДНК кад би се извадио из једра ћелије и размотао достигао би дужину једног до два метра.[6]Међутим и тада би био невидљив јер би његово 'влакно' било пречника свега 0,000000005 m. Зато се за одређивање величине и облика молекула користе посебне методе физичке хемије а нарочито инструменталне методе.
Однос елемената који граде једињење, изражава се емпиријском формулом. На пример, воду граде водоник и кисеоник у односу 2:1, H2O, а етил алкохол, (етанол) угљеник, водоник и кисеоник у односу 2:6:1, C2H6O. Овај однос не мора увек да одређује јединствени молекул - диметил етар има исти однос као етанол, на пример. Молекули који се састоје од истих атома, али у различитом распореду се зову изомери.
Хемијска или молекулска формула одређује тачније редослед атома који граде молекул, па је формула етанола CH3CH2OH а диметилетра CH3OCH3. За представљање сложенијих молекула где атоми могу бити различито распоређени у простору користе се структурне формуле. Молекулска маса је збир маса атома који чине молекул, и попут атомске, изражава се у атомским јединицама масе (атомска јединица масе = 1/12 масе изотопа 12C). Дуго се мислило да су дужине хемијски веза и њихови углови у молекулу константни. Међутим, модерним структурним методама нађено је да се геометрија хемијске везе незнатно мења, нарочито код сложенијих молекула.
Мол[уреди | уреди извор]
Мол (симбол: mol) је једна од седам СИ основних јединица која мери количину супстанце система. Један мол је количина супстанце која садржи толико честица колико има атома у тачно 0,012 килограма угљеника изотопа C12. Ова количина је позната као Авогадров број и приближно износи 6,0221415 × 10²³.
Због везе јединице атомске масе са Авогадровим бројем, практични начин исказивања овога за атоме или молекуле је: Количина супстанце која садржи исти број грама као и број атомске масе супстанце. Пошто гвожђе, на пример, има атомску масу од 55,845, у једном молу гвожђа има 55,845 грама (0,055845 килограма).
Када се мол користи да би се одредила количина супстанце, потребно је навести и о којој врсти честица се ради, јер то могу бити атоми, молекули, јони... На пример, 18 грама воде садржи 1 мол молекула, 2 мола атома водоника, 1 мол атома кисеоника или укупно 3 мола атома.
Елемент[уреди | уреди извор]
Хемијски елемент се карактерише одређеним бројем протона у језгру његових атома. Овај број се назива атомски број елемента. На пример, сви атоми са 6 протона у свом језгру су атоми хемијског елемента угљеника, а сви атоми са 92 протона су атоми уранијума. Изотопи неког хемијског елемента могу имати различити број неутрона у свом језгру, док им је број протона исти. На пример, обичан водоник има само један протон у језгру, а његови изотопи деутеријум и трицијум имају по један протон и по један, односно два неутрона у свом језгру.
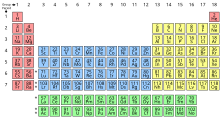
Најпогоднији начин за приказ хемијских елемената је периодни систем елемената, у ком су елементи груписани по својим атомским бројевима. Захваљујући њеном уређењу, групе (вертикалне колоне) и периоде (хоризонтални редови) елемената у табели деле заједничке хемијске особине, или прате одређен тренд у карактеристикама као што су атомски радијус, електронегативност, итд.
Једињење[уреди | уреди извор]
Хемијско једињење је чиста супстанца која се састоји из два или више елемената. Атоми који сачињавају једињење су међусобно везани хемијским везама и чине молекул (или кристалну решетку). Састав хемијских једињења је сталан без обзира на начин њиховог постанка (то значи да је однос атома који су повезани хемијским везама увек исти). Традиционално се хемијска једињења деле на органска и неорганска. Осим ових, постоје и разне потподеле (на киселине, базе, соли, оксиде итд.)
Смеша[уреди | уреди извор]

Смеше су скупови две или више различитих супстанци, за разлику од чистих (простих) супстанци које сачињава само један елемент или једно једињење. Особине смеша су адитивне, односно, она задржава особине свих супстанци које је чине. Тако ће смеша гвожђа и сумпора имати особине и једног и другог елемента (гвожђе ће и даље имати магнетна својства, а сумпор жуту боју). Смеше можемо поделити на хомогене и хетерогене. Оне су обично хетерогене, што значи да се јасно могу уочити разлике између супстанци које их чине. Међутим, дешава се да су састојци неке смеше довољно мали да се не могу видети голим оком, па такве смеше изгледају хомогено. Такав је случај са крвљу. Под микроскопом се види да крв сачињава безбојна течност са суспендованим честицама. Хомогена је она супстанца код које један део има потпуно исти састав и особине као сваки други део. Примери за праве хомогене смеше (јер се хетерогеност не може доказати) су неки водени раствори (шећера, соли итд.). Ослобађање топлоте, зрачења светлости или стварање струје су појаве које обично прате неку хемијску реакцију. Уколико не дође до ових појава приликом мешања супстанци, претпоставља се да се није десила хемијска реакција, већ да се направила смеша. Састојци у смеши се раздвајају коришћењем физичких промена супстанци. При томе се могу користити различита физичка својства, као што су магнетизам, специфична тежина, (не)растворљивост у одговарајућим растварачима, тачка мржњења, као и методе: дестилација, ликвација, дифузија, елутрација, флотација.
Супстанца[уреди | уреди извор]
Супстанца је облик постојања материје који је доступан људским чулима. Карактерише је маса мировања. Састоји се од веома ситних честица - атома. Данас је познато више од 40 милиона различитих супстанци, од којих су неке супстанце пронађене у природи, док се друге производе вештачким путем.[7]Без обзира на који од та два начина пронађене, велики број њих, око 100 хиљада има практичну примену.[8]
Свака супстанца има карактеристична својства по којима се мање-више разликује од других супстанци, на пример: боју, мирис, густину, температуру топљења, температуру кључања. Наведена и слична својства супстанци, која се одређују помоћу наших чула или инструмената, називају се физичка својства. Хемијска својства супстанци испољавају се при њиховим реакцијама са другим супстанцама.
Хемијске везе[уреди | уреди извор]
Хемијска веза је привлачна сила између два атома настала интеракцијом њихових периферних (валентних) електрона. Сила је много јача од енергије топлотног кретања тако да су атоми трајно везани образујући стабилну групу - молекул. Електрони су истог наелектрисања па би требало да се одбијају, међутим, у електронским орбиталама спаривање њихових спинова стабилизује електронске парове и укупан ефекат је образовање стабилне везе. Два основна типа хемијске везе су јонска и ковалентна, али се у природи срећу и 'мешане' везе, односно оне које имају делимично јонски и делимично ковалентни карактер. У прилог томе иде и то што ковалентна веза може бити поларна и неполарна. Посебан тип везе је метална веза која се ствара између атома метала.
Јони[уреди | уреди извор]

Јон је наелектрисана честица (атом или молекул) која примила или изгубила један или више електрона. Позитивно наелектрисани катјони (на пример натријумов катјон Na+) и негативно наелектрисани анјони (на пример хлоров анјон Cl−) могу да образују кристалну решетку неутралне соли (на пример натријум хлорид или кухињска со NaCl). Примери вишеатомских јона који се не распадају током киселинско-базних реакција су хидроксиди (OH−) и фосфати (PO43−).
Јонизовани гасови се често називају плазма.
Хемијска реакција[уреди | уреди извор]

Хемијске реакције представљају трајне промене у структури полазних супстанци (реактаната или реагујућих супстанци) и настајање нових супстанци (производа) које се по саставу и својствима разликују од полазних супстанци.
Хемијске реакције се грубо могу поделити на:
- Оксидо-редукционе реакције;
- Комплексне реакције;
- Хемијске реакције при којима долази до дисоцијације и асоцијације молекула, атома и јона.
Хемијске реакције одигравају се са променом супстанци и са одређеним топлотним ефектом, при чему се ослобађа енергија или троши (везује или отпушта). Уколико се приликом реакције троши или ослобађа топлота онда се говори о термохемијским реакцијама. Количина топлоте која се у току хемијске реакције ослобађа или везује назива се топлота реакције.
Хемијске реакције које се одигравају ослобађањем топлоте називају се егзотермне реакције. Хемијске реакције које се одигравају са везивањем топлоте називају се ендотермне реакције. Ако је хемијска реакција у једном смеру ендотермна у другом је егзотермна и обрнуто.
Енергија[уреди | уреди извор]
Неку хемијску реакцију увек прати повећање или губитак енергије супстанци које учествују у реакцији. Део енергије се размењује између околине и реактаната у облику топлоте или светлости, тако да продукти реакције могу имати више или мање енергије од реактаната. За реакцију се каже да је егзотермна ако је укупна количина енергије производа реакције нижа од почетне енергије реактаната, док је код ендотермних реакција ситуација обрнута.
Хемијске реакције нису могуће све док енергија реактаната не пређе енергетску баријеру која се назива енергија активације. Брзина хемијске реакције (на некој температури T) је повезана са енергијом активације E преко Болцмановог фактора - што је вероватноћа да молекул има енергију већу или једнаку E на датој температури T. Ова експоненцијална зависност брзине реакције од температуре назива се Аренијусова једначина. Енергија активације потребна за извођење хемијске реакције може бити у облику топлоте, светлости, електрицитета или механичке силе у облику ултразвука.[9]
Са овим је повезан концепт слободне енергије, која укључује и појам ентропије, а које је врло корисно средство за предвиђање изводљивости реакције и одређивања стања равнотеже хемијске реакције. Реакција је изводљива само ако је укупна промена Гибсове слободне енталпије негативна ; ако је једнака нули за хемијску реакцију се каже да је у равнотежи.
Постоје само ограничена могућа стања енергије електрона, атома и молекула. Она су одређена правилима квантне механике, која захтева квантовање енергије. За атоме/молекуле на вишем енергетском стању се каже да су побуђени. Ти атоми/молекули у побуђеном стању су често реактивнији, што је предуслов за хемијске реакције.
Агрегатно стање неке супстанце је увек одређено њеном енергијом и енергијом њене околине. Када су међумолекулске силе у супстанци такве да енергија окружења није довољна да их надјача, супстанца се налази у уређенијим стањима као што су течности и чврста тела, као што је случај са водом (H2O), која је течност на собној температури, јер су њени молекули повезани водоничним везама.[10] Са друге стране водоник сулфид (H2S) је гас на собној температури и нормалном притиску, јер су његови молекули повезани слабијом дипол-дипол интеракцијом.
Прелазак енергије са једне супстанце на другу зависи од величине енергетског кванта који емитују супстанце. Ипак, топлотна енергија се лако преноси са скоро сваке супстанце на другу јер су вибрациони и ротациони енергетски нивои супстанце смештени врло близу. Пошто електронски енергетски нивои нису близу један другог, ултраљубичасто електромагнетно зрачење се не преноси истом лакоћом, а слично је и са електричном енергијом.
Постојање карактеристичних линија енергетских прелаза различитих супстанци је корисно за њихову идентификацију анализом спектралних линија различитих врста спектара, која се често користи у хемијској спектроскопији, као на пример у инфрацрвеној или микроталасној спектроскопији, нуклеарној магнетној резонанцији, резонанцији електронског спина, итд. Ово се користи за идентификацију састава удаљених објеката, као што су звезде или удаљене галаксије, анализом њеног спектра.
Термин хемијска енергија се често користи да се наговести потенцијал супстанце да изврши трансформацију путем хемијске реакције односно способност да преобрази друге супстанце.
Види још[уреди | уреди извор]
- Нобелова награда за хемију
- Српски хемичари
- Периодни систем елемената
- Балансирање хемијских једначина
- Алхемија
Референце[уреди | уреди извор]
- ^ Логос 2017, стр. 219-220.
- ^ Alchemy Timeline Архивирано на сајту Wayback Machine (30. август 2008) - Chemical Heritage Society
- ^ Will Durant (1935): Our Oriental Heritage: Simon & Schuster
- ^ BBC - History - Robert Boyle (1627 - 1691), Приступљено 29. 4. 2013.
- ^ K. Peter C. Vollhardt, Neil E. Schore: Органска хемија — структура и функција, 4. издање, Дата Статус, Београд, 2004.
- ^ Length of a Human DNA Molecule, Приступљено 29. 4. 2013.
- ^ PubChem, Приступљено 29. 4. 2013.
- ^ „Emerald | Management of Environmental Quality: An International Journal | A Swedish overview of selecting hazardous substances as pollution indicators in wastewater”. Emeraldinsight.com. doi:10.1108/14777830410523116. Приступљено 24. 6. 2010.[мртва веза]
- ^ Reilly, Michael. (2007).
- Mechanical force induces chemical reaction, NewScientist.com news service, Reilly
- ^ Changing States of Matter - Chemforkids.com
Литература[уреди | уреди извор]
- Паркес. Г. Д. & Фил, Д. 1973. Мелорова модерна неорганска хемија. Научна књига. Београд.
- Рондовић, Д. 1991. Квалитативна хемијска анализа. Научна књига: Београд.
- Morris Hein, Susan Arena: Foundations of College Chemistry, 10th ed, Brooks/Cole Publishing Company, 2000.
- Логос, Александар А. (2017). Путовање мисли : увод у потрагу за истином. Београд.


