Електронска љуска
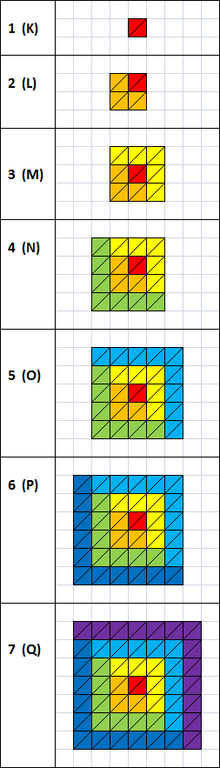
У хемији и атомској физици, електронска љуска, или главни енергетски ниво, може се сматрати орбитом коју прате електрони око језгра атома. Љуска најближа језгру назива се „1 љуска” (она се такође зове „K љуска”), а затим следи „2 љуска” (или „L љуска”), затим „3 љуска” (или „M љуска”) и тако даље и даље од језгра. Љуске одговарају главним квантним бројевима (n = 1, 2, 3, 4 ...) или су абецедно означене словима која се користе у рендгенској нотацији (K, L, M, ...).
Свака љуска може да садржи само фиксни број електрона. Прва љуска може да садржи до два електрона, друга љуска може да садржи до осам (2 + 6) електрона, трећа љуска може да држи до 18 (2 + 6 + 10 ) и тако даље. Општа формула је да n-та љуска може у принципу да садржи до 2(n2) електрона.[1] Будући се електроне привлачи језгро, електрони атома ће генерално заузимати спољашње љуске само ако су унутрашње љуске већ потпуно попунили други електрони. Међутим, то није строг захтев: атоми могу да имају две или чак три непотпуне спољашње љуске. (За више детаља погледајте Маделунгово правило).[2]
Електрони у најудаљенијој заузетој љусци (или љускама) одређују хемијска својства атома; она се назива валентна љуска. Свака љуска се састоји од једне или више подљуски, и свака подљуска се састоји од једне или више атомских орбитала.
Историја[уреди | уреди извор]
Терминологија љуске потиче из Арнолд Зомерфелдове модификације Боровог модела. Зомерфелд је задржао Боров планетарни модел, али је додао благо елиптичне орбите (окарактерисане додатним квантним бројевима ℓ и m) да би објаснио фину спектроскопску структуру неких елемената.[3] Вишеструки електрони са истим главним квантним бројем (n) имали су блиске орбите које су формирале „љуску” позитивне дебљине уместо бесконачно танке кружне орбите Боровог модела.
Постојање електронских љуски прво је експериментално примећено у студијама апсорпције рендгенских зрака Чарлса Баркла и Хенрија Мозлија. Баркл их је означио словима К, L, M, Н, О, П и Q.[4] Порекло ове терминологије било је абецедно. Сумљало се да постоји и „Ј” серија, мада су каснији експерименти показали да К апсорпционе линије производе најдубљи електрони. Касније је утврђено да се ова слова одговарају н вредностима 1, 2, 3, итд. Она се користе се у спектроскопској Сигбановој нотацији.
Физички хемичар Гилберт Њутон Луис био је одговоран за већи део раног развоја теорије о учешћу електрона валентне љуске у хемијском везивању. Лајнус Полинг је касније генерализовао и проширио теорију примењујући увиде из квантне механике.
Љуске[уреди | уреди извор]
Електронске љуске су означене са К, L, M, Н, О, П и Q; или 1, 2, 3, 4, 5, 6 и 7; идучи од љуске најближе језгру ка спољашњости. Електрони у спољним љускама имају вишу просечну енергију и путују даље од језгра од оних у унутрашњим љуштурама. Ово их чини важнијим у одређивању како атоми хемијски реагују и како се понашају као проводници, јер привлачење језгра атома слабије делује на њих и лакше се превладава. Стога је реактивност датог елемента у великој мери зависна од његове електронске конфигурације.
Подљуске[уреди | уреди извор]
Свака љуска је састављена од једне или више потљуски, које су и саме састављене од атомских орбитала. На пример, прва (K) љуска има једну подљуску, звану 1с; друга (L) љуска има две потљуске, које се зову 2с и 2п; трећа љуска има 3с, 3п и 3д; четврта љуска има 4с, 4п, 4д и 4ф; пета љуска има 5с, 5п, 5д и 5ф, и теоретски може да држи више у 5г подљусци, која није попуњена у основном стању електронске конфигурације било ког познатог елемента.[2] Различите могуће подљуске су приказане у следећој табели:
| Ознака подљске | ℓ | Макс. електрона | Љуске које је садрже | Историјско име |
|---|---|---|---|---|
| с | 0 | 2 | Свака љуска | sharp |
| п | 1 | 6 | 2. љуска и више | principal |
| д | 2 | 10 | 3. љуска и више | diffuse |
| ф | 3 | 14 | 4. љуска и више | fundamental |
| г | 4 | 18 | 5. љуска и више (теоретски) | (следеће у алфабету након ф, изузимајући и)[5] |
- Прва колона је „ознака подљуске”, која се пише малим словима. На пример, „4с подљуска” је потљуска четврте (Н) љуске, са типом с описаним у првом реду.
- Друга колона је азимутни квантни број (ℓ) подљуске. Прецизна дефиниција укључује квантну механику, али то је број који карактерише потљуску.
- Трећа колона је максимални број електрона који могу да заузимају подљуску тог типа. На пример, горњи ред наводи да свака подљуска с-типа (1с, 2с, итд.) може да има највише два електрона у себи. Свака подљуска осим прве може да има 4 електрона више од претходне.
- Четврта колона наводи које љуске имају подљуску датог типа. На пример, гледајући горња два реда, свака љуска има с подљуску, док само друга љуска и више имају п подљуску (и.е., не постоји 1п подљуска).
- Крајња колона наводи историјско порекло ознака: с, п, д, и ф. Оне потичу од раних студија атомских спектралних линија. Остале етикете, наиме г, х и и, су абецедни наставак након последње историјски настале етикете ф.
Иако се обично каже да сви електрони у љусци имају исту енергију, ово је апроксимација. Међутим, електрони у једној подљусци имају потпуно исти ниво енергије,[6] док следеће подљуске имају више енергије по електрону од претходних. Овај ефекат је довољно велики да се енергетски распони повезани са љускама могу преклапати (погледајте валентне љуске и Ауфбау принцип).
Број електрона у свакој љусци[уреди | уреди извор]
| Име љуске |
Име подљуске |
Макс. електрона у подљусци |
Макс. електрона у љусци |
|---|---|---|---|
| K | 1с | 2 | 2 |
| L | 2с | 2 | 2 + 6 = 8 |
| 2п | 6 | ||
| M | 3с | 2 | 2 + 6 + 10 = 18 |
| 3п | 6 | ||
| 3д | 10 | ||
| N | 4с | 2 | 2 + 6 + 10 + 14 = 32 |
| 4п | 6 | ||
| 4д | 10 | ||
| 4ф | 14 | ||
| O | 5с | 2 | 2 + 6 + 10 + 14 + 18 = 50 |
| 5п | 6 | ||
| 5д | 10 | ||
| 5ф | 14 | ||
| 5г | 18 |
Свака подљуска је ограничена да садржи највише 4ℓ + 2 електрона, наиме:
- Свака с подљуска садржи највише 2 електрона
- Свака п подљуска садржи највише 6 електрона
- Свака д подљуска садржи највише 10 електрона
- Свака ф подљуска садржи највише 14 електрона
- Свака г подљуска садржи највише 18 електрона
Стога, К љуска, која садржи само с подљуску, може да има само до 2 електрона; L љуска, која садржи с и п, може да садржи до 2 + 6 = 8 електрона, и тако даље; генерално, n-та љуска може да садржи до 2n2 електрона.[1]
Иако та формула у принципу даје максимум, у ствари се максимум једино постиже (код познатих елемената) за прве четири љуске (К, L, M, Н). Ни један познати елемент нема више од 32 електрона у било којој љусци.[7][8] То је зато што се подљуске попуњавају по Ауфбау принципу. Први елементи који би имали више од 32 електрона у једној љусци припадали би г-блоку 8. периоде периодног система. Ови елементи би имали неке од електрона у својој 5г подљусци и на тај начин имали би више од 32 електрона у О љусци (петој главној љусци).
Валентна љуска[уреди | уреди извор]
Валентна љуска је најудаљенија љуска атома. Валентни електрони у елементима који нису прелазни метали налазе се у овој љусци. Такви елементи са комплетном валентном шкољком (племенити гасови) су у највећој мери хемијски нереактивни, док су најреактивнији они који имају само један електрон у својој валентној љусци (алкални метали) или им недостаје само један електрон до комплетне љуске (халогени).[9]
Међутим, ова терминологија је донекле погрешна у случају прелазних метала. Код тих елемената валентни електрон такође може бити у унутрашњој љусци. Стога, електрони који одређују како атом хемијски реагује су они који се крећу најудаљеније од језгра, односно они са највишом енергијом, а не нужно у валентној љусци.
Списак елемената са бројем електрона по љусци[уреди | уреди извор]
Следећа листа даје елементе поређане по растућем атомском броју и приказује број електрона по љусци. На први поглед се види да подскупови листе показују очигледне обрасце. Конкретно, седам елемената (са плавом позадином) пре племенитог гаса (група 18, жутом) виши од хелијума, имају број електрона у валентној љусци у аритметичкој прогресији. (Међутим, овај образац се може да буде нарушен у седмој периоди због релативистичких ефеката.)
Сортирање табеле према хемијским групама показује додатне обрасце, посебно у односу на последње две најудаљеније љуске. (Елементи 57 до 71 припадају лантаноидима, док су 89 до 103 актиноиди.)
Следећа листа је првенствено у складу са Ауфбау принципом. Међутим, постоји неколико изузетака од правила; на пример, паладијум (атомски број 46) нема електроне у петој љусци, за разлику од других атома са нижим атомским бројем. Неки уноси у табели су несигурни, јер експериментални подаци нису доступни. (На пример, елементи изнад 108. имају тако кратак полуживот тако да њихове електронске конфигурације још нису мерене.)
| Z | Елемент | Бр. електрона/љуска | Група |
|---|---|---|---|
| 1 | Водоник | 1 | 1 |
| 2 | Хелијум | 2 | 18 |
| 3 | Литијум | 2, 1 | 1 |
| 4 | Берилијум | 2, 2 | 2 |
| 5 | Бор | 2, 3 | 13 |
| 6 | Угљеник | 2, 4 | 14 |
| 7 | Азот | 2, 5 | 15 |
| 8 | Кисеоник | 2, 6 | 16 |
| 9 | Флуор | 2, 7 | 17 |
| 10 | Неон | 2, 8 | 18 |
| 11 | Натријум | 2, 8, 1 | 1 |
| 12 | Магнезијум | 2, 8, 2 | 2 |
| 13 | Алуминијум | 2, 8, 3 | 13 |
| 14 | Силицијум | 2, 8, 4 | 14 |
| 15 | Фосфор | 2, 8, 5 | 15 |
| 16 | Сумпор | 2, 8, 6 | 16 |
| 17 | Хлор | 2, 8, 7 | 17 |
| 18 | Аргон | 2, 8, 8 | 18 |
| 19 | Калијум | 2, 8, 8, 1 | 1 |
| 20 | Калцијум | 2, 8, 8, 2 | 2 |
| 21 | Скандијум | 2, 8, 9, 2 | 3 |
| 22 | Титанијум | 2, 8, 10, 2 | 4 |
| 23 | Ванадијум | 2, 8, 11, 2 | 5 |
| 24 | Хром | 2, 8, 13, 1 | 6 |
| 25 | Манган | 2, 8, 13, 2 | 7 |
| 26 | Гвожђе | 2, 8, 14, 2 | 8 |
| 27 | Кобалт | 2, 8, 15, 2 | 9 |
| 28 | Никал | 2, 8, 16, 2 | 10 |
| 29 | Бакар | 2, 8, 18, 1 | 11 |
| 30 | Цинк | 2, 8, 18, 2 | 12 |
| 31 | Галијум | 2, 8, 18, 3 | 13 |
| 32 | Германијум | 2, 8, 18, 4 | 14 |
| 33 | Арсен | 2, 8, 18, 5 | 15 |
| 34 | Селенијум | 2, 8, 18, 6 | 16 |
| 35 | Бром | 2, 8, 18, 7 | 17 |
| 36 | Криптон | 2, 8, 18, 8 | 18 |
| 37 | Рубидијум | 2, 8, 18, 8, 1 | 1 |
| 38 | Стронцијум | 2, 8, 18, 8, 2 | 2 |
| 39 | Итријум | 2, 8, 18, 9, 2 | 3 |
| 40 | Цирконијум | 2, 8, 18, 10, 2 | 4 |
| 41 | Ниобијум | 2, 8, 18, 12, 1 | 5 |
| 42 | Молибден | 2, 8, 18, 13, 1 | 6 |
| 43 | Технецијум | 2, 8, 18, 13, 2 | 7 |
| 44 | Рутенијум | 2, 8, 18, 15, 1 | 8 |
| 45 | Родијум | 2, 8, 18, 16, 1 | 9 |
| 46 | Паладијум | 2, 8, 18, 18 | 10 |
| 47 | Сребро | 2, 8, 18, 18, 1 | 11 |
| 48 | Кадмијум | 2, 8, 18, 18, 2 | 12 |
| 49 | Индијум | 2, 8, 18, 18, 3 | 13 |
| 50 | Калај | 2, 8, 18, 18, 4 | 14 |
| 51 | Антимон | 2, 8, 18, 18, 5 | 15 |
| 52 | Телур | 2, 8, 18, 18, 6 | 16 |
| 53 | Јод | 2, 8, 18, 18, 7 | 17 |
| 54 | Ксенон | 2, 8, 18, 18, 8 | 18 |
| 55 | Цезијум | 2, 8, 18, 18, 8, 1 | 1 |
| 56 | Баријум | 2, 8, 18, 18, 8, 2 | 2 |
| 57 | Лантан | 2, 8, 18, 18, 9, 2 | 3 |
| 58 | Церијум | 2, 8, 18, 19, 9, 2 | |
| 59 | Празеодимијум | 2, 8, 18, 21, 8, 2 | |
| 60 | Неодимијум | 2, 8, 18, 22, 8, 2 | |
| 61 | Прометијум | 2, 8, 18, 23, 8, 2 | |
| 62 | Самаријум | 2, 8, 18, 24, 8, 2 | |
| 63 | Европијум | 2, 8, 18, 25, 8, 2 | |
| 64 | Гадолинијум | 2, 8, 18, 25, 9, 2 | |
| 65 | Тербијум | 2, 8, 18, 27, 8, 2 | |
| 66 | Диспрозијум | 2, 8, 18, 28, 8, 2 | |
| 67 | Холмијум | 2, 8, 18, 29, 8, 2 | |
| 68 | Ербијум | 2, 8, 18, 30, 8, 2 | |
| 69 | Тулијум | 2, 8, 18, 31, 8, 2 | |
| 70 | Итербијум | 2, 8, 18, 32, 8, 2 | |
| 71 | Лутецијум | 2, 8, 18, 32, 9, 2 | |
| 72 | Хафнијум | 2, 8, 18, 32, 10, 2 | 4 |
| 73 | Тантал | 2, 8, 18, 32, 11, 2 | 5 |
| 74 | Волфрам | 2, 8, 18, 32, 12, 2 | 6 |
| 75 | Ренијум | 2, 8, 18, 32, 13, 2 | 7 |
| 76 | Осмијум | 2, 8, 18, 32, 14, 2 | 8 |
| 77 | Иридијум | 2, 8, 18, 32, 15, 2 | 9 |
| 78 | Платина | 2, 8, 18, 32, 17, 1 | 10 |
| 79 | Злато | 2, 8, 18, 32, 18, 1 | 11 |
| 80 | Жива | 2, 8, 18, 32, 18, 2 | 12 |
| 81 | Талијум | 2, 8, 18, 32, 18, 3 | 13 |
| 82 | Олово | 2, 8, 18, 32, 18, 4 | 14 |
| 83 | Бизмут | 2, 8, 18, 32, 18, 5 | 15 |
| 84 | Полонијум | 2, 8, 18, 32, 18, 6 | 16 |
| 85 | Астат | 2, 8, 18, 32, 18, 7 | 17 |
| 86 | Радон | 2, 8, 18, 32, 18, 8 | 18 |
| 87 | Францијум | 2, 8, 18, 32, 18, 8, 1 | 1 |
| 88 | Радијум | 2, 8, 18, 32, 18, 8, 2 | 2 |
| 89 | Актинијум | 2, 8, 18, 32, 18, 9, 2 | 3 |
| 90 | Торијум | 2, 8, 18, 32, 18, 10, 2 | |
| 91 | Протактинијум | 2, 8, 18, 32, 20, 9, 2 | |
| 92 | Уранијум | 2, 8, 18, 32, 21, 9, 2 | |
| 93 | Нептунијум | 2, 8, 18, 32, 22, 9, 2 | |
| 94 | Плутонијум | 2, 8, 18, 32, 24, 8, 2 | |
| 95 | Америцијум | 2, 8, 18, 32, 25, 8, 2 | |
| 96 | Киријум | 2, 8, 18, 32, 25, 9, 2 | |
| 97 | Берклијум | 2, 8, 18, 32, 27, 8, 2 | |
| 98 | Калифорнијум | 2, 8, 18, 32, 28, 8, 2 | |
| 99 | Ајнштајнијум | 2, 8, 18, 32, 29, 8, 2 | |
| 100 | Фермијум | 2, 8, 18, 32, 30, 8, 2 | |
| 101 | Мендељевијум | 2, 8, 18, 32, 31, 8, 2 | |
| 102 | Нобелијум | 2, 8, 18, 32, 32, 8, 2 | |
| 103 | Лоренцијум | 2, 8, 18, 32, 32, 8, 3 | |
| 104 | Радерфордијум | 2, 8, 18, 32, 32, 10, 2 | 4 |
| 105 | Дубнијум | 2, 8, 18, 32, 32, 11, 2 | 5 |
| 106 | Сиборгијум | 2, 8, 18, 32, 32, 12, 2 | 6 |
| 107 | Боријум | 2, 8, 18, 32, 32, 13, 2 | 7 |
| 108 | Хасијум | 2, 8, 18, 32, 32, 14, 2 | 8 |
| 109 | Мајтнеријум | 2, 8, 18, 32, 32, 15, 2 (?) | 9 |
| 110 | Дармштатијум | 2, 8, 18, 32, 32, 16, 2 (?) | 10 |
| 111 | Рендгенијум | 2, 8, 18, 32, 32, 17, 2 (?) | 11 |
| 112 | Коперницијум | 2, 8, 18, 32, 32, 18, 2 (?) | 12 |
| 113 | Нихонијум | 2, 8, 18, 32, 32, 18, 3 (?) | 13 |
| 114 | Флеровијум | 2, 8, 18, 32, 32, 18, 4 (?) | 14 |
| 115 | Московијум | 2, 8, 18, 32, 32, 18, 5 (?) | 15 |
| 116 | Ливерморијум | 2, 8, 18, 32, 32, 18, 6 (?) | 16 |
| 117 | Тенесин | 2, 8, 18, 32, 32, 18, 7 (?) | 17 |
| 118 | Оганесон | 2, 8, 18, 32, 32, 18, 8 (?) | 18 |
Види још[уреди | уреди извор]
- Периодни систем (електронске конфигурације)
- Бројање електрона
- Правило 18-електрона
- Наелектрисање језгра
Референце[уреди | уреди извор]
- ^ а б Ре: Wхy до елецтрон схеллс хаве сет лимитс ? мадсци.орг, 17 Марцх 1999, Дан Бергер, Фацултy Цхемистрy/Сциенце, Блуффтон Цоллеге
- ^ а б Елецтрон Субсхеллс. Цорросион Соурце.
- ^ Доналд Садоwаy, Интродуцтион то Солид Стате Цхемистрy, Лецтуре 5 Архивирано на сајту Wayback Machine (29. јун 2011)
- ^ Баркла, Цхарлес Г. (1911). „XXXИX.Тхе спецтра оф тхе флуоресцент Рöнтген радиатионс”. Пхилосопхицал Магазине. Сериес 6. 22 (129): 396—412. дои:10.1080/14786440908637137. „Превиоуслy денотед бy леттерс Б анд А (...). Тхе леттерс К анд L аре, хоwевер, преферабле, ас ит ис хигхлy пробабле тхат сериес оф радиатионс ботх море абсорбабле анд море пенетратинг еxист.”
- ^ Јуе, Т. (2009). „Qуантум Мецханиц Басиц то Биопхyсицал Метходс”. Фундаментал Цонцептс ин Биопхyсицс. Берлин: Спрингер. стр. 33. ИСБН 978-1-58829-973-4.
- ^ Тхе статемент тхат тхе елецтронс ин оне субсхелл хаве еxацтлy тхе саме левел оф енергy ис труе ин ан исолатед атом, wхере ит фоллоwс qуантум-мецханицаллy фром тхе спхерицал сyмметрy оф тхе сyстем. Wхен тхе атом ис парт оф а молецуле, тхис но лонгер холдс; сее, фор еxампле, црyстал фиелд тхеорy.
- ^ Орбиталс. Цхем4Кидс. Ретриевед он 1 Децембер 2011.
- ^ Елецтрон & Схелл Цонфигуратион Архивирано на сајту Wayback Machine (28. децембар 2018). Цхемистрy.патент-инвент.цом. Ретриевед он 1 Децембер 2011.
- ^ Цхемицал Реацтионс. Висион Леарнинг (26 Јулy 2011). Ретриевед он 1 Децембер 2011.
