Литијум
 плута у уљу | |||||||||||||||||
| Општа својства | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Име, симбол | литијум, Li | ||||||||||||||||
| Изглед | сребрнобел | ||||||||||||||||
| Заступљеност | 0,006[1][2] | ||||||||||||||||
| У периодноме систему | |||||||||||||||||
| |||||||||||||||||
| Атомски број (Z) | 3 | ||||||||||||||||
| Група, периода | група 1 (алкални метали), периода 2 | ||||||||||||||||
| Блок | s-блок | ||||||||||||||||
| Категорија | алкални метал | ||||||||||||||||
| Рел. ат. маса (Ar) | [6,938, 6,997] конвенционална: 6,94 | ||||||||||||||||
| Ел. конфигурација | [He] 2s1[3] | ||||||||||||||||
по љускама | 2, 1 | ||||||||||||||||
| Физичка својства | |||||||||||||||||
| Агрегатно стање | чврсто | ||||||||||||||||
| Тачка топљења | 453,65 K (180,50 °C, 356,90 °F) | ||||||||||||||||
| Тачка кључања | 1603[4] K (1330 °C, 2426 °F) | ||||||||||||||||
| Густина при с.т. | 0,534[5][6] g/cm3 | ||||||||||||||||
| течно ст., на т.т. | 0,512[2] g/cm3 | ||||||||||||||||
| Критична тачка | 3220 K, 67 MPa (екстраполирано)[7] | ||||||||||||||||
| Топлота фузије | 3,00 kJ/mol | ||||||||||||||||
| Топлота испаравања | 136 kJ/mol | ||||||||||||||||
| Мол. топл. капацитет | 24,860 J/(mol·K) | ||||||||||||||||
Напон паре
| |||||||||||||||||
| Атомска својства | |||||||||||||||||
| Оксидациона стања | +1 (веома кисео оксид) | ||||||||||||||||
| Електронегативност | 0,98 | ||||||||||||||||
| Енергије јонизације | 1: 520,2 kJ/mol 2: 7298,1 kJ/mol 3: 11815,0 kJ/mol | ||||||||||||||||
| Атомски радијус | 152 pm | ||||||||||||||||
| Ковалентни радијус | 128±7 pm | ||||||||||||||||
| Валсов радијус | 182 pm | ||||||||||||||||
| Остало | |||||||||||||||||
| Кристална структура | унутрашњецентр. кубична (BCC) | ||||||||||||||||
| Брзина звука танак штап | 6000 m/s (на 20 °C) | ||||||||||||||||
| Топл. ширење | 46 µm/(m·K) (на 25 °C) | ||||||||||||||||
| Топл. водљивост | 84,8 W/(m·K) | ||||||||||||||||
| Електроотпорност | 92,8 nΩ·m (на 20 °C) | ||||||||||||||||
| Магнетни распоред | парамагнетичан (= 1,4 · 10−5)[8] | ||||||||||||||||
| Магнетна сусцептибилност (χmol) | +14,2·10−6 cm3/mol (298 K)[9] | ||||||||||||||||
| Јангов модул | 4,9 GPa | ||||||||||||||||
| Модул смицања | 4,2 GPa | ||||||||||||||||
| Модул стишљивости | 11 GPa | ||||||||||||||||
| Мосова тврдоћа | 0,6 | ||||||||||||||||
| Бринелова тврдоћа | 5 MPa | ||||||||||||||||
| CAS број | 7439-93-2 | ||||||||||||||||
| Историја | |||||||||||||||||
| Откриће | Јохан Август Арфведсон (1817) | ||||||||||||||||
| Прва изолација | Вилијам Томас Бранд (1821) | ||||||||||||||||
| Главни изотопи | |||||||||||||||||
| |||||||||||||||||
| 6Li садржај може бити низак и до 3,75% у природним узорцима. 7Li стога може да има садржај до 96,25%. | |||||||||||||||||
Литијум (грч. lithos — камен), ознака Li, је најлакши од свих познатих метала. Има редни број 3 у периодном систему елемената, атомску тежину 6,94, специфичну тежину 0,534 (при 20 °C). Он представља смешу два изотопа 7Li(92,6%) и 6Li(7,4%).[10] Литијум је мек, сребрнасто-бео алкални метал у другој периоди периодног система елемената. Литијум је врло лак метал и има најмању густину међу свим чврстим елементима (под стандардним услови), а такође је и елемент најмање густине међу чврстим елементима. Због своје велике реактивности и запаљивости, у природи се не налази у елементарном стању. На собној температури, само на потпуно сувом ваздуху је постојан дуже време, при чему врло споро реагује дајући литијум нитрид. У влажном ваздуху, на површини литијума врло брзо се формира мат сиви слој литијум хидроксида. Литијум се мора чувати у вакууму, инертној атмосфери, или под инертном течношћу као што је пречишћени керозин[11] или минерално уље. Као и сви алкални метали, елементарни литијум реагује одмах већ при додиру са влагом на кожи, те тако може проузроковати тешке опекотине и озледе због нагризања. Многа једињења литијума, која у воденим растворима дају јоне литијума сматрају се опасним за здравље, за разлику од аналогних једињења натријума и калијума.
Литијум се не јавља слободан у природи, већ се јавља углавном у виду пегматитских минерала, који су некада били главни извор литијума. Због своје растворљивости као јона, присутан је у океанској води и обично се добија из сланих раствора. Метални литијум се изолује електролитички из смеше литијум хлорида и калијум хлорида. Као микроелемент, литијум у облику својих соли је често саставни део минералних вода.
Језгро литијумовог атома је гранично стабилно, пошто два стабилна изотопа литијума пронађена у природи имају веома ниске енергије везивања по нуклеону. Због своје релативне нуклеарне нестабилности, литијум је мање заступљен у соларном систему од 25 од првих 32 хемијска елемената, иако су његова језгра веома лагана: то је изузетак од тренда по коме су тежа језгра ређа.[12] Из сродних разлога, литијум има важну употребу у нуклеарној физици. Трансмутација атома литијума у хелијум 1932. године била је прва нуклеарна реакција коју је у потпуности извршио човек, а литијум деутерид служи као гориво за фузију у термонуклеарном оружју.[13]
Литијум и његова једињења имају неколико индустријских примена, укључујући стакло и керамику отпорне на топлоту, литијумска мазива, топионичке адитиве за производњу гвожђа, челика и алуминијума, литијум-металне батерије и литијум-јонске батерије.
У људском организму налазе се врло мале количине овог елемента. Не сматра се неопходним за живот и нема познате биолошке функције у организму. Међутим, неке соли литијума показују медицинско деловање и употребљавају се у литијумској терапији при лечењу биполарних поремећаја, манија, депресија и других сличних болести.
Особине
[уреди | уреди извор]Физичке
[уреди | уреди извор]
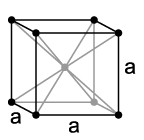
Алкални метали се такође називају породицом литијума, по њиговом водећем елементу. Као и други алкални метали (а то су натријум (Na), калијум (K), рубидијум (Rb), цезијум (Cs) и францијум (Fr), литијум има један валентни електрон који се, у присуству растварача, лако се ослобађа да формира Li+.[15] Због тога је литијум добар проводник топлоте и струје, као и високо реактиван елемент, мада је најмање реактиван од алкалних метала. Нижа реактивност литијума је последица близине његовог валентног електрона његовом језгру (преостала два електрона су у 1s орбитали, много мање енергије и не учествују у хемијским везама).[15] Растопљени литијум је знатно реактивнији од његовог чврстог облика.[16][17]
У чистом стању и у одсуству ваздуха, има сребрнастометални сјај, по чему личи на натријум и калијум, али од њих је тврђи. Метал литијум је довољно мекан да се може сећи ножем. На ваздуху оксидира у литијум оксид.[15] Такође, има и вишу тачку топљења, која износи 180,50 °C (453,65 K; 356,90 °F),[18] а кључа на 1.342 °C (1.615 K; 2.448 °F)[18], што су највише вредности од свих алкалних метала. Густина износи свега 0,534 g/cm3[19] и представља најмању густину од свих чврстих елемената.[20][21] Само водоник у чврстом стању при температури од −260 °C има мању густину од 0,0763 g/cm3.[19][22] Литијум може да плута на најлакшим угљоводоничним уљима и један је од само три метала који могу да плутају на води, при чему су друга два натријум и калијум.

Прилично је испарљив и његова пара боји пламен Бунзенове грејалице кармин црвено, што се користи приликом квалитативне анализе његових соли.[23] Има највећу специфичну топлоту од свих елемената и она износи 0,96 на 50 °C. Литијум међу осталим алкалним металима има највише тачке топљења и кључања као и највећи специфични топлотни капацитет. Иако он има највећу тврдоћу од свих алкалних метала, може се резати ножем а његова Мосова тврдоћа износи 0,6.[6][24] Као типичан метал, добар је проводник струје (проводљивост око 18% од проводљивости бакра[1]) као и топлоте.
Литијумски коефицијент топлотног ширења је два пута већи од алуминијума и скоро четири пута већи од гвожђа.[25] Литијум је суперпроводљив испод 400 μK при стандардном притиску[26] и на вишим температурама (више од 9 К) при веома високим притисцима (>20 GPa).[27] На температурама испод 70 K, литијум, као и натријум, пролази кроз фазну трансформацију без дифузије. На 4,2 K има ромбоедарски кристални систем (са размаком понављања у девет слојева); на вишим температурама трансформише се у тесерални, а затим у кубни кристални систем. На температурама течног хелијума (4 K) преовладава ромбоедарска структура.[28] Вишеструки алотропни облици су идентификовани за литијум при високим притисцима.[29]
Литијум има специфични топлотни капацитет масе од 3,58 килоџула по килограм-келвину, највећи од свих чврстих материја.[30][31] Због тога се метални литијум често користи у расхладним течностима за апликације преноса топлоте.[30]
Попут других алкалних метала, и литијум се кристализује у кубном, просторно центрираном, густо пакованом кристалном систему у просторној групи Im3m са параметром решетке a = 351 pm и две формулске јединице по елементарној ћелији. На изузетно ниским температурама од 78 K мења се кристална структура спонтаним прелазом било у хексагоналну структуру типа магнезијума са параметрима решетке a = 311 pm и c = 509 pm или изменом у изобличену кубну структуру типа бакра (кубна површинско центрирана) са параметром решетке a = 438 pm. Тачан узрок због чега се јавља једна од ових структура није познат.[14]
Литијум испољава велики број сличности са магнезијумом, што се, између осталог, исказује и у чињеници јављања хетеротипских мешаних кристала од литијума и магнезијума, а који имају особину изодиморфије. Иако се магнезијум најгушће кристализује хексагонално, док се насупрот њега литијум кристализује у кубину просторно центрирану кугласту решетку, оба метала се могу хетеротипски мешати.[32] Међутим, ово се дешава само у врло ограниченом распону концентрација, при чему код вишка неке од компоненти, једна од њих намеће (присиљава да промени) кристалну решетку другој.
Јон литијума са −520 kJ/mol[33] има највишу енталпију хидратације међу свим јонима алкалних метала. Стога се он у води у потпуности хидратизује и снажно привлачи молекуле воде. Јон литијума гради две хидратне љуске, једну унутрашњу са четири молекула воде, која је изузетно снажно повезана са литијумовим јоном преко својих атома кисеоника, те једну спољну љуску, која је повезана са јоном Li[H2O]4+ преко „водоничних мостова” са другим молекулима воде. Због тога је јонски радијус хидратизованих јона литијума веома велик, већи чак и од неких јона тешких алкалних метала као што су рубидијум и цезијум, који у воденим растворима не граде такву врсту снажно везаних хидратних љуски.

У гасовитом стању, литијум се не налази у виду појединачних атома, већ у молекуларном стању као дилитијум Li2. На тај начин једновалентни литијум достиже попуњену s-атомску орбиталу а тиме и енергетски повољнију ситуацију. Дилитијум има дужину везе од 267,3 pm и енергију везе од 101 kJ/mol.[34]
Хемијске
[уреди | уреди извор]
Литијум је, као и сви други алкални метали, врло реактиван и врло лако реагује са многим елементима и једињењима (попут воде дајући топлоту). Међу свим алкалним металима, он је највише реактиван. Посебност, по којој се литијум разликује од других алкалних метала је његова реакција са молекуларним азотом градећи литијум нитрид, реакција која се полако одвија већ и на собној температури:
- .
Ово је могуће због велике густине набоја јона литијума Li+ те тако и велике енергије решетке литијум нитрида. Литијум са -3,04 V[33] има најнижи електродни потенцијал у целом периодном систему, те је стога и најмање племенити елемент од свих. Као и сви алкални метали, елементарни литијум се може чувати у керозину (петролеуму) или парафинском уљу, јер у супротном реагује са азотом и кисеоником из ваздуха.
Пошто су радијуси јона литијума Li+ и магнезијума Mg2+ слични по величини, такође постоје и одређене сличности у особинама литијума односно његових једињења са магнезијумом или једињењима магнезијума. Ова сличност у особинама између два елемента из суседних група периодног система позната је и као дијагонална веза (дијагонални ефект). Тако литијум, за разлику од натријума, гради многа металноорганска једињења (органолитијумска једињења), попут бутил литијума или метил литијума. Иста сличност уочена је и између берилијума и алуминијума, као и између бора и силицијума.
На ваздуху гори бљештавом белом светлошћу попут магнезијума, градећи моноксид, али друге оксиде гради теже. Са водоником се једини на црвеном усијању градећи литијум хидрид, а са азотом литијум нитрид. Директно се једини и са халогенима и сумпором и може се рећи да је хемијски активан, али мање од других алкалних метала. Бурно реагује са киселинама, а у реакцији са водом се не пали, чак ни ако вода кључа. Тада настаје реакција:[20]
Изотопи
[уреди | уреди извор]У природи се јављају оба стабилна изотопа литијума 6Li (7,6%) и 7Li (92,4%).[35] Осим њих, познато је још неколико нестабилних изотопа почев од 4Li преко 8Li до 12Li, који се могу добити само вештачким путем. Њихова времена полураспада износе само неколико милисекунди.[36] Оба природна изотопа имају аномално ниску нуклеарну енергију везивања по нуклеону (у поређењу са суседним елементима у периодном систему, хелијумом и берилијумом); литијум је једини елемент са малим бројем који може произвести нето енергију кроз нуклеарну фисију. Два литијумова језгра имају нижу енергију везивања по нуклеону него било који други стабилни нуклиди осим водоника-1, деутеријума и хелијума-3.[37] Као резултат овога, иако веома мале атомске тежине, литијум је мање заступљен у соларном систему од 25 од прва 32 хемијска елемента.[12] Окарактерисано је седам радиоизотопа, од којих су најстабилнији 8Li са временом полураспада од 838 ms и 9Li са полуживотом од 178 ms. Сви преостали радиоактивни изотопи имају период полураспада који је краћи од 8,6 ms. Најкраће живећи изотоп литијума је 4Li, који се распада емисијом протона и има време полураспада од 7,6 × 10−23 s.[38] Изотоп 6Li је један од само пет стабилних нуклида који имају непаран број протона и непаран број неутрона, док су остала четири стабилна непарна-непарна нуклида водоник-2, бор-10, азот-14 и тантал-180m.[39]
7Li је један од примордијалних елемената (или, тачније, примордијалних нуклида) произведених у нуклеосинтези Великог праска. Мала количина 6Li и 7Li се производи у звездама током звездане нуклеосинтезе, али се даље „сагорева“ онолико брзо колико се производи.[40] 7Li се такође може генерисати у угљеничним звездама.[41] Додатне мале количине и 6Li и 7Li могу се генерисати из соларног ветра, космичких зрака који ударају у теже атоме и из раног 7Be радиоактивног распада у соларном систему.[42]
Изотопи литијума се у великој мери фракционишу током широког спектра природних процеса,[43] укључујући формирање минерала (хемијске преципитације), метаболизам и размену јона. Јони литијума замењују магнезијум и гвожђе на октаедарским местима у минералима глине, где је 6Li пожељнији од 7Li, што резултира обогаћивањем светлосног изотопа у процесима хиперфилтрације и промене стена. Познато је да егзотични 11Li показује неутронски ореол, са 2 неутрона који круже око његовог језгра од 3 протона и 6 неутрона. Процес познат као ласерско одвајање изотопа може се користити за одвајање литијумских изотопа, посебно 7Li од 6Li.[44]
Производња нуклеарног оружја и друге примене у нуклеарној физици су главни извор вештачког фракционисања литијума, при чему се лаки изотоп 6Li задржан у индустрији и војним залихама до те мере да је то изазвало благу, али мерљиву промену у односу 6Li према 7Li у природним изворима, као што су реке. Ово је довело до необичне несигурности у стандардизованој атомској тежини литијума, пошто ова количина зависи од природног односа обиља ових природно присутних стабилних изотопа литијума, као што су они доступни у комерцијалним изворима минерала литијума.[45] Оба стабилна изотопа литијума могу се ласерски хладити и коришћена су за производњу прве квантно дегенерисане Бозе–Фермијеве мешавине.[46]

Изотоп 6Li има врло важну улогу у технологији нуклеарне фузије. Поред улоге у нуклеарним фузијским реакторима, служи и као полазни материјал за добијање трицијума у хидрогенској бомби, који је неопходан за фузију са деутеријумом којом се производи енормна количина енергије. Трицијум настаје у плашту фузијског реактора (такозваном бланкету) или унутар хидрогенске бомбе поред хелијума бомбардирањем литијума 6Li неутронима, који настају током фузије, а према следећој нуклеарној реакцији:
- .
Такође, могућа је и реакција
али је она мање погодна.
Из овог разлога, изотоп 6Li се издваја при производњи литијума.[47] Раздвајање изотопа се може вршити на примјер путем размене изотопа литијум амалгама и неког раствореног литијумовог једињења (попут литијум хлорида у етанолу). При томе се може достићи принос од око 50%.[48]
Изотоп 7Li настаје у незнатним количинама у нуклеарним централама путем нуклеарне реакције изотопа бора 10B (кориштен као успоривач неутрона) са неутронима.[49]
Оба изотопа литијума 6Li и 7Li кориштена су у експериментима са ултрахладним квантним гасовима. Тако је начињен и први Бозе-Ајнштајнов кондензат са (бозон) изотопом 7Li.[50] Међутим 6Li је фермион[51][52] те су научници 2003. године успели да молекул овог изотопа претворе у суперфлуид.[53]
Налажење у природи
[уреди | уреди извор]
Заступљен је у земљиној кори у количини од 0,0018%, али је и поред мале процентуалне заступљености веома чест. За разлику од осталих алкалних метала, литијум се у природи налази у облику силиката. Минерали који га садрже су лепидолит, сподумен, амблигонит и петалит, од којих неки и служе као полазна сировина за његово добијање. Највећа лежишта руде литијума су у Боливији, Чилеу, Аргентини, Кини и Аустралији.[54] Пронађен је и у пепелу многих биљака као што је дуван, али и у млеку и крви.[20]
Астрономска заступљеност
[уреди | уреди извор]Иако је синтетисан у Великом праску, литијум (заједно са берилијумом и бором) је знатно мање заступљен у универзуму од других елемената. Ово је резултат релативно ниских звезданих температура неопходних за уништавање литијума, заједно са недостатком уобичајених процеса за његово формирање.[55]
Према савременој космолошкој теорији, литијум — у оба стабилна изотопа (литијум-6 и литијум-7) — је био један од три елемента синтетисана у Великом праску.[56] Иако количина литијума генерисана у нуклеосинтези Великог праска зависи од броја фотона по бариону, за прихваћене вредности може се израчунати заступљеност литијума, мада постоје „космолошка литијумска неслагања“ у универзуму: постоје индикације да старије звезде имају мање литијума него што би требало, а неке млађе звезде имају много више.[57] Недостатак литијума у старијим звездама је очигледно узрокован „мешањем“ литијума у унутрашњост звезда, где се уништава,[58] док се литијум производи у млађим звездама. Иако се трансмутира у два атома хелијума услед судара са протоном на температурама изнад 2,4 милиона степени Целзијуса (већина звезда лако достиже ову температуру у својој унутрашњости), литијум је у заступљенији него што би прорачуни предвидели за звезде касније генерације.[59]

Литијум се такође налази у смеђим патуљастим субзвезданим објектима и појединим аномалним наранџастим звездама. Пошто је литијум присутан у хладнијим, мање масивним смеђим патуљцима, али је уништен у топлијим црвеним патуљцима, његово присуство у спектру звезда може се користити у „литијумском тесту“ да се прави разлика између њих, јер су оба мања од Сунца.[59][61][62] Одређене наранџасте звезде такође могу садржати високу концентрацију литијума. Те наранџасте звезде за које је утврђено да имају већу концентрацију литијума од уобичајене (као што је Кентаур X-4) круже око масивних објеката — неутронских звезда или црних рупа — чија гравитација очигледно повлачи тежи литијум на површину водонично-хелијумске звезде, узрокујући да се више литијума да се запажа.[59]
Дана 27. маја 2020, астрономи су известили да су експлозије класичних нова галактички произвођачи литијума-7.[63][64]
Копнена заступљеност
[уреди | уреди извор]Иако је литијум широко распрострањен на Земљи, он се природно не јавља у елементарном облику због своје високе реактивности.[15] Укупни садржај литијума у морској води је веома велик и процењује се на 230 милијарди тона, при чему елемент постоји у релативно константној концентрацији од 0,14 до 0,25 делова на милион (ppm),[65][66] или 25 микромола;[67] веће концентрације које се приближавају 7 ppm налазе се у близини хидротермалних извора.[66]
Процене за садржај Земљине коре крећу се од 20 до 70 ppm по тежини.[68] Литијум чини око 0,002 процента Земљине коре..[69] У складу са својим именом, литијум чини мањи део магматских стена, са највећим концентрацијама у гранитима. Гранитни пегматити такође обезбеђују највеће обиље минерала који садрже литијум, а сподумен и петалит су комерцијално најисплативији извори.[68] Још један значајан минерал литијума је лепидолит што је сада застарео назив за серију коју чине полилитионит и трилитионит.[70][71] Други извор литијума је хекторитна глина, чији се једини активни развој остварује преко Вестерн литијум корпорације у Сједињеним Државама.[72] Са 20 mg литијума по kg Земљине коре,[73] литијум је 25. најзаступљенији елемент.
Према Приручнику литијума и природног калцијума, „литијум је релативно редак елемент, иако се налази у многим стенама и делу солана, увек је заступљен у веома ниским концентрацијама. Постоји прилично велики број минералних и соних наслага литијума, али само релативно мали број њих има стварну или потенцијалну комерцијалну вредност. Многе наслаге су веома мале, док су друге прениског садржаја.”[74]
Процењује се да Чиле (2020) има далеко највеће резерве (9,2 милиона тона),[75] а Аустралија највећу годишњу производњу (40.000 тона).[75] Једна од највећих резервних база[note 1] литијума налази се у области Салар де Ујуни у Боливији, која има 5,4 милиона тона. Други велики добављачи су Аустралија, Аргентина и Кина.[76][77] Од 2015. године, Чешки геолошки завод је читаве Рудне планине у Чешкој сматра литијумском провинцијом. Регистровано је пет лежишта, једно у близини Циновека се сматра потенцијално економичним налазиштем, са 160 000 тона литијума.[78] У децембру 2019, финска рударска компанија Келибер Ои је известила да њено лежиште литијума Рапасари садржи процењено доказане и вероватне резерве руде од 5,280 милиона тона.[79]
У јуну 2010. године Њујорк Тајмс је известио да су амерички геолози спроводили истраживања на сувим сланим језерима у западном Авганистану верујући да се тамо налазе велика налазишта литијума.[80] Ове процене су „углавном засноване на старим подацима које су прикупили углавном Совјети током своје окупације Авганистана од 1979–1989.“[81] Министарство одбране САД је проценило да су резерве литијума у Авганистану упоредиве са онима у Боливији и назвале су их потенцијалном „Саудијском Арабијом литијума“.[82] У Корнволу, Енглеска, присуство слане воде богате литијумом је било добро познато због историјске рударске индустрије у том региону, а приватни инвеститори су спровели тестове како би истражили потенцијалну екстракцију литијума у овој области.[83][84]
Биолошка заступљеност
[уреди | уреди извор]Литијум се налази у траговима у бројним биљкама, планктону и бескичмењацима, у концентрацијама од 69 до 5.760 делова на милијарду (ppb). Код кичмењака концентрација је нешто нижа, а скоро сва ткива и телесне течности кичмењака садрже литијум у распону од 21 до 763 ppb.[66] Морски организми имају тенденцију да биоакумулирају литијум више од копнених организама.[85] Није познато да ли литијум има физиолошку улогу у било ком од ових организама.[66] Концентрације литијума у људском ткиву су у просеку око 24 ppb (4 ppb у крви и 1,3 ppm у костима).[86]
Биљке лако апсорбују литијум[86] и концентрација литијума у биљном ткиву је типично око 1 ppm.[87] Неке породице биљака биоакумулирају више литијума од других.[87] Концентрације литијума у сувој тежини за чланове породице Solanaceae (која укључује кромпир и парадајз), на пример, могу бити и до 30 ppm, док за зрна кукуруза могу садржати и до 0,05 ppb.[86] Студије концентрације литијума у земљишту богатом минералима дају распон између 0,1 и 50–100 ppm, са неким концентрацијама и до 100–400 ppm, иако је мало вероватно да ће све то бити доступно биљкама.[87] Сматра се да акумулација литијума не утиче на састав есенцијалних хранљивих састојака биљака.[87] Толеранција на литијум варира у зависности од биљних врста и обично је паралелна са толеранцијом на натријум; Кукуруз и Родсова трава, на пример, веома су толерантни на литијумске повреде, док су авокадо и соја веома осетљиви.[87] Слично, литијум у концентрацији од 5 ppm смањује клијавост семена код неких врста (нпр. азијски пиринач и леблебија), али не и код других (нпр. јечам и пшеница).[87]
Многи од главних биолошких ефеката литијума могу се објаснити његовом конкуренцијом са другим јонима.[88] Једновалентни литијумски катјон Li+
такмичи се са другим јонима као што је натријум (непосредно испод литијума у периодичној табели), који је као и литијум такође моновалентни алкални метал. Литијум се такође такмичи са бивалентним јонима магнезијума, чији је јонски радијус (86 pm) приближно једнак литијумском јону[88] (90 pm). Механизми који транспортују натријум кроз ћелијске мембране такође транспортују литијум. На пример, натријумски канали (напонски и епителни) су главни путеви уласка литијума.[88] Јони литијума такође могу да продиру кроз лигандно зависне јонске канале, као и да прођу кроз нуклеарне и митохондријске мембране.[88] Као и натријум, литијум може да уђе и делимично блокира (иако не прожима) калијумове и калцијумове канале.[88] Биолошки ефекти литијума су бројни и разноврсни, али су механизми његовог деловања само делимично схваћени.[89] На пример, студије пацијената лечених литијумом са биполарним поремећајем показују да, између многих других ефеката, литијум делимично преокреће скраћивање теломера код ових пацијената и такође повећава митохондријалну функцију, иако није разјашњено како литијум производи ове фармаколошке ефекте.[89][90] Чак ни тачни механизми укључени у токсичност литијума нису у потпуности схваћени.
Историја
[уреди | уреди извор]
Петалит (LiAlSi4O10) је 1800. године открио бразилски хемичар и државник Хосе Бонифацио де Андрада е Силва у руднику са острва Уте у Шведској.[91][92][93][94] Међутим, тек 1817. Јохан Аугуст Арфведсон, тада радећи у лабораторији хемичара Јенса Јакоба Берцелијуса, открива присуство непознатог елемента док је анализирао руду петалита (Li[4]Al[4][Si4O10]),[95][96][97][98] а недуго касније и у минералима сподумену (LiAl[Si2O6]) и лепидолиту (K(Li,Al)3[(Al,Si)4O10](F,OH)2), након анализе минералних узорака са острва Уте.[99][93] Овај елемент је формирао једињења слична онима натријума и калијума, иако су његови карбонат и хидроксид били мање растворљиви у води и мање алкални.[100] Његов академски учитељ Јакоб Берцелијус предложио је назив lithion, изведеницу из грчког λίθος líthos‚ камен, име које је изведено из материјала из којег је изолован, слично као и код других, до тада познатих, алкалних метала натријума и калијума, а касније се то име усталило у својој латинизираној форми lithium.[101][15][93][98] Немачки хемичар Кристиан Готлоб Гмелин приметио је 1818. године да соли литијума боје пламен у црвену боју.[93][102]
Оба научника су наредних година покушавали да добију овај елемент у чистом стању.[93][98][103] Ово је успело исте године Бранду и Дејвију помоћу поступка електролизе литијум оксида (Li2O), процеса који је раније користио хемичар сер Хамфри Дејви за изоловање алкалних метала калијума и натријума.[59][103][104][105][106] Бранд је такође описао неке чисте соли литијума, као што је хлорид, и процењујући да литија (литијум оксид) садржи око 55% метала, претпоставио је да је атомска тежина литијума око 9,8 g/mol (модерна вредност ~6,94 g/mol).[107] Роберт Бунзен i Огастус Матиесен успели су 1855. помоћу електролизе литијум хлорида (LiCl) да добију још веће количине елементарног литијума.[93][108] Атомску тежину литијума је одредио Ричардс претварањем литијум-хлорида у литијум перхлорат.[20]
Прва комерцијална производња почела је 1923. у немачкој компанији Metallgesellschaft AG (данас Chemetall GmbH), где се добијао помоћу електролизе истопљене смесе литијум- (LiCl) и калијум хлорида (KCl).[93][109][110] Вилхелм Шленк је 1917. синтетисао прво литијуморганско једињење из органских једињења живе.[111] Све до краја Другог светског рата, осим употребе као средство за подмазивање (минерално уље са додатком литијум стеарата) и у индустрији стакла (литијум карбонат или литијум оксид), готово да и нису постојале апликације у којима се користио литијум. Међутим, то се променило након што је САД-у затребао трицијум за прављење хидрогенске бомбе, а који се може добити из литијума. Почела је знатна производња литијума, а једно од најиздашнијих налазишта био је рудник у близини града Кингс Маунтин у Северној Каролини.[112] Пошто трицијум има врло кратко време полураспада, неопходне количине литијума су константно расле, те су у САД у периоду од 1953. до 1963. нагомилане огромне залихе овог метала, које су тек након завршетка Хладног рата 1993. доспеле на светско тржиште.[112]
Осим класичних рударских извора, јефтиније добијање литијума је могуће и из сланих вода. Данас се литијум користи у великим количинама за разне сврхе као што је производња батерија, за полимеризацију еластомера, у грађевинарству, те за органске синтезе у фармацији и аргохемијској индустрији. Од 2007. најважнији сегмент употребе литијума су примарне (такозване „литијумске”) батерије и акумулатори (секундарне или литијум-јонске батерије).[113]
Аустралијски психијатар Џон Кејд је заслужан за поновно увођење и популаризацију употребе литијума за лечење маније 1949. године.[114] Убрзо након тога, током средине 20. века, примењивост литијума за стабилизацију расположења пацијената са манијом и депресијом узела је маха у Европи и Сједињеним Државама.
Производња и употреба литијума претрпела је неколико драстичних промена у историји. Прва велика примена литијума била је у високотемпературним литијумским мастима за авионске моторе и сличне примене у Другом светском рату и убрзо након тога. Ова употреба је подржана чињеницом да сапуни на бази литијума имају вишу тачку топљења од других алкалних сапуна и да су мање корозивни од сапуна на бази калцијума. Мала потражња за литијумским сапунима и мастима за подмазивање била је подржана од стране неколико малих рударских операција, углавном у САД. Потражња за литијумом се драматично повећала током Хладног рата са производњом нуклеарно фузионих оружја. Литијум-6 и литијум-7 производе трицијум када су озрачени неутронима, те су стога корисни за производњу самог трицијума, као и облик чврстог фузионог горива који се користи у водоничним бомбама у облику литијум деутерида. САД су постале главни произвођач литијума између касних 1950-их и средине 1980-их. На крају, залихе литијума биле су отприлике 42.000 тона литијум хидроксида. Залихе литијума су исцрпљене у погледу литијума-6 за 75%, што је било довољно да се утиче на измерену атомску тежину литијума у многим стандардизованим хемикалијама, те чак и на атомску тежину литијума у неким „природним изворима“ литијумских јона који су били „контаминирани“ литијумовим солима испуштеним из постројења за сепарацију изотопа, које су нашле пут у подземне воде.[45][115]
Литијум се користи за смањење температуре топљења стакла и за побољшање понашања при топљењу алуминијум оксида у Хол-Хероултовом процесу.[116][117] Ове две употребе су доминирале тржиштем све до средине 1990-их. Након завршетка трке у нуклеарном наоружању, потражња за литијумом је опала, а продаја залиха Министарства енергије на отвореном тржишту додатно је смањила цене.[115] Средином 1990-их, неколико компанија је почело да изолује литијум из слане воде, што се показало као јефтинија опција од подземног или отвореног рударства. Већина рудника се затворила или се фокусирала на друге материјале, јер се само руда из зонираних пегматита могла копати по конкурентној цени. На пример, амерички рудници у близини Кингс планине у Северној Каролини затворени су пре почетка 21. века.
Развој литијум-јонских батерија повећао је потражњу за литијумом и постао је доминантан вид употребе 2007. године.[118] Са порастом потражње за литијумом у батеријама током 2000-их, нове компаније су прошириле напоре за изолацију из слане воде како би задовољиле растућу потражњу.[112][119]
Сматра се да ће литијум бити један од главних објеката геополитичке конкуренције у свету који ради на обновљиву енергију и зависи од батерија, али ова перспектива је такође критикована због потцењивања моћи економских подстицаја за проширену производњу.[120]
Хемија
[уреди | уреди извор]Метал
[уреди | уреди извор]Литијум лако реагује са водом, али са приметно мањом снагом од других алкалних метала. Реакција формира гас водоник и литијум хидроксид.[15] Када се ставе изнад пламена, једињења литијума дају упадљиву гримизну боју, док кад метал снажно гори, пламен постаје бриљантно сребрн. Литијум се пали и сагорева у кисеонику када је изложен води или воденој пари. У влажном ваздуху, литијум брзо тамни и формира црну превлаку од литијум хидроксида (LiOH и LiOH·H2O), литијум нитрида (Li3N) и литијум карбоната (Li2CO3, насталог секундарном реакцијом између LiOH и CO2).[68] Литијум је један од ретких метала који реагују са гасовитим азотом.[121][122]
Због своје реактивности са водом, а посебно са азотом, метални литијум се обично складишти под угљоводоничним заптивачем, често под вазелином. Иако се тежи алкални метали могу складиштити под минералним уљем, литијум није довољно густ да се потпуно урони у ове течности.[59]
Литијум има дијагонални однос са магнезијумом, елементом сличног атомског и јонског радијуса. Хемијске сличности између два метала укључују формирање нитрида реакцијом са N2, формирање оксида (Li
2O) и пероксида (Li
2O
2) при сагоревању у O2, соли сличне растворљивости и термичке нестабилности карбоната и нитрида.[68][123] Метал реагује са гасовитим водоником на високим температурама да би се добио литијум хидрид (LiH).[124]
Литијум формира различите бинарне и тернарне материјале директном реакцијом са елементима главне групе. Ове Зинтлове фазе,[125][126][127] иако високо ковалентне, могу се посматрати као соли полиатомских ањона као што су Si44-, P73-, и Te52-. Са графитом, литијум формира низ интеркалационих једињења.[123]
Литијум се раствара у амонијаку (и аминима) дајући [Li(NH3)4]+ и солватирани електрон.[123]
Неорганска једињења
[уреди | уреди извор]Литијум формира деривате сличне солима са свим халогенидима и псеудохалидима. Неки примери укључују халогениде LiF, LiCl, LiBr, LiI, као и псеудохалиде и сродне анјоне. Литијум карбонат је описан као најважније једињење литијума.[123] Ова бела чврста супстанца је главни производ оплемењивања литијумових руда. То је претходник другим солима укључујући керамику и материјале за литијумске батерије.
Једињења LiBH
4 и LiAlH
4 су корисни реагенси. Ове соли и многе друге литијумове соли показују изразито високу растворљивост у етрима, за разлику од соли тежих алкалних метала.
У воденом раствору, координациони комплекс [Li(H2O)4]+ преовлађује за многе литијумове соли. Сродни комплекси су познати са аминима и етрима.
Органска хемија
[уреди | уреди извор]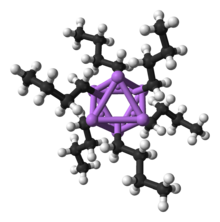
Органолитијумова једињења су бројна и корисна. Дефинисана су присуством везе између угљеника и литијума. Она служе као карбанјони стабилизовани металом, иако су њихови раствори и структуре чврстог стања сложеније од овог поједностављеног погледа.[128] Дакле, ово су изузетно моћне базе и нуклеофили. Такође су примењују у асиметричној синтези у фармацеутској индустрији. За лабораторијску органску синтезу, многи органолитијумски реагенси су комерцијално доступни у облику раствора. Ови реагенси су веома реактивни, а понекад су и пирофорни.
Као и његова неорганска једињења, скоро сва органска једињења литијума формално следе дуетно правило (нпр. BuLi, MeLi). Међутим, важно је напоменути да у одсуству координирајућих растварача или лиганада, органолитијумова једињења формирају димерне, тетрамерне и хексамерне кластере (нпр. BuLi је заправо [BuLi]6, а MeLi је заправо [MeLi]4) који имају вишеструке центре везивања, чиме се повећава координациони број око литијума. Ови кластери се разлажу на мање или мономерне јединице у присуству растварача као што је диметоксиетан (DME) или лиганда као што је тетраметилетилендиамин (TMEDA).[129] Као изузетак од правила дуета, кристалографски је окарактерисан двокоординатни литатни комплекс са четири електрона око литијума, [Li(thf)4]+[((Me3Si)3C)2Li]–.[130]
Структура
[уреди | уреди извор]Иако су једноставне врсте алкиллитијума често представљене као мономер RLi, оне постоје као агрегати (олигомери) или полимери.[131] Степен агрегације зависи од органског супституента и присуства других лиганада.[132][133] Ове структуре су разјашњене различитим методама, посебно 6Li, 7Li, and 13C НМР спектроскопијом и анализом дифракције рендгенских зрака.[134] Рачунарска хемија подржава ове задатке.[131]
Природа везе угљеник-литијум
[уреди | уреди извор]
Релативна електронегативност угљеника и литијума сугерише да је C−Li веза високо поларна.[135][136][137] Међутим, одређена органолитијумова једињења поседују својства као што је растворљивост у неполарним растварачима која компликују проблем.[135] Док већина података сугерише да је C−Li веза у суштини јонска, било је дебате о томе колико ковалентног карактера постоји у њој.[136][137] Према једној процени проценат јонског карактера једињења алкиллитијума износи 80 до 88%.[138]
У алил литијумским једињењима, литијумски катјон се координира према површини угљеничне π везе на η3 начин уместо локализованог, карбанионског центра, тако да су алилитијуми често мање агрегирани од алкиллитијума.[132][139] У ариллитијумским комплексима, литијумски катјон се координира ка једном карбанјонском центру преко Li−C σ типа везе.[132][140]
Структура чврстог стања
[уреди | уреди извор]
Као и друге врсте које се састоје од поларних подјединица, органолитијумске врсте се агрегирају.[133][141] На формирање агрегата утичу електростатичке интеракције, координација између литијума и околних молекула растварача или поларних адитива, и стерички ефекти.[133]
Основни градивни блок за изградњу сложенијих структура је карбанјонски центар који остварује интеракцију са Li3 троуглом на η3- начин.[131] У једноставним алкиллитијумским реагенсима, ови троуглови се агрегирају и формирају тетраедарске или октаедарске структуре. На пример, метиллитијум, етиллитијум и tert-бутиллитијум постоје у тетрамеру [RLi]4. Метиллитијум постоји у виду тетрамера у кластеру кубног типа у чврстом стању, са четири центра литијума који формирају тетраедар. Сваки метанид у тетрамеру у метиллитијуму може имати агостичну интеракцију са литијумским катјонима у суседним тетрамерима.[131][133] Етиллитијум и tert-бутиллитијум, с друге стране, не манифестују ову интеракцију, те су стога растворљиви у неполарним угљоводоничним растварачима. Друга класа алкиллитијума поприма хексамерне структуре, као што су n-бутиллитијум, изопропиллитијум и циклохексаниллитијум.[131]

Уобичајени литијум амиди, нпр. литијум бис(триметилсилил)амид и литијум диизопропиламид, такође су подложни агрегацији.[142] Литијумски амиди усвајају структуре типа полимерне лествице у некоординационом растварачу у чврстом стању, и генерално постоје као димери у етеричним растварачима. У присуству снажно донирајућих лиганада, формирају се три- или тетрамерни литијумски центри.[143] На пример, LDA постоји првенствено у виду димера у THF.[142] Структуре уобичајених литијумских амида, као што су литијум диизопропиламид (LDA) и литијум хексаметилдисилазид (LiHMDS) су свеобухватно проучавали Колам и његови сарадници користећи NMR спектроскопију.[144] Друга важна класа реагенса су силиллитијуми, који се екстензивно користе у синтези органометалних комплекса и полисиланских дендримера.[133][145] У чврстом стању, за разлику од алкиллитијумских реагенаса, већина силиллитијума тежи да формира мономерне структуре координисане са молекулима растварача као што је THF, а само неколико силиллитијума је окарактерисано као виши агрегати.[133] Ова разлика може произаћи из методе припреме силиллитијума, стеричне сметње узроковане гломазним алкил супституентима на силицијуму и мање поларизоване природе Si−Li веза. Додавање снажно донирајућих лиганда, као што су TMEDA и (-)-спартеин, може заменити координирајуће молекуле растварача у силиллитијумима.[133]
Структура у раствору
[уреди | уреди извор]Могуће је да органолитијумски реагенси у раствору усвоје структуре које се разликују од чврстог стања.[132][146] NMR спектроскопија се појавила као моћно средство за проучавање органолитијумских агрегата у раствору. За алкиллитијумске врсте, C−Li Ј спрега се често може користити за одређивање броја литијума у интеракцији са карбанјонским центром, и да ли су ове интеракције статичке или динамичке.[132] Одвојени NMR сигнали такође могу разликовати присуство вишеструких агрегата од заједничке мономерне јединице.[147]
Органолитијумова једињења везују Луисове базе као што су тетрахидрофуран (THF), диетил етар (Et2O), тетраметилетилен диамин (TMEDA) или хексаметилфосфорамид (HMPA).[131] Метиллитијум је посебан случај: на његову тетрамерну структуру не утиче етар или чак HMPA.[133] С друге стране, THF деагрегира хексамерни бутил литијум: тетрамер је главна врста, а ΔG за међуконверзију између тетрамера и димера је око 11 kcal/mol.[148] TMEDA такође може да хелатира са литијумским катјонима у n-бутиллитијуму и формира солватне димере као што је [(TMEDA) LiBu-n)]2.[131][132] Показано је да фениллитијум постоји као искривљени тетрамер у кристализованом етарском солвату и као мешавина димера и тетрамера у етарском раствору.[132]
| Алкил група | Растварач | Структура |
|---|---|---|
| метил | THF | тетрамер |
| етар/HMPA | тетрамер | |
| n‑бутил | пентан | хексамер |
| етар | тетрамер | |
| THF | тетрамер-димер | |
| sec‑бутил | пентан | хексамер-тетрамер |
| изопропил | пентан | хексамер-тетрамер |
| tert‑бутил | пентан | тетрамер |
| THF | мономер | |
| фенил | етар | тетрамер-димер |
| етар/HMPA | димер |
Структура и реактивност
[уреди | уреди извор]Како се структуре органолитијумских реагенаса мењају у зависности од њиховог хемијског окружења, мења се и њихова реактивност и селективност.[133][149] Једно питање које обухвата однос структуре и реактивности је да ли постоји корелација између степена агрегације и реактивности органолитијумских реагенса. Првобитно је предложено да су нижи агрегати као што су мономери реактивнији у алкиллитијумима.[150] Међутим, такође су откривени реакциони путеви у којима су димер или други олигомери реактивне врсте,[151] а за литијум амиде као што је LDA, реакције засноване на димерима су уобичајене..[152] Серија студија кинетике раствора реакција којима посредује LDA сугерише да нижи агрегати енолата не доводе нужно до веће реактивности.[144]
Такође, неке Луисове базе повећавају реактивност органолитијумских једињења.[153][154] Међутим, није увек јасно да ли ови адитиви функционишу као јаки хелатни лиганди и како се уочено повећање реактивности односи на структурне промене у агрегатима изазваним овим адитивима.[153][154] На пример, TMEDA повећава стопе и ефикасност у многим реакцијама које укључују органолитијумске реагенсе.[133] Према алкиллитијум реагенсима, TMEDA делује као донорски лиганд, смањује степен агрегације,[131] и повећава нуклеофилност ових врста.[155] Међутим, TMEDA не функционише увек као донорски лиганд за литијумски катјон, посебно у присуству анјонских центара кисеоника и азота. На пример, он само слабо реагује са LDA и LiHMDS чак и у угљоводоничним растварачима без конкурентских донорских лиганда.[156] У литирању имином, док THF делује као јак донирајући лиганд за LiHMDS, слабо координирајући TMEDA се лако одваја од LiHMDS, што доводи до формирања LiHMDS димера који су реактивније врсте. Дакле, у случају LiHMDS, TMEDA не повећава се реактивност смањењем агрегационог стања.[157] Такође, за разлику од једноставних алкиллитијумових једињења, TMEDA не деагрегира литио-ацетофенолат у THF раствору.[132][158] Додавање HMPA литијум амидима као што су LiHMDS и LDA често резултира мешавином димер/мономерних агрегата у THF. Међутим, однос врста димер/мономер се не мења са повећањем концентрације HMPA, тако да уочено повећање реактивности није резултат деагрегације. Механизам којим ови адитиви повећавају реактивност се још увек истражује.[149]
Реактивност и примена
[уреди | уреди извор]C−Li веза у органолитијумским реагенсима је високо поларизована. Као резултат тога, угљеник привлачи већину електронске густине у вези и подсећа на карбанјон. Дакле, органолитијумски реагенси су јако базични и нуклеофилни. Неке од најчешћих примена органолитијумских реагенаса у синтези укључују њихову употребу као нуклеофила, јаких база за депротонацију, иницијатора за полимеризацију и полазног материјала за припрему других органометалних једињења.
Као нуклеофил
[уреди | уреди извор]Реакције карболитиције
[уреди | уреди извор]Као нуклеофили, органолитијумски реагенси пролазе кроз реакције карболитијације, при чему се веза угљеник-литијум додаје преко двоструке или троструке везе угљеник-угљеник, формирајући нове органолитијумске врсте.[159] Ова реакција је најраспрострањенија реакција органолитијумових једињења. Карболитијација је кључна у процесима анјонске полимеризације, а n-бутиллитијум се користи као катализатор за иницирање полимеризације стирена, бутадиена или изопрена или њихових смеша.[160][161]
Друга примена која користи предност ове реактивности је формирање карбоцикличних и хетероцикличних једињења интрамолекуларном карболитијацијом.[159] Као облик анјонске циклизације, реакције интрамолекуларне карболитијације нуде неколико предности у односу на радикалну циклизацију. Прво, могуће је да цикличне органолитијумске врсте производа реагују са електрофилима, мада је често тешко изоловати радикални интермедијер кореспондирајуће структуре. Друго, анјонске циклизације су често регио- и стереоспецифичније од радикалне циклизације, посебно у случају 5-хексениллитијума. Интрамолекуларна карболитијација омогућава додавање алкил-, виниллитијума на троструке везе и моно-алкил супституисане двоструке везе. Ариллитијуми такође могу бити подвргнути додавању ако се формира петочлани прстен. Ограничења интрамолекуларне карболитијације укључују потешкоће у формирању 3 или 4-чланих прстенова, пошто средње цикличне врсте органолитијума често имају тенденцију да се подвргавају отварању прстена.[159] Испод је дат пример реакције интрамолекуларне карболитијације. Врсте литијума које потичу из литијум-халогенске размене циклизују се да формирају виниллитијум кроз 5-егзо-триг затварање прстена. Виниллитијумове врсте даље реагују са електрофилима и производе функционализована једињења циклопентилидена.[162]
Додатак карбонилним једињењима
[уреди | уреди извор]Нуклеофилни органолитијумски реагенси могу да се додају електрофилним карбонилним двоструким везама да би се формирале везе угљеник-угљеник. Они могу да реагују са алдехидима и кетонима да би произвели алкохоле. Додавање се одвија углавном поларном адицијом, у којој нуклеофилне органолитијумске врсте нападају из екваторијалног правца и стварају аксијални алкохол.[163] Додавање литијумових соли као што је LiClO4 може побољшати стереоселективност реакције.[164]
Када је кетон стерички ометан, употреба Григнардових реагенса често доводи до редукције карбонилне групе уместо адиције.[163] Међутим, мање је вероватно да ће алкиллитијумски реагенси редуковати кетон и могу се користити за синтезу супституисаних алкохола.[165] Испод је пример додавања етиллитијума адамантону за производњу терцијарног алкохола.[166]
Органолитијумски реагенси су такође бољи од Григнардових реагенса у погледу своје способности да реагују са карбоксилним киселинама и формирају кетоне.[163] Ова реакција се може оптимизовати пажљивим контролисањем количине додатог органолитијумског реагенса, или коришћењем триметилсилил хлорида да се уклони вишак литијумског реагенса.[167] Чешћи начин за синтезу кетона је додавање органолитијумских реагенаса Вајнребовим амидима (N-метокси-N-метил амиди). Ова реакција доводи до формирања кетона када се органолитијумски реагенси користе у вишку, услед хелације литијумских јона између N-метокси кисеоника и карбонил кисеоника, који формира тетраедарски међупроизвод који колапсира након киселинског третмана.[168]
Органолитијумски реагенси такође реагују са угљен-диоксидом да би након даљих корака формирали карбоксилне киселине.[169]
У случају енонског супстрата, где су могућа два места нуклеофилне адиције (1,2 адиција карбонилном угљенику или 1,4 конјугована адиција β угљенику), већина високо реактивних органолитијумских врста фаворизује 1,2 адицију, међутим, постоји неколико начина да се органолитијумски реагенси подвргну додавању конјугата. Прво, пошто је 1,4 адукт вероватно термодинамички повољнија врста, адиција конјугата се може постићи еквилибрацијом (изомеризација два производа), посебно када је литијумски нуклеофил слаб и 1,2 адиција је реверзибилна. Друго, додавање донорских лиганда у реакцију формира хетероатомом стабилизоване врсте литијума које фаворизују додавање 1,4 конјугата. У једном примеру, додавање ниског нивоа HMPA растварачу фаворизује 1,4 додавање. У одсуству донорског лиганда, литијум катјон је блиско координисан са атомом кисеоника, међутим, када је литијумски катјон растворен помоћу HMPA, координација између карбонилног кисеоника и литијумског јона је ослабљена. Овај метод се генерално не може користити да утиче на региоселективност алкил- и ариллитијумских реагенаса.[170][171]
Органолитијумски реагенси такође могу извршити енантиоселективно нуклеофилно додавање карбонилу и његовим дериватима, често у присуству хиралних лиганда. Ова реактивност се широко примењује у индустријским синтезама фармацеутских једињења. Један пример је Мерк и Дупонтова синтеза ефавиренза, снажног инхибитора реверзне транскриптазе HIV-а. Литијум ацетилид се додаје у прохирални кетон да би се добио производ хиралног алкохола. Структура активног реакционог интермедијера је одређена NMR спектроскопским студијама у стању раствора, и рендгенском кристалографијом чврстог стања, да је кубни 2:2 тетрамер.[172]
SN2 тип реакција
[уреди | уреди извор]Органолитијумски реагенси могу послужити као нуклеофили и спровести реакције SN2 типа са алкил или алил халидима.[173] Иако се сматрају реактивнијим од Григнардових реагенса у алкилацији, њихова употреба је и даље ограничена због конкурентских споредних реакција као што су радикалне реакције или метал-халогенска размена. Већина органолитијумских реагенса који се користе у алкилацијама је у већој мери стабилизована, мање базна и мање агрегирана, као што су стабилизовани хетероатоми, арил- или алиллитијумски реагенси..[132] Показало се да HMPA повећава брзину реакције и приносе производа, а реактивност ариллитијумског реагенса је често побољшана додатком калијум алкоксида.[163] Органолитијумски реагенси такође могу да изврше нуклеофилне нападе са епоксидима да би се формирали алкохоли.
Као база
[уреди | уреди извор]Органолитијумски реагенси пружају широк спектар базичности. tert-Бутиллитијум, са три алкил групе које слабо донирају електроне, је најјача комерцијално доступна база (pKa = 53). Као резултат тога, кисели протони на −OH, −NH и −SH су често заштићени у присуству органолитијумских реагенса. Неке од најчешће коришћених литијумских база су алкиллитијумове врсте као што су n-бутиллитијум и литијум диалкиламиди (LiNR2). Реагенси са гломазним R групама као што су литијум диизопропиламид (LDA) и литијум бис(триметилсилил)амид (LiHMDS) су често стерички ометани за нуклеофилно додавање, те су стога селективнији према депротонацији. Литијум диалкиламиди (LiNR2</sub) се широко користе при формирању енолата и алдолној реакцији.[174] На реактивност и селективност ових база такође утичу растварачи и други контрајони.
Металација
[уреди | уреди извор]Металација са органолитијумским реагенсима, такође позната као литијација или литијум-водонична размена, постиже се када органолитијумски реагенс, најчешће алкиллитијум, апстрахује протон и формира нову органолитијумску врсту.
-
(1)
Уобичајени реагенси за метализацију су бутиллитијуми. tert-бутиллитијум и sec-бутиллитијум су генерално реактивнији и имају бољу селективност од n-бутиллитијума, међутим, они су такође скупљи и њима се тешко рукује.[174] Метализација је уобичајен начин припреме разноврсних органолитијумских реагенаса. Позиција металације је углавном контролисана киселошћу C-H везе. Литијација се често јавља на позицији α према групама које повлаче електроне, пошто су оне добре у стабилизацији електронске густине анјона. Усмеравајуће групе на ароматичним и хетероцикличним једињењима обезбеђују региоселективна места металације; усмерена орто металација је важна класа реакција металације. Металирани сулфони, ацил групе и α-металирани амиди су важни интермедијери у хемијској синтези. Металирање алил етра са алкиллитијумом или LDA формира анјон у α положају према кисеонику, и може да се настави до 2,3-Витиговог преуређења. Додавање донорских лиганада као што су TMEDA и HMPA може повећати брзину металације и проширити обим супстрата.[175] Хиралним органолитијумским реагенсима се може приступити асиметричном металацијом.[176]
Усмерена орто металација је важно средство у синтези региоспецифичних супституисаних ароматичних једињења. Овај приступ литијацији и накнадном уклањању интермедијерних литијумских врста са електрофилом је често боље од електрофилне ароматичне супституције због своје високе региоселективности. Ова реакција се одвија депротонацијом органолитијумских реагенсима на позицијама α до директне металационе групе (DMG) на ароматичном прстену. DMG је често функционална група која садржи хетероатом који је Луисно базан и може да се координира са Луисно киселим литијум-катјоном. Ово генерише комплексно индуковани ефекат близине, који усмерава депротонацију на α позицији да би се формирала врста ариллитијума која може даље да реагује са електрофилима. Неки од најефикаснијих DMG агенаса су амиди, карбамати, сулфони и сулфонамиди. То су групе које јако повлаче електроне чиме повећавају киселост алфа-протона на ароматичном прстену. У присуству два DMG-а, металација се често јавља орто према јачој усмеравајућој групи, мада се примећују и мешовити производи. Бројна хетероциклична једињења који садрже киселе протоне такође могу бити подвргнута орто-металацији. Међутим, за хетероциклична једињења сиромашна електронима, генерално се користе литијум амидне базе као што је LDA, пошто је примећено да алкиллитијум врши адицију у хетероциклична једињења сиромашна електронима, а не депротонацију. У одређеним прелазним метал-аренским комплексима, као што је фероцен, прелазни метал привлачи електронску густину из арена, чинећи тако ароматичне протоне киселијим и спремним за орто-металацију.[177]
Супербазе
[уреди | уреди извор]Додавање калијум алкоксида алкиллитијуму у великој мери повећава базичност органолитијумских врста.[178] Најчешћа „супербаза” се може формирати додавањем KOtBu бутиллитијуму, често скраћено као „LiCKOR” реагенси. Ове „супербазе” су високо реактивни и често стереоселективни реагенси. У примеру испод, LiCKOR база генерише стереоспецифичну кротилборонатну врсту металацијом и накнадном литијум-металоидном разменом.[179]
Асиметрична металација
[уреди | уреди извор]Енантиообогаћене органолитијумске врсте могу се добити асиметричном металацијом прохиралних супстрата. Асиметрична индукција захтева присуство хиралног лиганда као што је (-)-спартеин.[176] На енантиомерни однос хиралних врста литијума често утичу разлике у стопама депротонације. У примеру испод, третман N-Boc-N-бензиламина са n-бутиллитијумом у присуству (-)-спартеина даје један енантиомерни производ са високим енантиомерним вишком. Трансметалација са триметилкалајхлоридом даје супротан енантиомер.[180]
Формирање енолата
[уреди | уреди извор]Литијумски енолати се формирају депротонацијом C−H везе на α позицији у односу на карбонилну групу од стране органолитијумске врсте. Литијумски енолати се широко користе као нуклеофили у реакцијама формирања везе угљеник-угљеник као што су алдолна кондензација и алкилација. Они су такође важан интермедијер у формирању силил енолног етра.
Формирање литијум енолата може се генерализовати као кисело-базна реакција, у којој релативно кисели протон у α позицији у односу на карбонилну групу (pK =20-28 у DMSO) реагује са органолитијумском базом. Генерално се користе јаке, ненуклеофилне базе, посебно литијумски амиди као што су LDA, LiHMDS и LiTMP. THF и DMSO су уобичајени растварачи у реакцијама литијум енолата.[181]
Стереохемија и механизам формирања енолата изазвали су велико интересовање у хемијској заједници. Многи фактори утичу на исход стереохемије енолата, као што су стерички ефекти, растварач, поларни адитиви и типови органолитијумских база. Међу многим моделима који се користе за објашњење и предвиђање селективности у стереохемији литијум енолата је ирски модел.[182]
У овој претпоставци, мономерни LDA реагује са карбонилним супстратом и формира циклично прелазно стање типа Зимерман-Тракслер. (E)-енолат је фаворизован због неповољне интеракције syn-пентана у (Z)-енолатном прелазном стању.[181]
Додавање поларних адитива као што су HMPA или DMPU фаворизује формирање (Z) енолата. Ирски модел наводи да се ови донорски лиганди координирају са литијумским катјонима, као резултат тога, интеракција карбонил кисеоника и литијума је смањена, а прелазно стање није тако чврсто везано као шесточлана столица. Проценат (Z) енолата се такође повећава када се користе литијумске базе са гломазнијим бочним ланцима (као што је LiHMDS).[181] Међутим, и даље се расправља о механизму путем ког ови адитиви преокрећу стереоселективност.
Било је извесних изазова у погледу применљивости ирског модела, јер он приказује литијумске ентитете као мономере у прелазном стању. У стварности, различити литијумски агрегати се често примећују у растворима литијум енолата, и у зависности од специфичног супстрата, растварача и реакционих услова, може бити тешко одредити који је агрегат стварна реактивна врста у раствору.[181]
Литијум-халогенска размена
[уреди | уреди извор]Литијум-халогенска размена укључује размену хетероатома између органохалида и органолитијумских врста.
-
(2)
Литијум-халогенска размена је веома корисна у припреми нових органолитијумских реагенаса. Примена литијум-халогенске размене је илустрована Пархамовом циклизацијом.[183]
Трансметалација
[уреди | уреди извор]Органолитијумски реагенси се често користе за припрему других органометалних једињења трансметалацијом. Органобакар, органокалај, органосилицијум, органобор, органофосфор, органоцеријум и органосумпорна једињења се често припремају реакцијом органолитијумских реагенса са одговарајућим електрофилима.
-
(3)
Уобичајени типови трансметалације укључују Li/Sn, Li/Hg, и Li/Te размену, која је брза на ниским температурама.[174] Предност Li/Sn размене је у томе што прекурзори три-алкилстанана пролазе кроз неколико споредних реакција, пошто су резултујући нуспроизводи n-Bu3Sn нереактивни према алкиллитијумским реагенсима.[174] У следећем примеру, винилстанан, добијен хидростанилацијом терминалног алкина, формира виниллитијум трансметалацијом са n-BuLi.[184]
Органолитијум се такође може користити за припрему органоцинкових једињења путем трансметалације са солима цинка.[185]
Литијум диорганокупрати се могу формирати реакцијом алкил литијумских једињења са бакар(I) халидом. Добијени органокупрати су генерално мање реактивни према алдехидима и кетонима од органолитијумских реагенса или Григнардових реагенaса.[186]
Припрема
[уреди | уреди извор]Већина једноставних алкиллитијумских реагенса, и уобичајених литијумских амида је комерцијално доступна у различитим растварачима и концентрацијама. Органолитијумски реагенси се такође могу припремити у лабораторији. Испод су наведене неке уобичајене методе за припрему органолитијумских реагенаса.
Реакција са металним литијумом
[уреди | уреди извор]Редукција алкил халида металним литијумом може дати једноставне алкил и арил органолитијумске реагенсе.[163]
-
(4)
Индустријска припрема органолитијумског реагенаса се овим методом постиже третирањем алкил хлорида металним литијумом који садржи 0,5–2% натријума. Конверзија је веома егзотермна. Натријум покреће радикални пут и повећава стопу реакције.[187] Редукција се одвија механизмом радикала. Испод је пример припреме функционализованог литијумског реагенса коришћењем редукције металним литијумом.[188] Понекад се метални литијум у облику финог праха користи у реакцији са одређеним катализаторима као што су нафтален или 4,4'-ди-t-бутилбифенил (DTBB). Још један супстрат који се може редуковати металним литијумом за генерисање алкиллитијумских реагенса су сулфиди. Редукција сулфида је корисна у формирању функционализованих органолитијумских реагенаса као што су алфа-лито етри, сулфиди и силани.[189]
Металација
[уреди | уреди извор]Други метод припреме органолитијумских реагенаса је метализација (размена литијум водоника). Релативна киселост атома водоника контролише положај литијације.
Ово је најчешћи метод за припрему алкиниллитијумског реагенаса, јер је терминални водоник који је везан за sp угљеник веома кисео и лако се депротонира.[163] За ароматична једињења, положај литијације је такође одређен усмеравајућим дејством супституентских група.[190] Неке од најефикаснијих усмеравајућих група супституента су алкокси, амидо, сулфоксид, сулфонил. Металација се често јавља на орто позицији ових супституената. У хетероароматичним једињењима, метализација се обично дешава на орто позицији према хетероатому.[163][190]
Литијум-халогенска размена
[уреди | уреди извор]Трећи метод за припрему органолитијумских реагенса је литијум-халогенска размена.
tert-бутиллитијум или n-бутиллитијум су најчешће коришћени реагенси за генерисање нових органолитијумских врста путем литијум-халогенске размене. Литијум-халогенска размена се углавном користи за претварање арил и алкенил јодида и бромида са sp2 угљеницима у одговарајућа органолитијумова једињења. Реакција је изузетно брза и често се одвија на -60 до -120 °C.[175]
Трансметалација
[уреди | уреди извор]Четврта метода за припрему органолитијумских реагенаса је трансметалација. Овај метод се може користити за припрему виниллитијума.
Шапирова реакција
[уреди | уреди извор]У Шапировој реакцији, два еквивалента јаке алкиллитијумске базе реагују са једињењима p-тозилхидразона да би се произвео виниллитијум, као и олефинск производ.
Руковање
[уреди | уреди извор]Органолитијумска једињења су високо реактивне материје и захтевају специјализоване технике руковања. Често су корозивна, запаљива, а понекад и пирофорна (долази до спонтаног паљења када су изложена ваздуху или влази).[191] Алкиллитијумски реагенси такође могу да се подвргну термичкој разградњи да би се формирале одговарајуће алкил врсте и литијум хидрид.[192] Органолитијумски реагенси се обично чувају на температури испод 10 °C. Реакције се спроводе безваздушним техникама.[74] Концентрација алкиллитијумског реагенса се често одређује титрацијом.[193][194][195]
Органолитијумски реагенси реагују, често споро, са етрима, који се често користе као растварачи.[196]
| Растварач | Темп | n-BuLi | s-BuLi | t-BuLi | MeLi | CH2=C(OEt)-Li | CH2=C(SiMe3)-Li |
|---|---|---|---|---|---|---|---|
| THF | −40 °C | 338 min | |||||
| THF | −20 °C | 42 min | |||||
| THF | 0 °C | 17 h | |||||
| THF | 20 °C | 107 min | >15 h | 17 h | |||
| THF | 35 °C | 10 min | |||||
| THF/TMEDA | −20 °C | 55 h | |||||
| THF/TMEDA | 0 °C | 340 min | |||||
| THF/TMEDA | 20 °C | 40 min | |||||
| Етар | −20 °C | 480 min | |||||
| Етар | 0 °C | 61 min | |||||
| Етар | 20 °C | 153 h | <30 min | 17 d | |||
| Етар | 35 °C | 31 h | |||||
| Етар/TMEDA | 20 °C | 603 min | |||||
| DME | −70 °C | 120 min | 11 min | ||||
| DME | −20 °C | 110 min | 2 min | ≪2 min | |||
| DME | 0 °C | 6 min |
Добијање
[уреди | уреди извор]Производња литијума је значајно порасла од краја Другог светског рата. Главни извори литијума су слана вода и руде. Метални литијум се производи електролизом примењеном на мешавину са 55% литијум хлорида и 45% калијум хлорида на око 450 °C.[197]
| Земља | Продукција | Резерве[note 1] | Ресурси |
|---|---|---|---|
| Аргентина | 6.590 | 3.600.000 | 22.000.000 |
| Аустралија | 74.700 | 6.200.000 | 8.700.000 |
| Аустрија | - | - | 60.000 |
| Боливија | - | - | 23.000.000 |
| Бразил | 2.630 | 390.000 | 800.000 |
| Канада | 520 | 930.000 | 3.000.000 |
| Чиле | 38.000 | 9.300.000 | 11.000.000 |
| Кина | 22.600 | 3.000.000 | 6.800.000 |
| Чешка | - | - | 1.300.000 |
| ДР Конго | - | - | 3.000.000 |
| Финска | - | - | 68.000 |
| Немачка | - | - | 3.800.000 |
| Гана | - | - | 200.000 |
| Индија | - | - | 5.900.000[198][199] |
| Казахстан | - | - | 50.000 |
| Мали | - | - | 890.000 |
| Мексико | - | - | 1.700.000 |
| Намибија | - | - | 230.000 |
| Перу | - | - | 1.000.000 |
| Португалија | 380 | 60.000 | 270.000 |
| Русија | - | - | 1.000.000 |
| Србија | - | - | 1.200.000 |
| Шпанија | - | - | 320.000 |
| Сједињене Државе | 870[note 2] | 1.100.000 | 14.000.000 |
| Зимбабве | 1.030 | 310.000 | 690.000 |
| Друге земље | - | 2.800.000 | - |
| Светски тотал | 146.000[note 3] | 28.000.000 | 105.000.000+ |
Добија се екстракцијом из минерала на разне начине, али се сви они заснивају или на слабијој растворљивости литијум-карбоната, а у односу на карбонате других алкалних метала или на растворљивости литијум хлорида у алкохолу. Такође, литијум се може добити електролизом стопљеног литијум хлорида.[20] Из сланих раствора који садрже литијум, може се исталожити литијум-карбонат разблаживањем водом и додавањем натријум карбоната (соде). Затим се упарава слана вода у ваздуху све док удео литијума не пређе 0,5%. Додавањем натријум карбоната из ње се почиње таложити тешко растворљиви литијум карбонат:
- .
Не рачунајући производњу у САД, током 2008. године у свету је произведено око 27.400 тона литијума,[200] а углавном се на тржишту продавао у облику литијум карбоната (Li2CO3). Од ове количине 12.000 тона отпада на чилеанску Салар де Атакама, а готово 7.000 тона на аустралијски рудник Гринбушес.
Да би се добио метални литијум, прво се литијум карбонату додаје хлороводонична киселина. При томе настаје угљен-диоксид који се издваја као гас, те преостаје растворени литијум хлорид. Овај раствор се ставља у вакуумски испаривач где се упарава, све док се хлорид не искристализује:
Уређаји и опрема која се користи за добијање литијум-хлорида морају бити начињени из посебних врста челика или легура никла, јер слани раствор делује изузетно корозивно. Метални литијум се добија електролизом топивим електродама при температури од 352 °C из истопљене еутектичне смесе из 52 масена постотка литијум хлорида и 48 масена постотка калијум хлорида:
односно:
- .
Међутим, у процесу електролизе, калијум се не издваја, јер у истопљеном хлориду он има нижи електродни потенцијал. За разлику од њега, трагови натријума се издвајају, те чине литијум изузетно реактивним (што је предност у органској хемији, али не и за Li-батерије). Течни литијум се скупља на површини електролита, те се релатно лако може издвојити из електролитичке ћелије. Литијум је такође могуће добити и електролизом литијум-хлорида у пиридину. Ова метода је посебно погодна за лабораторијско добијање мањих количина литијума.
Резерве и заступљеност
[уреди | уреди извор]Мала јонска величина отежава укључивање литијума у ране фазе кристализације минерала. Као резултат, литијум остаје у растопљеним фазама, где се обогаћује, све док се не очврсне у завршним фазама. Такво обогаћивање литијумом је одговорно за настанак свих комерцијално обећавајућих лежишта литијумске руде. Слане воде (и сува со) су још један важан извор Li++. Иако је број познатих наслага и сланишта који садрже литијум велики, већина њих је или мала или има прениске концентрације Li+. Стога се сматра да само неколико има комерцијалну вредност.[201]
Амерички геолошки завод (USGS) процењује да су широм света идентификоване резерве литијума у 2020. и 2021. години износиле 17 милиона и 21 милион тона, респективно.[76][75] Тачна процена светских резерви литијума је тешка.[202][203] Један од разлога за ово је што је већина шема класификације литијума развијена за чврста лежишта руде, док је слани раствор флуид коју је проблематично третирати истом шемом класификације због различитих концентрација и ефеката пумпања.[204]
Године 2019, светска производња литијума из сподумена[205][206][207] била је око 80.000 тона годишње, првенствено из гринбушког пегматита и из неких кинеских и чилеанских извора. Рудник Талисон у Гринбушу је вероватно највећи, и сматра се да има највиши ниво руде са 2,4% Li2O (подаци из 2012. године).[208]
Литијумски троугао и други извори
[уреди | уреди извор]Четири земље с највећом производњом литијума од 2019. године, према извештају Геолошког завода САД, су Аустралија, Чиле, Кина и Аргентина.[76]
Три земље Чиле, Боливија и Аргентина садрже регион познат као литијумски троугао.[209][210] Литијумски троугао је познат по својим висококвалитетним соланама, које укључују боливијски Салар де Ујуни, чилеански Салар де Атакама и аргентински Салар де Аризаро. Верује се да литијумски троугао садржи преко 75% постојећих познатих резерви литијума.[211] Наслаге се такође налазе у Јужној Америци широм планинског ланца Анда. Чиле је водећи произвођач, а следи му Аргентина. Обе земље извлаче литијум из базена слане воде. Према USGS-у, пустиња Ујуни у Боливији има 5,4 милиона тона литијума.[212][213] Половина светских познатих резерви налази се у Боливији дуж централно источних падина Анда. Боливијска влада је уложила 900 милиона долара у производњу литијума и 2021. године је успешно произведено 540 тона.[214][212] Расоли у соланама литијумског троугла веома варирају у садржају литијума.[215] Концентрације такође могу варирати током времена јер су слани раствори променљиве и покретне течности.[215]
У САД, литијум се добија из сланих базена у Невади.[30] Пројекти су такође у развоју у Литијумској долини у Калифорнији.[216]
Тврдостенске наслаге
[уреди | уреди извор]Од 2018. познато је да Демократска Република Конго има једно од највећих налазишта на свету литијумских сподуменских депозита у виду тврдих стена.[217] Налазиште које се налази у Манону, ДРК, може да садржи до 1,5 милијарди тона литијумског сподумена. Два највећа налазишта пегматита (позната као Carriere de l'Este Pegmatite и Roche Dure Pegmatite) су сличне величине или већi од познатог Гринбушког пегматита у Западној Аустралији. Стога се очекује да ће Демократска Република Конго бити значајан добављач литијума у свету високог квалитета и ниским садржајем нечистоћа.
Дана 16. јула 2018. године, 2,5 милиона тона висококвалитетних ресурса литијума и 124 милиона фунти ресурса уранијума пронађено је у тврдостенском лежишту Фалчани у региону Пуно, Перу.[218] Аустралија је 2020. године доделила статус главног пројекта (MPS) Финиском литијумском пројекату за стратешки важно налазиште литијума: процењених 3,45 милиона тона (Mt) минералних ресурса са 1,4 процента литијум оксида.[219][220] Оперативно ископавање је почело 2022. године.[221]
Процењује се да лежиште откривено 2013. године у вајоминшком Рок Спрингс Уплифту садржи 228.000 тона. Додатна лежишта у истој формацији процењена су на чак 18 милиона тона.[222] Слично у Невади, Макдермитова калдера је локација вулканског блата са литијумом који се састоји од највећих познатих депозита литијума у Сједињеним Државама.[223]
Познато је да провинција Пампеан Пегматит у Аргентини има тотал од најмање 200.000 тона сподумена са садржајем литијум оксида (Li2O) који варира између 5 и 8 тежинских %.[224]
Колмозерскоје, највеће налазиште литијума у Русији, налази се у Мурманској области. Године 2023, Поларни литијум, заједничко предузеће Норникла и Росатома, добило је право да развија налазиште. Пројекат има за циљ производњу 45.000 тона литијум карбоната и хидроксида годишње и планира се достизање пуног пројектованог капацитета до 2030. године.[225]
Извори
[уреди | уреди извор]Још један потенцијални извор литијума према подацима из 2012. године идентификован је као процедне воде геотермалних бунара, које се извлаче на површину.[226] Издвајање ове врсте литијума је демонстрирано на терену; литијум се одваја једноставном филтрацијом.[227] Резерве су ограниченије од резерви резервоара слане воде и тврдих стена.
Цене
[уреди | уреди извор]
Године 1998. цена литијум метала је била око 95 USD/kg.[228] После финансијске кризе 2007. године, водећи добављачи, као што је Сосиједад Кимика и Минера (SQM), снизили су цене литијум карбоната за 20%.[229] Цене су порасле 2012. године. У једном чланку објављеном у часопису Пословна недеља из 2012. описана је олигополија литијумског простора: „SQM, који контролише милијардер Хулио Понс, је други по величини, а следи Роквуд, који подржава ККР & Ко. Хенрија Крависа, и филаделфијски FMC“, при чему се Талисон спомиње као највећи произвођач.[230] Сматрало се да глобална потрошња може скочити на 300.000 метричких тона годишње до 2020. са око 150.000 тона у 2012. години, како би подмирила потражња за литијумским батеријама која расте за око 25% годишње, надмашујући укупни пораст производних капацитета литијума од 4% до 5%.[230]
Информативни сервис о ценама ISE – Институт за елементе ретких земаља и стратешке метале – даје за различите литијумске супстанце у просеку од марта до августа 2022. године следеће цене килограма стабилне у току курса: литијум карбонат чистоће 99,5% мин, различитих произвођача између 63 и 72 EUR/kg. Литијум хидроксид монохидрат LiOH 56,5% мин, Кина, 66 до 72 EUR/kg; испоручено Јужној Кореји - 73 EUR/kg. Метални литијум 99,9% мин, испоручено Кини - 42 EUR/kg.[231]
Екстракција
[уреди | уреди извор]
Литијум и његова једињења су историјски изоловани и екстраховани из тврдих стена, али су до 1990-их минерални извори, базени са сланом водом и слановодни депозити постали доминантни извор. Највише их је било у Чилеу, Аргентини и Боливији.[75] Велика лежишта литијумске глине која се развијају у Макдермитовој калдери (Невада, Сједињене Државе) захтевају концентровану сумпорну киселину да би се литијум извукао из глинене руде.[232]
До почетка 2021. године, велики део ископаног литијума на глобалном нивоу долази или из „сподумена, минерала садржаног у тврдим стенама које се налазе на локацијама као што су Аустралија и Северна Каролина“[233] или из слане слане воде која се испумпава директно из земље, као што је на локацијама у Чилеу.[233][215] У чилеанској Салар де Атаками, концентрација литијума у сланој води се повећава соларним испаравањем у систему језера.[215] За обогаћивање процесом испаравања може бити потребно и до годину и по, када слана вода достиже садржај литијума од 6%.[215] Финална обрада у овом примеру се врши у близини града Антофагаста на обали где се чисти литијум карбонат, литијум хидроксид и литијум хлорид производе из слане воде.[215]
Очекује се да ће кобалтне катоде за литијумске батерије захтевати литијум хидроксид, а не литијум карбонат као сировину, а тај тренд фаворизује стену као извор.[234][235][236]
Једна метода за екстракцију литијума, као и других вредних минерала, је обрада геотермалне слане воде кроз електролитичку ћелију која се налази унутар мембране.[237]
Предложена је употреба електродијализе и електрохемијске интеркалације за екстракцију литијумових једињења из морске воде (која садржи литијум у количини од 0,2 дела на милион).[238][239][240][241] Јонско-селективне ћелије унутар мембране у принципу могу сакупљати литијум било коришћењем електричног поља или разликом у концентрацији.[241]
Еколошки проблеми
[уреди | уреди извор]Производни процеси литијума, укључујући раствараче и рударски отпад, представљају значајне опасности по животну средину и здравље.[242][243][244] Екстракција литијума може бити фатална за водени живот због загађења воде.[245] Познато је да се узрокује контаминација површинских вода, контаминација воде за пиће, респираторни проблеми, деградација екосистема и оштећење пејзажа.[242] То такође доводи до неодрживе потрошње воде у сушним регионима (1,9 милиона литара по тони литијума).[242] Огромно стварање нуспроизвода екстракције литијума такође представља нерешене проблеме, као што су велике количине отпада од магнезијума и креча.[246]
У Сједињеним Државама, експлоатација отвореног копа и експлоатација планинских врхова се такмиче са експлоатацијом из слане воде.[247] Забринутост за животну средину обухвата деградацију станишта дивљих животиња, загађење воде за пиће укључујући загађење арсеном и антимоном, неодрживо смањење нивоа воде и масивни рударски отпад, укључујући нуспроизвод радиоактивног уранијума и испуштање сумпорне киселине.
Питања људских права
[уреди | уреди извор]Студија односа између компанија за вађење литијума и староседелачког становништва у Аргентини показала је да држава није заштитила права аутохтоних народа на слободан претходни и информисани пристанак, и да компаније за екстракцију генерално контролишу приступ заједнице информацијама и постављају услове за дискусију о пројекту и подели користи.[248]
Развој рудника литијума Такеров превој у Невади, Сједињене Државе, наишао је на протесте и тужбе неколико домородачких племена која су изјавила да нису дала слободан претходни и информисани пристанак, и да пројекат угрожава културна и света места.[249] Они су такође изразили забринутост да ће развој пројекта створити ризик за урођеничке жене, јер је вађење ресурса повезано са несталим и убијеним домородачким женама.[250] Демонстранти су држали под окупацијом локацију предложеног рудника од јануара 2021. године.[251][247]
Употреба
[уреди | уреди извор]
Највећи део произведених соли литијума се не редукује до металног литијума, већ се користи било директно као литијум карбонат, литијум хидроксид, литијум хлорид, литијум бромид или се преводи у неки друго једињење литијума. Као метал, он је неопходан у одређеном броју апликација, међу којима је највише у индустрији батерија и индустрији стакла и керамике.
Као метал
[уреди | уреди извор]Део произведеног металног литијума користи се за добијање његових једињења, која се не могу директно добити из литијум карбоната. То су, у првом реду, органолитијумска једињења попут бутил литијума, једињења литијума и водоника као литијум хидрида (LiH) или литијум алуминијум хидрида као и литијум амида. Због способности литијума да реагује директно са азотом, користи се и за уклањање тог гаса тамо где је то неопходно.
Метални литијум је изузетно снажно редукционо средство. Он редукује многе материјале, који иначе не реагују са другим редукционим средствима. Употребљава се и за делимично хидрирање ароматичних једињења (Бирчова редукција). У металургији, користи се за одстрањивање сумпора из истопљеног жељеза, дезоксидацију и уклањање угљеника из истопљених метала.
Пошто литијум има веома низак електродни потенцијал, може се употребљавати у батеријама као анода. Такве литијумске батерије имају врло велику густину енергије, а могу произвести посебно висок електрични напон. Треба разликовати литијумске батерије које се не могу поновно пунити са пуњивим литијум-јонским батеријама (акумулаторима), код којих се као катода користи метални оксид литијума као на примјер литијум кобалт оксид, а на страни аноде користи се графит или неко једињење на којем се интеркалирају јони литијума.[252]
Металургија
[уреди | уреди извор]Литијум (нпр. као литијум карбонат) се користи као адитив шљаци из калупа за континуално ливење где повећава флуидност,[253][254] што је употреба која сачињава 5% глобалне потрошње литијума (2011).[76] Једињења литијума се такође користе као адитиви (флуксови) за ливнички песак за ливење гвожђа да би се смањило стварање вена.[255]
Литијум (као литијум флуорид) се користи као адитив у топионицама алуминијума (Хол–Хероултов процес), смањујући температуру топљења и повећавајући електрични отпор,[256] што је употреба која конзумира 3% произведене количине (2011).[76]
Када се користи као флукс за заваривање или лемљење, метални литијум промовише стапање метала током процеса[257] и елиминише стварање оксида апсорбујући нечистоће.[258] Легуре метала са алуминијумом, кадмијумом, бакром и манганом се користе за израду делова авиона високих перформанси и мале густине (видети такође легуре литијум-алуминијума).[259]
Силицијумско нано-заваривање
[уреди | уреди извор]Утврђено је да литијум помаже савршенству силицијумских нано-варова у електронским компонентама за електричне батерије и друге уређаје.[260]
Истраживање (атомска физика)
[уреди | уреди извор]У области атомске физике, литијум се врло често употребљава, јер је као 6Li једини међу алкалним металима са стабилним фермионским изотопом, због чега је погодан за истраживање ефеката у ултрахладним фермионским квантним гасовима. Истовремено, исказује веома широку Фешбачову резонанцу, која омогућава да се дужина распршења између атома подешава по жељи, при чему се не мора посебно прецизно одржавати магнетно поље због ширине резонанце.

Батерије
[уреди | уреди извор]У 2021. години највећи део литијума се користи за прављење литијум-јонских батерија за електричне аутомобиле и мобилне уређаје.
Керамика и стакло
[уреди | уреди извор]Литијум оксид се широко користи као [Flux (metallurgy)[флукс]] за прераду силицијум диоксида, смањујући тачку топљења и вискозитет материјала и доводећи до глазура са побољшаним физичким својствима укључујући ниске коефицијенте топлотног ширења. Широм света, ово је једна од највећих употреба литијумских једињења.[262][263] За посуђе за рерне користе се глазуре које садрже литијум оксиде. Литијум карбонат (Li2CO3) се генерално користи у овом виду примене, јер се при загревању претвара у оксид.[264]
Електрика и електроника
[уреди | уреди извор]Крајем 20. века, литијум је постао важна компонента електролита и електрода батерија, због свог високог електродног потенцијала. Због своје ниске атомске масе, он има висок однос пуњења и снаге према тежини. Типична литијум-јонска батерија може да генерише приближно 3 волта по ћелији, у поређењу са 2,1 волта за оловну киселину и 1,5 волта за цинк-угљеник. Литијум-јонске батерије, које се могу вишеструко пунити и имају високу густину енергије, разликују се од литијум металних батерија, које су једнократне (примарне) батерије са литијумом или његовим једињењима као анодом.[265][266] Остале пуњиве батерије које користе литијум укључују литијум-јонску полимерну батерију, литијум-гвожђе-фосфатну батерију и наножичну батерију.
Током година мишљења су се разликовала о потенцијалном порасту. Једна студија из 2008. је закључила да би „реално остварива производња литијум карбоната била довољна за само мали део будућих захтева глобалног тржишта за PHEV и EV“, да ће „потражња из сектора преносиве електронике апсорбовати већи део планираног повећања производње у наредној деценији“ , те да „масовна производња литијум карбоната није еколошки подобна, да ће нанети непоправљиву еколошку штету екосистемима које треба заштитити и да је литијумско јонски погон некомпатибилан са појмом ’Зеленог аутомобила’“.[77]
Масти за подмазивање
[уреди | уреди извор]Трећа најчешћа употреба литијума је у мазивима. Литијум хидроксид је јака база, а када се загреје са масти, производи сапун, као што је литијум стеарат из стеаринске киселине. Литијумски сапун има способност згушњавања уља и користи се за производњу мазивих масти за све намене на високим температурама.[30][267][268]
Пиротехника
[уреди | уреди извор]
Једињења литијума се користе као пиротехничка бојила и оксиданти у црвеним ватрометима и бакљама.[30][270]
Пречишћавање ваздуха
[уреди | уреди извор]Литијум хлорид и литијум бромид су хигроскопни и користе се као средства за сушење гасних токова.[30] Литијум хидроксид и литијум пероксид су соли које се најчешће користе у затвореним просторима, као што су свемирске летелице и подморнице, за уклањање угљен-диоксида и пречишћавање ваздуха. Литијум хидроксид апсорбује угљен-диоксид из ваздуха формирајући литијум карбонат, и преферира се у односу на друге алкалне хидроксиде због своје мале тежине.
Литијум пероксид (Li2O2) у присуству влаге не само да реагује са угљен-диоксидом и формира литијум карбонат, већ и ослобађа кисеоник.[271][272] Реакција је следећа:
- 2 Li2O2 + 2 CO2 → 2 Li2CO3 + O2
Нека од поменутих једињења, као и литијум перхлорат, користе се у кисеоничним свећама које снабдевају подморнице кисеоником. Она такође могу укључивати мале количине бора, магнезијума, алуминијума, силицијума, титанијума, мангана и гвожђа.[273]
Оптика
[уреди | уреди извор]Литијум флуорид, у облику вештачки формираног кристала, је бистар и транспарентан и често се користи у специјализованој оптици за IR, UV и VUV (вакуумске UV) апликације. Он има један од најнижих индекса преламања и најдаљи опсег трансмисије у дубоким UV зрацима међу уобичајеним материјала.[274] Фино уситњени прах литијум флуорида је коришћен за термолуминисцентну дозиметрију зрачења (TLD): када је такав узорак изложен зрачењу, он акумулира кристалне дефекте који се, када се загреју, решавају ослобађањем плавичасте светлости чији је интензитет пропорционалан апсорбованој дози, што омогућава да се ово квантификује.[275] Литијум флуорид се понекад користи у фокалним сочивима телескопа.[30][276]
Висока нелинеарност литијум ниобата такође га чини корисним у апликацијама нелинеарне оптике. Широко се користи у телекомуникационим производима као што су мобилни телефони и оптички модулатори, за компоненте као што су резонантни кристали. Литијумске апликације се користе у више од 60% мобилних телефона.[277]
Органска и полимерна хемија
[уреди | уреди извор]Органолитијумска једињења се широко користе у производњи полимера и финих хемикалија. У индустрији полимера, која је доминантни потрошач ових реагенаса, једињења алкил литијума су катализатори/иницијатори[278] у анјонској полимеризацији нефункционализованих олефина.[279][280][281] За производњу финих хемикалија, органолитијумова једињења функционишу као јаке базе и као реагенси за формирање угљеник-угљеник веза. Органолитијумска једињења се припремају од металног литијума и алкил халида.[282]
Многа друга једињења литијума се користе као реагенси за припрему органских једињења. Нека популарна једињења укључују литијум алуминијум хидрид (LiAlH4), литијум триетилборохидрид, n-бутиллитијум и tert-бутиллитијум.
Војна примена
[уреди | уреди извор]
Метални литијум и његови комплексни хидриди, као што је литијум алуминијум хидрид (LiAlH4), користе се као високоенергетски адитиви за ракетна горива.[59] LiAlH4 се може користити и сам као чврсто гориво.[283]
Погонски систем са хемијском енергијом (SCEPS) у торпеду Марк 50 користи мали резервоар сумпор хексафлуорида, који се распршује преко блока чврстог литијума. Реакција генерише топлоту, стварајући пару која покреће торпедо у затвореном Ранкиновом циклусу.[284]
Литијум хидрид који садржи литијум-6 се користи у термонуклеарном оружју, где служи као гориво за фузиону фазу бомбе.[285]
Нуклеарна примена
[уреди | уреди извор]Литијум-6 је цењен као изворни материјал за производњу трицијума и као апсорбер неутрона у нуклеарној фузији. Природни литијум садржи око 7,5% литијума-6 из којег су велике количине литијум-6 произведене сепарацијом изотопа за употребу у нуклеарном оружју.[286] Постоји интересовање за употребу литијум-7 у расхладним течностима нуклеарних реактора.[287]

Литијум деутерид је био преферентно фузионо гориво у раним верзијама хидрогенске бомбе. Када су бомбардовани неутронима, 6Li и 7Li производе трицијум - ова реакција, која није била у потпуности схваћена када су водоничне бомбе први пут тестиране, била је одговорна за одбегли принос нуклеарног теста Касл Браво. Трицијум се спаја са деутеријумом у реакцији фузије коју је релативно лако постићи. Иако детаљи остају тајни, литијум-6 деутерид очигледно још увек игра улогу у модерном нуклеарном оружју као фузиони материјал.[288]
Литијум флуорид, када је високо обогаћен изотопом литијум-7, представља основни састојак мешавине флуоридне соли LiF-BeF2 која се користи у нуклеарним реакторима са течним флуором. Литијум флуорид је изузетно хемијски стабилан и смеше LiF-BeF2 имају ниске тачке топљења. Поред тога, 7Li, Be, и F су међу ретким нуклидима са довољно малим попречним пресецима хватања термалних неутрона да не отрују реакције фисије унутар реактора нуклеарне фисије.[note 4][289]
У концептуализованим (хипотетичким) електранама нуклеарне фузије, литијум ће се користити за производњу трицијума у магнетно ограниченим реакторима користећи деутеријум и трицијум као гориво. Природни трицијум је изузетно редак и мора се синтетички производити окружујући реагујућу плазму 'прекривачем' који садржи литијум, где ће неутрони из реакције деутеријум-трицијум у плазми цепати литијум да би произвели више трицијума:
- 6Li + n → 4He + 3H.
Литијум се такође користи као извор за алфа честице, или језгра хелијума. Када 7Li бомбардују убрзани протони, формира се 8Be, који скоро одмах подлеже фисији да би се формирале две алфа честице. Овај подвиг, у то време назван „цепање атома“, био је прва нуклеарна реакција коју је у потпуности направио човек. Остварили су га Кокрофт и Волтон 1932. године.[290][291] Убризгавање литијумовог праха се користи у фузионим реакторима за манипулацију интеракција плазме и материјала, и дисипацију енергије у врућој термонуклеарној фузионој граници плазме.[292][293]
У 2013. години, САД Служба за одговорност изјавила је да недостатак литијума-7 који је критичан за рад 65 од 100 америчких нуклеарних реактора „донекле доводи њихову способност да наставе да обезбеђују електричну енергију у ризик“. Касл Браво је први пут користио литијум-7 у Шримпу, свом првом уређају, који је тежио само 10 тона, и створио је огромну нуклеарну атмосферску контаминацију атола Бикини. Ово је можда разлог за назадовање америчке нуклеарне инфраструктуре.[294] Опрема потребна за одвајање литијума-6 од литијума-7 углавном је остатак Хладног рата. САД су затвориле већину ових постројења 1963. године, када су имале огроман вишак издвојеног литијума, који се углавном трошио током двадесетог века. У извештају се наводи да ће бити потребно пет година и 10 до 12 милиона долара да се поново успоставе капацитети раздвајања литијум-6 од литијума-7.[295]
Реактори који користе литијум-7 загревају воду под високим притиском и преносе топлоту кроз измењиваче топлоте који су склони корозији. Реактори користе литијум да би се супротставили корозивним ефектима борне киселине, која се додаје у воду да апсорбује вишак неутрона.[295]
Медицина
[уреди | уреди извор]Литијум је користан у лечењу биполарног поремећаја.[296] Литијумове соли такође могу бити од помоћи за сродне дијагнозе, као што су шизоафективни поремећај и циклична велика депресија. Активни део ових соли је литијумски јон Li+.[296] Литијум може повећати ризик од развоја Ебстеинове срчане аномалије код одојчади рођених од жена које узимају литијум током првог триместра трудноће.[297]
Већ од 1850. литијум се почео користити у медицини западноевропских земаља као средство против гихта. Међутим, није се показао делотворан. И други видови употребе литијумских соли у медицини су такође остали безуспешни, између осталих и као средство против инфективних болести.
Тек 1949. аустралијски физијатар Џон Кејд описао је могућу област употребе литијумових соли. Он је заморцима убризгавао различита хемијска једињења, између осталих и соли литијума, од чега су они много слабије реаговали на спољне надражаје, те су били много мирнији али не и поспани.[298] Тек након што је исто испробао и на себи између 1952. и 1954. Кејд је подржао употребу литијум карбоната као лека у терапији депресивних, шизофрених и маничних пацијената, а након спроведене опсежне студије на психијатријској болници у Рискову (Данска).[299] Тиме су постављени будући темељи данашње терапије литијумом.
Превентивне мере
[уреди | уреди извор]| Опасности | |
|---|---|
| ГХС пиктограми |  
|
| ГХС сигналне речи | Опасност |
| H260, H314 | |
| P223, P231+232, P280, P305+351+338, P370+378, P422[300] | |
| NFPA 704 | |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
Метални литијум је корозиван и неопходно је посебно руковање како би се избегао контакт са кожом. Удисање литијумове прашине или једињења литијума (која су често алкална) у почетку иритира нос и грло, док већа изложеност може изазвати накупљање течности у плућима, што доводи до плућног едема. Сам метал представља опасност за руковање, јер контакт са влагом производи каустични литијум хидроксид. Литијум се безбедно складишти у нереактивним једињењима као што је нафта.[302]
Види још
[уреди | уреди извор]- Космолошки проблем литијума
- Дилитијум
- Хало језгро
- Изотопи литијума
- Списак земаља према производњи литијума
- Литијска вода
- Литијум-ваздушна батерија
- Сагоревање литијума
- Једињења литијума (категорија)
- Литијум-јонска батерија
- Експеримент са литијумским токамаком
Напомене
[уреди | уреди извор]- ^ а б Appendixes Архивирано 6 новембар 2011 на сајту Wayback Machine. By USGS definitions, the reserve base "may encompass those parts of the resources that have a reasonable potential for becoming economically available within planning horizons beyond those that assume proven technology and current economics. The reserve base includes those resources that are currently economic (reserves), marginally economic (marginal reserves), and some of those that are currently subeconomic (subeconomic resources)."
- ^ In 2013
- ^ Excludes U.S. production
- ^ Берилијум и флуор се јављају само као један изотоп, 9Be и 19F респективно. Ова два, заједно са 7Li, као и 2H, 11B, 15N, 209Bi, и стабилни изотопи C, и O, једини су нуклиди са довољно малим попречним пресецима хватања топлотних неутрона осим актинида да служе као главни састојци растопљене соли оплемењивачког реакторског горива.
Референце
[уреди | уреди извор]- ^ а б dtv-Atlas Chemie. 1 (9 изд.). dtv. 2000. ISBN 9783423032179.
- ^ а б Binder, Harry H. der chemischen Elemente (1999). Lexikon. Stuttgart: S. Hirzel Verlag. ISBN 978-3-7776-0736-8.
- ^ Wieser, Michael E.; Coplen, Tyler B. (2010). „Atomic weights of the elements 2009 (IUPAC Technical Report)”. Pure and Applied Chemistry. 83 (2): 359—396. S2CID 95898322. doi:10.1351/PAC-REP-10-09-14.
- ^ Zhang, Yiming; Julian R. G. Evans; Yang, Shoufeng (2011). „Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks” (PDF). Journal of Chemical & Engineering Data. 56 (2): 328—337. doi:10.1021/je1011086.
- ^ Greenwood, N. N.; Earnshaw, A. (1988). Chemie der Elemente (1 изд.). Weinheim: VCH. стр. 97. ISBN 978-3-527-26169-7.
- ^ а б "„Lithium”. The Gale Encyclopedia of Science. Gale. 2008. ISBN 978-1578516803.
- ^ Bergmann, Ludwig; Schaefer, Clemens; Kassing, Rainer (2005). Lehrbuch der Experimentalphysik, Band 6: Festkörper (2 изд.). Walter de Gruyter. стр. 361. ISBN 978-3-11-017485-4.
- ^ Robert C. Weast, ур. (1990). CRC Handbook of Chemistry and Physics. Boca Raton: CRC (Chemical Rubber Publishing Company). стр. E—129 do E—145. ISBN 978-0-8493-0470-5.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. стр. E110. ISBN 978-0-8493-0464-4.
- ^ Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. изд.). Prentice Hall. ISBN 978-0-13-175553-6.
- ^ Spellman, F. R. (2023). The Science of Lithium. CRC Press.
- ^ а б Numerical data from: Lodders, Katharina (10. 7. 2003). „Solar System Abundances and Condensation Temperatures of the Elements” (PDF). The Astrophysical Journal. The American Astronomical Society. 591 (2): 1220—1247. Bibcode:2003ApJ...591.1220L. S2CID 42498829. doi:10.1086/375492. Архивирано из оригинала (PDF) 7. 11. 2015. г. Приступљено 1. 9. 2015. Graphed at File:SolarSystemAbundances.jpg
- ^ Nuclear Weapon Design. Federation of American Scientists (21 October 1998). fas.org
- ^ а б Schubert, K. (1974). „Ein Modell für die Kristallstrukturen der chemischen Elemente”. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 30: 193—204. doi:10.1107/S0567740874002469..
- ^ а б в г д ђ Krebs, Robert E. (2006). The History and Use of Our Earth's Chemical Elements: A Reference Guide. Westport, Conn.: Greenwood Press. ISBN 978-0-313-33438-2.
- ^ Huang, Chuanfu; Kresin, Vitaly V. (јун 2016). „Note: Contamination-free loading of lithium metal into a nozzle source”. Review of Scientific Instruments (на језику: енглески). 87 (6): 066105. Bibcode:2016RScI...87f6105H. ISSN 0034-6748. PMID 27370506. doi:10.1063/1.4953918.
- ^ Addison, C. C. (1984). The chemistry of the liquid alkali metals. Chichester [West Sussex]: Wiley. ISBN 978-0-471-90508-0. OCLC 10751785.
- ^ а б „PubChem Element Summary for AtomicNumber 3, Lithium”. National Center for Biotechnology Information. 2021. Архивирано из оригинала 10. 9. 2021. г. Приступљено 10. 9. 2021.
- ^ а б Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). Lehrbuch der Anorganischen Chemie (91–100 изд.). Berlin: de Gruyter. стр. 928—931. ISBN 978-3-11-007511-3.
- ^ а б в г д Паркес, Г. Д. & Фил, Д. 1973. Мелорова модерна неорганска хемија. Научна књига. Београд.
- ^ „It's Elemental - The Element Lithium”. education.jlab.org. Архивирано из оригинала 5. 10. 2019. г. Приступљено 9. 10. 2019.
- ^ „Nitrogen, N2, Physical properties, safety, MSDS, enthalpy, material compatibility, gas liquid equilibrium, density, viscosity, inflammability, transport properties”. Encyclopedia.airliquide.com. Архивирано из оригинала 21. 7. 2011. г. Приступљено 29. 9. 2010.
- ^ Рондовић, Д. 1991. Квалитативна хемијска анализа. Научна књига: Београд.
- ^ Litijum na stranici webelements.com, fizičke osobine.
- ^ „Coefficients of Linear Expansion”. Engineering Toolbox. Архивирано из оригинала 30. 11. 2012. г. Приступљено 9. 1. 2011.
- ^ Tuoriniemi, Juha; Juntunen-Nurmilaukas, Kirsi; Uusvuori, Johanna; Pentti, Elias; Salmela, Anssi; Sebedash, Alexander (2007). „Superconductivity in lithium below 0.4 millikelvin at ambient pressure”. Nature. 447 (7141): 187—9. Bibcode:2007Natur.447..187T. PMID 17495921. S2CID 4430500. doi:10.1038/nature05820. Архивирано из оригинала 25. 6. 2019. г. Приступљено 20. 4. 2018.
- ^ Struzhkin, V. V.; Eremets, M. I.; Gan, W; Mao, H. K.; Hemley, R. J. (2002). „Superconductivity in dense lithium”. Science. 298 (5596): 1213—5. Bibcode:2002Sci...298.1213S. PMID 12386338. S2CID 21030510. doi:10.1126/science.1078535.
- ^ Overhauser, A. W. (1984). „Crystal Structure of Lithium at 4.2 K”. Physical Review Letters. 53 (1): 64—65. Bibcode:1984PhRvL..53...64O. doi:10.1103/PhysRevLett.53.64.
- ^ Schwarz, Ulrich (2004). „Metallic high-pressure modifications of main group elements”. Zeitschrift für Kristallographie. 219 (6–2004): 376—390. Bibcode:2004ZK....219..376S. S2CID 56006683. doi:10.1524/zkri.219.6.376.34637.
- ^ а б в г д ђ е Hammond, C. R. (2000). The Elements, in Handbook of Chemistry and Physics (81st изд.). CRC press. ISBN 978-0-8493-0481-1.
- ^ SPECIFIC HEAT OF SOLIDS. bradley.edu
- ^ Malissa, H. (1959). „Die Trennung des Lithiums vom Magnesium in Lithium-Magnesium-Legierungen”. Fresenius' Zeitschrift für Analytische Chemie. 171 (4): 281—282. S2CID 94700911. doi:10.1007/BF00555410..
- ^ а б Binnewies, M. (2004). Allgemeine und Anorganische Chemie (1 изд.). Spektrum Verlag. стр. 241. ISBN 978-3827402080.
- ^ Winter, Mark J. Bonding (1994). Chemical. Oxford University Press. ISBN 978-0-19-855694-7.
- ^ Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). „The NUBASE2020 evaluation of nuclear properties” (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ The Nubase evaluation of nuclear and decay properties Архивирано на сајту Wayback Machine (24. јул 2013) (PDF, engl.).
- ^ File:Binding energy curve - common isotopes.svg shows binding energies of stable nuclides graphically; the source of the data-set is given in the figure background.
- ^ Sonzogni, Alejandro. „Interactive Chart of Nuclides”. National Nuclear Data Center: Brookhaven National Laboratory. Архивирано из оригинала 23. 7. 2007. г. Приступљено 6. 6. 2008.
- ^ Various (2002). Lide, David R., ур. Handbook of Chemistry & Physics (88th изд.). CRC. ISBN 978-0-8493-0486-6. OCLC 179976746. Архивирано из оригинала 24. 7. 2017. г. Приступљено 2008-05-23.
- ^ Asplund, M.; et al. (2006). „Lithium Isotopic Abundances in Metal-poor Halo Stars”. The Astrophysical Journal. 644 (1): 229—259. Bibcode:2006ApJ...644..229A. S2CID 394822. arXiv:astro-ph/0510636
 . doi:10.1086/503538.
. doi:10.1086/503538.
- ^ Denissenkov, P. A.; Weiss, A. (2000). „Episodic lithium production by extra-mixing in red giants”. Astronomy and Astrophysics. 358: L49—L52. Bibcode:2000A&A...358L..49D. arXiv:astro-ph/0005356
 .
.
- ^ Chaussidon, M.; Robert, F.; McKeegan, K. D. (2006). „Li and B isotopic variations in an Allende CAI: Evidence for the in situ decay of short-lived 10Be and for the possible presence of the short−lived nuclide 7Be in the early solar system” (PDF). Geochimica et Cosmochimica Acta. 70 (1): 224—245. Bibcode:2006GeCoA..70..224C. doi:10.1016/j.gca.2005.08.016. Архивирано из оригинала (PDF) 18. 7. 2010. г.
- ^ Seitz, H. M.; Brey, G. P.; Lahaye, Y.; Durali, S.; Weyer, S. (2004). „Lithium isotopic signatures of peridotite xenoliths and isotopic fractionation at high temperature between olivine and pyroxenes”. Chemical Geology. 212 (1–2): 163—177. Bibcode:2004ChGeo.212..163S. doi:10.1016/j.chemgeo.2004.08.009.
- ^ Duarte, F. J (2009). Tunable Laser Applications. CRC Press. стр. 330. ISBN 978-1-4200-6009-6.
- ^ а б Coplen, T. B.; Bohlke, J. K.; De Bievre, P.; Ding, T.; Holden, N. E.; Hopple, J. A.; Krouse, H. R.; Lamberty, A.; Peiser, H. S.; et al. (2002). „Isotope-abundance variations of selected elements (IUPAC Technical Report)”. Pure and Applied Chemistry. 74 (10): 1987. doi:10.1351/pac200274101987
 .
.
- ^ Truscott, Andrew G.; Strecker, Kevin E.; McAlexander, William I.; Partridge, Guthrie B.; Hulet, Randall G. (2001-03-30). „Observation of Fermi Pressure in a Gas of Trapped Atoms”. Science (на језику: енглески). 291 (5513): 2570—2572. Bibcode:2001Sci...291.2570T. ISSN 0036-8075. PMID 11283362. S2CID 31126288. doi:10.1126/science.1059318.
- ^ ABC oružje.
- ^ Bauer, Richard (1985). „Lithium – wie es nicht im Lexikon steht”. Chemie in unserer Zeit. 19 (5): 167—173. doi:10.1002/ciuz.19850190505.
- ^ Volkmer, Martin (2007). Kernenergie Basiswissen (PDF). Inforum. стр. 39. ISBN 978-3-926956-44-6. Архивирано из оригинала (PDF) 17. 6. 2012. г. Приступљено 1. 4. 2019.
- ^ Bradley, C. C.; Sackett, C. A.; Tollett, J. J.; Hulet, R. G. (1995). „Evidence of Bose-Einstein Condensation in an Atomic Gas with Attractive Interactions”. Physical Review Letters. 75 (9): 1687—1690. PMID 10060366. doi:10.1103/PhysRevLett.75.1687. hdl:1911/79442.
- ^ Fermionic Studies in 6Lithium
- ^ Ling, A. V. (2006). Focus on Boson Research. Nova Publishers. стр. 184. ISBN 9781594545207.
- ^ Jochim, S.; Bartenstein, M.; Altmeyer, A.; Hendl, G.; Riedl, S.; Chin, C.; Hecker Denschlag, J.; Grimm, R. (2003). „Bose-Einstein Condensation of Molecules”. Science. 302 (5653): 2101—2103. PMID 14615548. S2CID 13041446. doi:10.1126/science.1093280.
- ^ Dodaci; Po definicijama USGS, bazne rezerve obuhvataju one dijelove resursa koji imaju dovoljan potencijal da postanu ekonomski dostupne u okviru planiranih nivoa a izvan onih koji pretpostavljaju dokazane tehnologije i trenutne ekonomije. Bazna rezerva uključuje one resurse koji su trenutno ekonomični (rezerve), granično ekonomični (granične rezerve) i neke od onih koji su trenutno neekonomični (subekonomski resursi).
- ^ „Element Abundances” (PDF). Архивирано из оригинала (PDF) 1. 9. 2006. г. Приступљено 17. 11. 2009.
- ^ Boesgaard, A. M.; Steigman, G. (1985). „Big bang nucleosynthesis – Theories and observations”. Annual Review of Astronomy and Astrophysics. Palo Alto, CA. 23: 319—378. Bibcode:1985ARA&A..23..319B. doi:10.1146/annurev.aa.23.090185.001535. A86-14507 04–90.
- ^ Woo, Marcus (21. 2. 2017). „The Cosmic Explosions That Made the Universe”. earth. BBC. Архивирано из оригинала 21. 2. 2017. г. Приступљено 21. 2. 2017. „A mysterious cosmic factory is producing lithium. Scientists are now getting closer at finding out where it comes from”
- ^ Cain, Fraser (16. 8. 2006). „Why Old Stars Seem to Lack Lithium”. Архивирано из оригинала 4. 6. 2016. г.
- ^ а б в г д ђ Emsley, John (2001). Nature's Building Blocks. Oxford: Oxford University Press. ISBN 978-0-19-850341-5.
- ^ „First Detection of Lithium from an Exploding Star”. Архивирано из оригинала 1. 8. 2015. г. Приступљено 29. 7. 2015.
- ^ Cain, Fraser. „Brown Dwarf”. Universe Today. Архивирано из оригинала 25. 2. 2011. г. Приступљено 17. 11. 2009.
- ^ Reid, Neill (10. 3. 2002). „L Dwarf Classification”. Архивирано из оригинала 21. 5. 2013. г. Приступљено 6. 3. 2013.
- ^ Arizona State University (1. 6. 2020). „Class of stellar explosions found to be galactic producers of lithium”. EurekAlert!. Архивирано из оригинала 3. 6. 2020. г. Приступљено 2. 6. 2020.
- ^ Starrfield, Sumner; et al. (27. 5. 2020). „Carbon–Oxygen Classical Novae Are Galactic 7Li Producers as well as Potential Supernova Ia Progenitors”. The Astrophysical Journal. 895 (1): 70. Bibcode:2020ApJ...895...70S. S2CID 203610207. arXiv:1910.00575
 . doi:10.3847/1538-4357/ab8d23
. doi:10.3847/1538-4357/ab8d23  .
.
- ^ „Lithium Occurrence”. Institute of Ocean Energy, Saga University, Japan. Архивирано из оригинала 2. 5. 2009. г. Приступљено 13. 3. 2009.
- ^ а б в г „Some Facts about Lithium”. ENC Labs. Архивирано из оригинала 10. 7. 2011. г. Приступљено 15. 10. 2010.
- ^ Schwochau, Klaus (1984). „Extraction of metals from sea water”. Inorganic Chemistry. Topics in Current Chemistry. 124. Springer Berlin Heidelberg. стр. 91—133. ISBN 978-3-540-13534-0. S2CID 93866412. doi:10.1007/3-540-13534-0_3.
- ^ а б в г Kamienski, Conrad W.; McDonald, Daniel P.; Stark, Marshall W.; Papcun, John R. (2004). „Lithium and lithium compounds”. Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. ISBN 978-0-471-23896-6. doi:10.1002/0471238961.1209200811011309.a01.pub2.
- ^ „lithium”. Britannica encyclopedia. Архивирано из оригинала 5. 8. 2020. г. Приступљено 4. 8. 2020.
- ^ Atkins, Peter (2010). Shriver & Atkins' Inorganic Chemistry (5th изд.). New York: W. H. Freeman and Company. стр. 296. ISBN 978-0-19-923617-6.
- ^ „Mindat.org - Mines, Minerals and More”. www.mindat.org. Архивирано из оригинала 22. 4. 2011. г. Приступљено 4. 8. 2019.
- ^ Moores, S. (јун 2007). „Between a rock and a salt lake”. Industrial Minerals. 477: 58.
- ^ Taylor, S. R.; McLennan, S. M.; The continental crust: Its composition and evolution, Blackwell Sci. Publ., Oxford, 330 pp. (1985).
- ^ Garrett, Donald (2004) Handbook of Lithium and Natural Calcium, Academic Press, cited in The Trouble with Lithium 2 Архивирано 14 јул 2011 на сајту Wayback Machine, Meridian International Research (2008)
- ^ а б в г д „Mineral Commodity Summaries 2024” (PDF). U.S. Geological Survey. 29. 1. 2024. Архивирано (PDF) из оригинала 21. 3. 2024. г. Приступљено 21. 3. 2024.
- ^ а б в г д Lithium Statistics and Information, U.S. Geological Survey, 2018, Архивирано из оригинала 3. 3. 2016. г., Приступљено 25. 7. 2002
- ^ а б „The Trouble with Lithium 2” (PDF). Meridian International Research. 2008. Архивирано из оригинала (PDF) 14. 7. 2011. г. Приступљено 29. 9. 2010.
- ^ Czech Geological Survey (октобар 2015). Mineral Commodity Summaries of the Czech Republic 2015 (PDF). Prague: Czech Geological Survey. стр. 373. ISBN 978-80-7075-904-2. Архивирано (PDF) из оригинала 6. 1. 2017. г.
- ^ „Ore Reserve grows its Finland lithium deposit by 50%”. 2019. Архивирано из оригинала 10. 12. 2019. г. Приступљено 10. 12. 2019.
- ^ Risen, James (13. 6. 2010). „U.S. Identifies Vast Riches of Minerals in Afghanistan”. The New York Times. Архивирано из оригинала 17. 6. 2010. г. Приступљено 13. 6. 2010.
- ^ Page, Jeremy; Evans, Michael (15. 6. 2010). „Taleban zones mineral riches may rival Saudi Arabia says Pentagon”. The Times. London. Архивирано из оригинала 14. 5. 2011. г.
- ^ Hosp, Gerald (30. 8. 2021). „Afghanistan: die konfliktreichen Bodenschätze”. Neue Zürcher Zeitung (на језику: немачки). Архивирано из оригинала 8. 9. 2021. г. Приступљено 2021-09-01.
- ^ Bliss, Dominic (28. 5. 2021). „National Geographic”. In Cornwall, ruinous tin and copper mines are yielding battery-grade lithium. Here's what that means. Архивирано из оригинала 13. 6. 2021. г. Приступљено 13. 6. 2021.
- ^ „Cornwall lithium deposits 'globally significant'”. BBC. 17. 9. 2020. Архивирано из оригинала 13. 6. 2021. г. Приступљено 13. 6. 2021.
- ^ Chassard-Bouchaud, C.; Galle, P.; Escaig, F.; Miyawaki, M. (1984). „Bioaccumulation of lithium by marine organisms in European, American, and Asian coastal zones: microanalytic study using secondary ion emission”. Comptes Rendus de l'Académie des Sciences, Série III. 299 (18): 719—24. PMID 6440674.
- ^ а б в Emsley, John (25. 8. 2011). Nature's Building Blocks: An A-Z Guide to the Elements. OUP Oxford. стр. 290—298. ISBN 978-0-19-960563-7. Архивирано из оригинала 26. 8. 2023. г. Приступљено 17. 6. 2016.
- ^ а б в г д ђ Bach, Ricardo O.; Gallicchio, Vincent S., ур. (1990). Lithium and Cell Physiology. New York, NY: Springer New York. стр. 25—46. ISBN 978-1-4612-7967-9. S2CID 44374126. doi:10.1007/978-1-4612-3324-4.
- ^ а б в г д Jakobsson, Eric; Argüello-Miranda, Orlando; Chiu, See-Wing; Fazal, Zeeshan; Kruczek, James; Nunez-Corrales, Santiago; Pandit, Sagar; Pritchet, Laura (2017-11-10). „Towards a Unified Understanding of Lithium Action in Basic Biology and its Significance for Applied Biology”. The Journal of Membrane Biology. Springer Science and Business Media LLC. 250 (6): 587—604. ISSN 0022-2631. PMC 5696506
 . PMID 29127487. doi:10.1007/s00232-017-9998-2.
. PMID 29127487. doi:10.1007/s00232-017-9998-2.
- ^ а б Alda, M (17. 2. 2015). „Lithium in the treatment of bipolar disorder: pharmacology and pharmacogenetics”. Molecular Psychiatry. Nature Publishing Group. 20 (6): 661—670. ISSN 1359-4184. PMC 5125816
 . PMID 25687772. doi:10.1038/mp.2015.4.
. PMID 25687772. doi:10.1038/mp.2015.4.
- ^ Martinsson, L; Wei, Y; Xu, D; Melas, P A; Mathé, A A; Schalling, M; Lavebratt, C; Backlund, L (2013). „Long-term lithium treatment in bipolar disorder is associated with longer leukocyte telomeres”. Translational Psychiatry. Nature Publishing Group. 3 (5): e261—. ISSN 2158-3188. PMC 3669924
 . PMID 23695236. doi:10.1038/tp.2013.37.
. PMID 23695236. doi:10.1038/tp.2013.37.
- ^ D'Andraba (1800). „Des caractères et des propriétés de plusieurs nouveaux minérauxde Suède et de Norwège, avec quelques observations chimiques faites sur ces substances”. Journal de Physique, de Chimie, d'Histoire Naturelle, et des Arts. 51: 239. Архивирано из оригинала 13. 7. 2015. г.
- ^ „Petalite Mineral Information”. Mindat.org. Архивирано из оригинала 16. 2. 2009. г. Приступљено 10. 8. 2009.
- ^ а б в г д ђ е „Lithium:Historical information”. Архивирано из оригинала 16. 10. 2009. г. Приступљено 10. 8. 2009.
- ^ Weeks, Mary (2003). Discovery of the Elements. Whitefish, Montana, United States: Kessinger Publishing. стр. 124. ISBN 978-0-7661-3872-8.
- ^ Berzelius (1817). „Ein neues mineralisches Alkali und ein neues Metall” [A new mineral alkali and a new metal]. Journal für Chemie und Physik. 21: 44—48. Архивирано из оригинала 3. 12. 2016. г. From p. 45: "Herr August Arfwedson, ein junger sehr verdienstvoller Chemiker, der seit einem Jahre in meinem Laboratorie arbeitet, fand bei einer Analyse des Petalits von Uto's Eisengrube, einen alkalischen Bestandtheil, … Wir haben es Lithion genannt, um dadurch auf seine erste Entdeckung im Mineralreich anzuspielen, da die beiden anderen erst in der organischen Natur entdeckt wurden. Sein Radical wird dann Lithium genannt werden." (Mr. August Arfwedson, a young, very meritorious chemist, who has worked in my laboratory for a year, found during an analysis of petalite from Uto's iron mine, an alkaline component … We've named it lithion, in order to allude thereby to its first discovery in the mineral realm, since the two others were first discovered in organic nature. Its radical will then be named "lithium".)
- ^ „Johan August Arfwedson”. Periodic Table Live!. Архивирано из оригинала 7. 10. 2010. г. Приступљено 10. 8. 2009.
- ^ „Johan Arfwedson”. Архивирано из оригинала 5. 6. 2008. г. Приступљено 10. 8. 2009.
- ^ а б в van der Krogt, Peter. „Lithium”. Elementymology & Elements Multidict. Архивирано из оригинала 16. 6. 2011. г. Приступљено 5. 10. 2010.
- ^ See:
- Arfwedson, Aug. (1818) „Afhandlingar i fysik, kemi och mineralogi”. 1818. Архивирано из оригинала 25. 11. 2017. г. Приступљено 27. 7. 2017., Afhandlingar i Fysik, Kemi och Mineralogi, 6 : 145–172. (in Swedish)
- Arfwedson, Aug. (1818) "Untersuchung einiger bei der Eisen-Grube von Utö vorkommenden Fossilien und von einem darin gefundenen neuen feuerfesten Alkali" Архивирано 13 март 2021 на сајту Wayback Machine (Investigation of some minerals occurring at the iron mines of Utö and of a new refractory alkali found therein), Journal für Chemie und Physik, 22 (1) : 93–117. (in German)
- ^ Clark, Jim (2005). „Compounds of the Group 1 Elements”. Архивирано из оригинала 11. 3. 2009. г. Приступљено 10. 8. 2009.
- ^ Figurowski, N. (1981). Die Entdeckung der chemischen Elemente und der Ursprung ihrer Namen. Köln: Aulis-Verlag Deubner. стр. 135. ISBN 978-3-7614-0561-1.
- ^ Gmelin, C. G. (1818). „Von dem Lithon” [On lithium]. Annalen der Physik. 59 (7): 238—241. Bibcode:1818AnP....59..229G. doi:10.1002/andp.18180590702. Архивирано из оригинала 9. 11. 2015. г. „p. 238 Es löste sich in diesem ein Salz auf, das an der Luft zerfloss, und nach Art der Strontiansalze den Alkohol mit einer purpurrothen Flamme brennen machte. (There dissolved in this [solvent; namely, absolute alcohol] a salt that deliquesced in air, and in the manner of strontium salts, caused the alcohol to burn with a purple-red flame.)”
- ^ а б Enghag, Per (2004). Encyclopedia of the Elements: Technical Data – History –Processing – Applications. Wiley. стр. 287—300. ISBN 978-3-527-30666-4.
- ^ Brande, William Thomas (1821) A Manual of Chemistry, 2nd ed. London, England: John Murray, vol. 2, Brande, William Thomas (1821). „A manual of chemistry”. Архивирано из оригинала 19. 1. 2023. г. Приступљено 13. 8. 2015.
- ^ „The Quarterly journal of science and the arts”. The Quarterly Journal of Science and the Arts. Royal Institution of Great Britain. 5: 338. 1818. Архивирано из оригинала 13. 3. 2021. г. Приступљено 5. 10. 2010.
- ^ „Timeline science and engineering”. DiracDelta Science & Engineering Encyclopedia. Архивирано из оригинала 5. 12. 2008. г. Приступљено 18. 9. 2008.
- ^ Brande, William Thomas; MacNeven, William James (1821). A manual of chemistry. Long. стр. 191. Приступљено 8. 10. 2010.
- ^ Bunsen, R. (1855). „Darstellung des Lithiums” [Preparation of lithium]. Annalen der Chemie und Pharmacie. 94: 107—111. doi:10.1002/jlac.18550940112. Архивирано из оригинала 6. 11. 2018. г. Приступљено 13. 8. 2015.
- ^ Green, Thomas (11. 6. 2006). „Analysis of the Element Lithium”. echeat. Архивирано из оригинала 21. 4. 2012. г.
- ^ Garrett, Donald E. (5. 4. 2004). Handbook of Lithium and Natural Calcium Chloride. Elsevier. стр. 99. ISBN 978-0-08-047290-4. Архивирано из оригинала 3. 12. 2016. г.
- ^ Elschenbroich, C. (2009). Organometallchemie (6 изд.). Leipzig: Teubner B.G. Gmbh. стр. 16. ISBN 9783835192232.
- ^ а б в Kogel, Jessica Elzea (2006). „Lithium”. Industrial minerals & rocks: commodities, markets, and uses. Littleton, Colo.: Society for Mining, Metallurgy, and Exploration. стр. 599. ISBN 978-0-87335-233-8. Архивирано из оригинала 7. 11. 2020. г. Приступљено 6. 11. 2020.
- ^ United States Geological Survey: Minerals Yearbook 2007: Lithium. (PDF), 2007.
- ^ Shorter, Edward (јун 2009). „The history of lithium therapy”. Bipolar Disorders. 11 (Suppl 2): 4—9. ISSN 1398-5647. PMC 3712976
 . PMID 19538681. doi:10.1111/j.1399-5618.2009.00706.x.
. PMID 19538681. doi:10.1111/j.1399-5618.2009.00706.x.
- ^ а б Ober, Joyce A. (1994). „Commodity Report 1994: Lithium” (PDF). United States Geological Survey. Архивирано (PDF) из оригинала 9. 6. 2010. г. Приступљено 3. 11. 2010.
- ^ Deberitz, Jürgen; Boche, Gernot (2003). „Lithium und seine Verbindungen - Industrielle, medizinische und wissenschaftliche Bedeutung”. Chemie in unserer Zeit. 37 (4): 258—266. doi:10.1002/ciuz.200300264.
- ^ Bauer, Richard (1985). „Lithium - wie es nicht im Lehrbuch steht”. Chemie in unserer Zeit. 19 (5): 167—173. doi:10.1002/ciuz.19850190505.
- ^ Ober, Joyce A. (1994). „Minerals Yearbook 2007: Lithium” (PDF). United States Geological Survey. Архивирано (PDF) из оригинала 17. 7. 2010. г. Приступљено 3. 11. 2010.
- ^ McKetta, John J. (18. 7. 2007). Encyclopedia of Chemical Processing and Design: Volume 28 – Lactic Acid to Magnesium Supply-Demand Relationships. M. Dekker. ISBN 978-0-8247-2478-8. Архивирано из оригинала 28. 5. 2013. г.
- ^ Overland, Indra (2019-03-01). „The geopolitics of renewable energy: Debunking four emerging myths” (PDF). Energy Research & Social Science. 49: 36—40. Bibcode:2019ERSS...49...36O. ISSN 2214-6296. doi:10.1016/j.erss.2018.10.018
 . Архивирано (PDF) из оригинала 13. 3. 2021. г. Приступљено 25. 8. 2019.
. Архивирано (PDF) из оригинала 13. 3. 2021. г. Приступљено 25. 8. 2019.
- ^ Krebs, Robert E. (2006). The history and use of our earth's chemical elements: a reference guide. Greenwood Publishing Group. стр. 47. ISBN 978-0-313-33438-2. Архивирано из оригинала 4. 8. 2016. г.
- ^ Institute, American Geological; Union, American Geophysical; Society, Geochemical (1. 1. 1994). „Geochemistry international”. Google Books. 31 (1–4): 115. Архивирано из оригинала 4. 6. 2016. г.
- ^ а б в г Greenwood, Norman N.; Earnshaw, A. (1984). Chemistry of the Elements. Oxford: Pergamon. стр. 97—99. ISBN 0-08-022057-6. doi:10.1002/crat.2170200510.
- ^ Beckford, Floyd. „University of Lyon course online (powerpoint) slideshow”. Архивирано из оригинала 4. 11. 2005. г. Приступљено 27. 7. 2008. „definitions:Slides 8–10 (Chapter 14)”
- ^ Sevov, S.C., Zintl Phases in Intermetallic Compounds, Principles and Practice: Progress, Westbrook, J.H.; *Freisher, R.L.: Eds.; John Wiley & Sons. Ltd., Chichester, England, 2002, pp. 113-132 Slavi Chapter
- ^ Zintl, E; Goubeau, J; Dullenkopf, W (1931). „Metals and alloys. I. Salt-like compounds and intermetallic phases of sodium in liquid ammonia.”. Z. Phys. Chem. A (154): 1—46.
- ^ Diehl, Lothar; Khodadadeh, Keyumarss; Kummer, Dieter; Strähle, Joachim (октобар 1976). „Anorganische Polyederverbindungen, III. Zintl's "Polyanionige Salze"︁: Darstellung und Eigenschaften der kristallinen Verbindungen [Na4·7 en]Sn9, [Na4·5 en]Ge9 und [Na3·4 en]Sb7 und ihrer Lösungen Die Kristallstruktur von [Na4·7 en]Sn9”. Anorganische Chemie. 109 (10): 3404—3418. doi:10.1002/cber.19761091018 — преко Chemistry Europe.
- ^ Sapse, Anne-Marie; von R. Schleyer, Paul (1995). Lithium chemistry: a theoretical and experimental overview. Wiley-IEEE. стр. 3—40. ISBN 978-0-471-54930-7. Архивирано из оригинала 31. 7. 2016. г.
- ^ Nichols, Michael A.; Williard, Paul G. (1993-02-01). „Solid-state structures of n-butyllithium-TMEDA, -THF, and -DME complexes”. Journal of the American Chemical Society. 115 (4): 1568—1572. ISSN 0002-7863. doi:10.1021/ja00057a050.
- ^ C., Mehrotra, R. (2009). Organometallic chemistry: a unified approach. [Place of publication not identified]: New Age International Pvt. ISBN 978-81-224-1258-1. OCLC 946063142.
- ^ а б в г д ђ е ж з Stey, Thomas; Stalke, Dietmar (2009). „Lead structures in lithium organic chemistry”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0298.
- ^ а б в г д ђ е ж з и Reich, Hans J. (2013). „Role of Organolithium Aggregates and Mixed Aggregates in Organolithium Mechanisms”. Chemical Reviews. 113 (9): 7130—7178. PMID 23941648. doi:10.1021/cr400187u.
- ^ а б в г д ђ е ж з и Strohmann, C; et al. (2009). „Structure Formation Principles and Reactivity of Organolithium Compounds.” (PDF). Chem. Eur. J. 15 (14): 3320—3334. PMID 19260001. doi:10.1002/chem.200900041.
- ^ Zabicky, Jacob (2009). „Analytical aspects of organolithium compounds”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0304.
- ^ а б Jemmis, E.D.; Gopakumar, G. (2009). „Theoretical studies in organolithium chemistry”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0297.
- ^ а б Streiwieser, A. (2009). „Perspectives on Computational Organic Chemistry”. J. Org. Chem. 74 (12): 4433—4446. PMC 2728082
 . PMID 19518150. doi:10.1021/jo900497s.
. PMID 19518150. doi:10.1021/jo900497s.
- ^ а б Bickelhaupt, F. M.; et al. (2006). „Covalency in Highly Polar Bonds. Structure and Bonding of Methylalkalimetal Oligomers (CH3M)n (M = Li−Rb; n = 1, 4)”. J. Chem. Theory Comput. 2 (4): 965—980. PMID 26633056. doi:10.1021/ct050333s.
- ^ Weiss, Erwin (новембар 1993). „Structures of Organo Alkali Metal Complexes and Related Compounds”. Angewandte Chemie International Edition in English (на језику: енглески). 32 (11): 1501—1523. ISSN 0570-0833. doi:10.1002/anie.199315013.
- ^ Fraenkel, G.; Qiu, Fayang (1996). „Observation of a Partially Delocalized Allylic Lithium and the Dynamics of Its 1,3 Lithium Sigmatropic Shift”. J. Am. Chem. Soc. 118 (24): 5828—5829. doi:10.1021/ja960440j.
- ^ Fraenkel. G; et al. (1995). „The carbon-lithium bond in monomeric arllithium: Dynamics of exchange, relaxation and rotation”. J. Am. Chem. Soc. 117 (23): 6300—6307. doi:10.1021/ja00128a020.
- ^ Power, P.P; Hope H. (1983). „Isolation and crystal structures of the halide-free and halide-rich phenyllithium etherate complexes [(PhLi.Et2O)4] and [(PhLi.Et2O)3.LiBr].”. Journal of the American Chemical Society. 105 (16): 5320—5324. doi:10.1021/ja00354a022.
- ^ а б Williard, P. G.; Salvino, J. M. (1993). „Synthesis, isolation, and structure of an LDA-THF complex”. Journal of Organic Chemistry. 58 (1): 1—3. doi:10.1021/jo00053a001.
- ^ Hilmersson, Goran; Granander, Johan (2009). „Structure and dynamics of chiral lithium amides”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0342.
- ^ а б Collum, D.B.; et al. (2007). „Lithium Diisopropylamide: Solution Kinetics and Implications for Organic Synthesis”. Angew. Chem. Int. Ed. 49 (17): 3002—3017. PMID 17387670. doi:10.1002/anie.200603038.
- ^ Sekiguchi, Akira.; et al. (2000). „Lithiosilanes and their application to the synthesis of polysilane dendrimers”. Coord. Chem. Rev. 210: 11—45. doi:10.1016/S0010-8545(00)00315-5.
- ^ Collum, D. B.; et al. (2008). „Solution Structures of Lithium Enolates, Phenolates, Carboxylates, and Alkoxides in the Presence of N,N,N′,N′-Tetramethylethylenediamine: A Prevalence of Cyclic Dimers”. J. Org. Chem. 73 (19): 7743—7747. PMC 2636848
 . PMID 18781812. doi:10.1021/jo801532d.
. PMID 18781812. doi:10.1021/jo801532d.
- ^ Reich, H. J.; et al. (1998). „Aggregation and reactivity of phenyllithium solutions”. J. Am. Chem. Soc. 120 (29): 7201—7210. doi:10.1021/ja980684z.
- ^ McGarrity, J. F.; Ogle, C.A. (1985). „High-field proton NMR study of the aggregation and complexation of n-butyllithium in tetrahydrofuran”. J. Am. Chem. Soc. 107 (7): 1805—1810. doi:10.1021/ja00293a001.
- ^ а б Reich, H. J. (2012). „What's going on with these lithium reagents”. J. Org. Chem. 77 (13): 5471—5491. PMID 22594379. doi:10.1021/jo3005155.
- ^ Wardell, J.L. (1982). „Chapter 2”. Ур.: Wilinson, G.; Stone, F. G. A.; Abel, E. W. Comprehensive Organometallic Chemistry, Vol. 1 (1st изд.). New York: Pergamon. ISBN 978-0080406084.
- ^ Strohmann, C.; Gessner, V.H. (2008). „Crystal Structures of n-BuLi Adducts with (R,R)-TMCDA and the Consequences for the Deprotonation of Benzene”. J. Am. Chem. Soc. 130 (35): 11719—11725. PMID 18686951. doi:10.1021/ja8017187.
- ^ Collum, D. B.; et al. (2007). „Lithium Diisopropylamide: Solution Kinetics and Implications for Organic Synthesis”. Angew. Chem. Int. Ed. 46 (17): 3002—3017. PMID 17387670. doi:10.1002/anie.200603038.
- ^ а б Chalk, A.J; Hoogeboom, T.J (1968). „Ring metalation of toluene by butyllithium in the presence of N,N,N′,N′-tetramethylethylenediamine”. J. Organomet. Chem. 11: 615—618. doi:10.1016/0022-328x(68)80091-9.
- ^ а б Reich, H.J; Green, D.P (1989). „Spectroscopic and Reactivity Studies of Lithium Reagent - HMPA Complexes”. Journal of the American Chemical Society. 111 (23): 8729—8731. doi:10.1021/ja00205a030.
- ^ Williard, P.G; Nichols, M.A (1993). „Solid-state structures of n-butyllithium-TMEDA, -THF, and -DME complexes”. Journal of the American Chemical Society. 115 (4): 1568—1572. doi:10.1021/ja00057a050.
- ^ Collum, D.B. (1992). „Is N,N,N,N-Tetramethylethylenediamine a Good Ligand for Lithium?”. Acc. Chem. Res. 25 (10): 448—454. doi:10.1021/ar00022a003.
- ^ Bernstein, M.P.; Collum, D.B. (1993). „Solvent- and substrate-dependent rates of imine metalations by lithium diisopropylamide: understanding the mechanisms underlying krel”. J. Am. Chem. Soc. 115 (18): 8008—8010. doi:10.1021/ja00071a011.
- ^ Seebach, D (1988). „Structure and Reactivity of Lithium Enolates. From Pinacolone to Selective C-Alkylations of Peptides. Difficulties and Opportunities Afforded by Complex Structures.” (PDF). Angew. Chem. Int. Ed. 27 (12): 1624—1654. doi:10.1002/anie.198816241.
- ^ а б в Fananas, Francisco; Sanz, Roberto (2009). „Intramolecular carbolithiation reactions”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0341.
- ^ Heinz-Dieter Brandt, Wolfgang Nentwig1, Nicola Rooney, Ronald T. LaFlair, Ute U. Wolf, John Duffy, Judit E. Puskas, Gabor Kaszas, Mark Drewitt, Stephan Glander "Rubber, 5. Solution Rubbers" in Ullmann's Encyclopedia of Industrial Chemistry, 2011, Wiley-VCH, Weinheim. doi:10.1002/14356007.o23_o02
- ^ Baskaran, D.; Müller, A.H. (2010). „Anionic Vinyl Polymerization”. Controlled and living polymerizations: From mechanisms to applications. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. ISBN 9783527629091. doi:10.1002/9783527629091.ch1.
- ^ Bailey, W.F.; et al. (1989). „Preparation and facile cyclization of 5-alkyn-1-yllithiums”. Tetrahedron Lett. 30 (30): 3901—3904. doi:10.1016/S0040-4039(00)99279-7.
- ^ а б в г д ђ е Carey, Francis A. (2007). „Organometallic compounds of Group I and II metals”. Advanced Organic Chemistry: Reaction and Synthesis Pt. B (Kindle изд.). Springer. ISBN 978-0-387-44899-2.
- ^ Ashby, E.C.; Noding, S.R. (1979). „The effects of added salts on the stereoselectivity and rate of organometallic compound addition to ketones”. J. Org. Chem. 44 (24): 4371—4377. doi:10.1021/jo01338a026.
- ^ Yamataka, Hiroshi (2009). „Addition of organolithium reagents to double bonds”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0310.
- ^ Landa, S.; et al. (1967). „Über adamantan und dessen derivate IX. In 2-stellung substituierte derivate”. Collection of Czechoslovak Chemical Communications. 72 (2): 570—575. doi:10.1135/cccc19670570.
- ^ Rubottom, G.M.; Kim, C (1983). „Preparation of methyl ketones by the sequential treatment of carboxylic acids with methyllithium and chlorotrimethylsilane”. J. Org. Chem. 48 (9): 1550—1552. doi:10.1021/jo00157a038.
- ^ Zadel, G.; Breitmaier, E. (1992). „A One-Pot Synthesis of Ketones and Aldehydes from Carbon Dioxide and Organolithium Compounds”. Angew. Chem. Int. Ed. 31 (8): 1035—1036. doi:10.1002/anie.199210351.
- ^ Ronald, R.C. (1975). „Methoxymethyl ethers. An activating group for rapid and regioselective metalation”. Tetrahedron Lett. 16 (46): 3973—3974. doi:10.1016/S0040-4039(00)91212-7.
- ^ Hunt, D.A. (1989). „Michael addition of organolithium compounds. A Review”. Org. Prep. Proc. Int. 21 (6): 705—749. doi:10.1080/00304948909356219.
- ^ Reich, H. J.; Sikorski, W. H. (1999). „Regioselectivity of Addition of Organolithium Reagents to Enones: The Role of HMPA”. J. Org. Chem. 64 (1): 14—15. PMID 11674078. doi:10.1021/jo981765g.
- ^ Collum, D.B.; et al. (2001). „NMR Spectroscopic Investigations of Mixed Aggregates Underlying Highly Enantioselective 1,2-Additions of Lithium Cyclopropylacetylide to Quinazolinones”. J. Am. Chem. Soc. 123 (37): 9135—9143. PMID 11552822. doi:10.1021/ja0105616.
- ^ Sommmer, L.H.; Korte, W. D. (1970). „Stereospecific coupling reactions between organolithium reagents and secondary halides”. J. Org. Chem. 35: 22—25. doi:10.1021/jo00826a006.
- ^ а б в г Organolithium Reagents Reich, H.J. 2002 https://organicchemistrydata.org/hansreich/resources/organolithium/organolithium_data/orgli-primer.pdf
- ^ а б The Preparation of Organolithium Reagents and Intermediates Leroux.F., Schlosser. M., Zohar. E., Marek. I., Wiley, New York. 2004. ISBN 978-0-470-84339-0
- ^ а б Hoppe, Dieter; Christoph, Guido (2009). „Asymmetric deprotonation with alkyllithium– (−)-sparteine”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0313.
- ^ Clayden, Jonathan (2009). „Directed metallization of aromatic compounds”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0306.
- ^ Schlosser, M (1988). „Superbases for organic synthesis”. Pure Appl. Chem. 60 (11): 1627—1634. doi:10.1351/pac198860111627
 .
.
- ^ Roush, W.R.; et al. (1988). „Enantioselective synthesis using diisopropyl tartrate modified (E)- and (Z)-crotylboronates: Reactions with achiral aldehydes”. Tetrahedron Lett. 29 (44): 5579—5582. doi:10.1016/S0040-4039(00)80816-3.
- ^ Park, Y.S.; et al. (1996). „(−)-Sparteine-Mediated α-Lithiation of N-Boc-N-(p-methoxyphenyl)benzylamine: Enantioselective Syntheses of (S) and (R) Mono- and Disubstituted N-Boc-benzylamines”. J. Am. Chem. Soc. 118 (15): 3757—3758. doi:10.1021/ja9538804.
- ^ а б в г Valnot, Jean-Yves; Maddaluno, Jacques (2009). „Aspects of the synthesis, structure and reactivity of lithium enolates”. PATAI'S Chemistry of Functional Groups. John Wiley & Sons, Ltd. ISBN 9780470682531. doi:10.1002/9780470682531.pat0345.
- ^ Ireland. R. E.; et al. (1976). „The ester enolate Claisen rearrangement. Stereochemical control through stereoselective enolate formation”. J. Am. Chem. Soc. 98 (10): 2868—2877. doi:10.1021/ja00426a033.
- ^ Parham, W.P.; Bradsher, C.K. (1982). „Aromatic organolithium reagents bearing electrophilic groups. Preparation by halogen-lithium exchange”. Acc. Chem. Res. 15 (10): 300—305. doi:10.1021/ar00082a001.
- ^ Corey, E.J.; Wollenberg, R.H. (1975). „Useful new organometallic reagents for the synthesis of allylic alcohols by nucleophilic vinylation”. J. Org. Chem. 40 (15): 2265—2266. doi:10.1021/jo00903a037.
- ^ Reeder, M.R.; et al. (2003). „An Improved Method for the Palladium Cross-Coupling Reaction of Oxazol-2-ylzinc Derivatives with Aryl Bromides”. Org. Process Res. Dev. 7 (5): 696—699. doi:10.1021/op034059c.
- ^ Nakamura, E.; et al. (1997). „Reaction Pathway of the Conjugate Addition of Lithium Organocuprate Clusters to Acrolein”. J. Am. Chem. Soc. 119 (21): 4900—4910. doi:10.1021/ja964209h.
- ^ "Organometallics in Organic Synthesis", Schlosser, M., Ed, Wiley: New York, 1994. ISBN 0-471-93637-5
- ^ Si-Fodil, M.; et al. (1998). „Obtention of 2,2-(diethoxy) vinyl lithium and 2-methyl-4-ethoxy butadienyl lithium by arene-catalysed lithiation of the corresponding chloro derivatives. Synthetic applications”. Tetrahedron Lett. 39 (49): 8975—8978. doi:10.1016/S0040-4039(98)02031-0.
- ^ Cohen, T; Bhupathy. M (1989). „Organoalkali compounds by radical anion induced reductive metalation of phenyl thioethers”. Acc. Chem. Res. 22 (4): 152—161. doi:10.1021/ar00160a006.
- ^ а б Snieckus, V (1990). „Directed ortho metalation. Tertiary amide and O-carbamate directors in synthetic strategies for polysubstituted aromatics”. Chem. Rev. 90 (6): 879—933. doi:10.1021/cr00104a001.
- ^ Schwindeman, James A.; Woltermann, Chris J.; Letchford, Robert J. (2002). „Safe handling of organolithium compounds in the laboratory”. Chemical Health and Safety. 9 (3): 6—11. ISSN 1074-9098. doi:10.1016/S1074-9098(02)00295-2.
- ^ Gellert, H; Ziegler, K. (1950). „Organoalkali compounds. XVI. The thermal stability of lithium alkyls.”. Liebigs Ann. Chem. 567: 179—185. doi:10.1002/jlac.19505670110.
- ^ Juaristi, E.; Martínez-Richa, A.; García-Rivera, A.; Cruz-Sánchez, J. S. (1983). „Use of 4-Biphenylmethanol, 4-Biphenylacetic Acid and 4-Biphenylcarboxylic Acid/Triphenylmethane as Indicators in the Titration of Lithium Alkyls. Study of the Dianion of 4-Biphenylmethanol”. The Journal of Organic Chemistry. 48 (15): 2603—2606. doi:10.1021/jo00163a038.
- ^ „Titrating Soluble RM, R2NM and ROM Reagents” (PDF). Приступљено 2014-06-04.
- ^ „Methods for Standardizing Alkyllithium Reagents (literature through 2006)” (PDF). Приступљено 2014-06-04.
- ^ Stanetty, P.; Koller, H.; Mihovilovic, M. (1992). „Directed Ortho-Lithiation of Phenylcarbamic Acid 1,l-Dimethylethyl Ester (N-Boc-aniline). Revision and Improvements”. J. Org. Chem. 57 (25): 6833—6837. doi:10.1021/jo00051a030.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (II изд.). Oxford: Butterworth-Heinemann. стр. 73. ISBN 0080379419.
- ^ „India finds 5.9 million tonnes lithium deposits in Jammu and Kashmir”. Hindustan Times. 10. 2. 2023. Архивирано из оригинала 10. 2. 2023. г. Приступљено 11. 2. 2023.
- ^ „5.9 million tonnes Lithium deposits found in J&K: Why it's important”. The Times of India. 10. 2. 2023. Архивирано из оригинала 10. 2. 2023. г. Приступљено 11. 2. 2023.
- ^ Lithium na USGS Mineral Resources, 2009 (PDF).
- ^ SGU. Mineralmarknaden, Tema: Litium [in Swedish]. Publication by the Swedish Geological Survey; 2009. ISSN 0283-2038
- ^ Tarascon, J. M. (2010). „Is lithium the new gold?”. Nature Chemistry. 2 (6): 510. Bibcode:2010NatCh...2..510T. PMID 20489722. doi:10.1038/nchem.680
 .
.
- ^ Woody, Todd (19. 10. 2011). „Lithium: The New California Gold Rush”. Forbes. Архивирано из оригинала 19. 12. 2014. г.
- ^ Houston, J.; Butcher, A.; Ehren, P.; Evans, K.; Godfrey, L. (2011). „The Evaluation of Brine Prospects and the Requirement for Modifications to Filing Standards” (PDF). Economic Geology. 106 (7): 1225—1239. Bibcode:2011EcGeo.106.1225H. doi:10.2113/econgeo.106.7.1225. Архивирано (PDF) из оригинала 20. 7. 2018. г. Приступљено 28. 6. 2019.
- ^ Warr, L.N. (2021). „IMA–CNMNC approved mineral symbols”. Mineralogical Magazine. 85 (3): 291—320. Bibcode:2021MinM...85..291W. S2CID 235729616. doi:10.1180/mgm.2021.43
 .
.
- ^ Schwartz, G. (1928). „The Black Hills Mineral Region”. American Mineralogist. 13: 56—63.
- ^ Robert Louis Bonewitz, 2005, Rock and Gem, London, Dorling Kindersley
- ^ „Greenbushes Lithium Mine”. Golden Dragon Capital (на језику: енглески). Архивирано из оригинала 19. 1. 2019. г. Приступљено 18. 1. 2019.
- ^ Anlauf, Axel (2016). „Greening the imperial mode of living? Socio- ecological (in)justice, electromobility, and lithium mining in Argentina”. Ур.: Pichler, Melanie; Staritz, Cornelia; Küblböck, Karin; Plank, Christina; Raza, Werner; Ruiz Peyré, Fernando. Fairness and Justice in Natural Resource Politics.
- ^ López Steinmetz, Romina Lucrecia; Salvi, Stefano (2021). „Brine grades in Andean salars: When basin size matters A review of the Lithium Triangle”. Earth-Science Reviews. 217. Bibcode:2021ESRv..21703615L. S2CID 233846211. doi:10.1016/j.earscirev.2021.103615.
- ^ Halpern, Abel (30. 1. 2014). „The Lithium Triangle”. Latin Trade. Архивирано из оригинала
 10. 6. 2018. г.
10. 6. 2018. г.
- ^ а б Romero Simon (2. 2. 2009). „In Bolivia, a Tight Grip on the Next Big Resource”. The New York Times. Архивирано из оригинала 1. 7. 2017. г.
- ^ „USGS Mineral Commodities Summaries 2009” (PDF). USGS. Архивирано (PDF) из оригинала 14. 6. 2010. г.
- ^ Dube, Ryan (11. 8. 2022). „The Place With the Most Lithium Is Blowing the Electric-Car Revolution”. The Wall Street Journal (на језику: енглески). CCLXXX (35). стр. A1, A8. ISSN 1042-9840. Архивирано из оригинала 10. 8. 2022. г. Приступљено 11. 8. 2022.
- ^ а б в г д ђ Cabello, J (2022). „Reserves, resources and lithium exploration in the salt flats of northern Chile”. Andean Geology. 49 (2): 297—306. doi:10.5027/andgeoV49n2-3444]. Архивирано из оригинала 12. 12. 2022. г. Приступљено 3. 7. 2022.
- ^ Bernick, Michael (12. 12. 2023). „The Jobs Perplex Of The Lithium Valley”. Forbes (на језику: енглески). Архивирано из оригинала 5. 2. 2024. г. Приступљено 2024-02-05.
- ^ „This Congo project could supply the world with lithium”. MiningDotCom. 10. 12. 2018. Архивирано из оригинала 14. 4. 2021. г. Приступљено 26. 3. 2021.
- ^ „Plateau Energy Metals Peru unit finds large lithium resources”. Reuters. 16. 7. 2018. Архивирано из оригинала 26. 7. 2018. г.
- ^ Matthis, Simon (17. 3. 2021). „Australia grants MPS for Core Lithium's Finniss lithium project”. MiningMetalNews. Архивирано из оригинала 13. 10. 2022. г. Приступљено 13. 10. 2022.
- ^ CORE Lithium : Finnis Lithium Архивирано 13 октобар 2022 на сајту Wayback Machine, retrieved 13 October 2022
- ^ „Finniss Lithium Project, Northern Territory, Australia”. Mining Technology. 13. 1. 2022. Архивирано из оригинала 13. 10. 2022. г. Приступљено 13. 10. 2022.
- ^ Daly, John C.K. (26. 4. 2013). „Researchers Have Stumbled On A Massive Lithium Mine That Could Meet All US Demand”. Business Insider. New York City, U.S.: OilPrice.com. Архивирано из оригинала 3. 5. 2013. г.
- ^ Benson, Tom (16. 8. 2016). „Lithium enrichment in intracontinental rhyolite magmas leads to Li deposits in caldera basins”. Nature Communications. 8 (1): 270. PMC 5559592
 . PMID 28814716. doi:10.1038/s41467-017-00234-y.
. PMID 28814716. doi:10.1038/s41467-017-00234-y.
- ^ Galliski, Miguel Ángel; Márquez-Zavalía, María Florencia; Roda-Robles, Encarnación; von Quadt, Albrecht (2022). „The Li-Bearing Pegmatites from the Pampean Pegmatite Province, Argentina: Metallogenesis and Resources”. Minerals. MDPI. 12 (7): 841. Bibcode:2022Mine...12..841G. doi:10.3390/min12070841
 .
.
- ^ „Polar Lithium awarded right to develop Russia's largest lithium deposit”. 9. 2. 2023. Архивирано из оригинала 22. 7. 2023. г. Приступљено 22. 7. 2023.
- ^ Parker, Ann. Mining Geothermal Resources Архивирано 17 септембар 2012 на сајту Wayback Machine. Lawrence Livermore National Laboratory
- ^ Patel, P. (16 November 2011) Startup to Capture Lithium from Geothermal Plants Архивирано 21 јул 2022 на сајту Wayback Machine. technologyreview.com
- ^ Ober, Joyce A. „Lithium” (PDF). United States Geological Survey. стр. 77—78. Архивирано (PDF) из оригинала 11. 7. 2007. г. Приступљено 19. 8. 2007.
- ^ „SQM Announces New Lithium Prices – SANTIAGO, Chile”. PR Newswire. 30. 9. 2009. Архивирано из оригинала 30. 5. 2013. г.
- ^ а б Riseborough, Jesse. „IPad Boom Strains Lithium Supplies After Prices Triple”. Bloomberg BusinessWeek. Архивирано из оригинала 22. 6. 2012. г. Приступљено 1. 5. 2013.
- ^ „ISE Metal-quotes”. Архивирано из оригинала 9. 7. 2023. г. Приступљено 29. 9. 2022.
- ^ Thacker Pass Lithium Mine Project Final Environmental Impact Statement (PDF) (Технички извештај). Bureau of Land Management and the U.S. Fish and Wildlife Service. 4. 12. 2020. DOI-BLM-NV-W010-2020-0012-EIS. Приступљено 16. 3. 2021.
- ^ а б Patterson, Scott; Ramkumar, Amrith (9. 3. 2021). „America's Battery-Powered Car Hopes Ride on Lithium. One Producer Paves the Way”. The Wall Street Journal. Архивирано из оригинала 12. 3. 2021. г. Приступљено 13. 3. 2021.
- ^ Cafariello, Joseph (10. 3. 2014). „Lithium: A Long-Term Investment Buy Lithium!”. wealthdaily.com. Архивирано из оригинала 12. 6. 2018. г. Приступљено 2015-04-24.
- ^ Kaskey, Jack (16. 7. 2014). „Largest Lithium Deal Triggered by Smartphones and Teslas”. Bloomberg. Архивирано из оригинала 12. 6. 2018. г. Приступљено 2015-04-24.
- ^ Marcelo Azevedo; Nicolò Campagnol; Toralf Hagenbruch; Ken Hoffman; Ajay Lala; Oliver Ramsbottom (јун 2018). „Lithium and cobalt – a tale of two commodities”. McKinsey. стр. 9. Архивирано из оригинала 11. 12. 2019. г. Приступљено 29. 1. 2020.
- ^ Sun, Sen; Yu, Xiaoping; Li, Mingli; Duo, Ji; Guo, Yafei; Deng, Tianlong (2020-02-20). „Green recovery of lithium from geothermal water based on a novel lithium iron phosphate electrochemical technique”. Journal of Cleaner Production (на језику: енглески). 247: 119178. Bibcode:2020JCPro.24719178S. ISSN 0959-6526. S2CID 211445414. doi:10.1016/j.jclepro.2019.119178.
- ^ Chong Liu; Yanbin Li; Dingchang Lin; Po-Chun Hsu; Bofei Liu; Gangbin Yan; Tong Wu Yi Cui; Steven Chu (2020). „Lithium Extraction from Seawater through Pulsed Electrochemical Intercalation”. Joule. 4 (7): 1459—1469. Bibcode:2020Joule...4.1459L. S2CID 225527170. doi:10.1016/j.joule.2020.05.017.
- ^ Tsuyoshi Hoshino (2015). „Innovative lithium recovery technique from seawater by using world-first dialysis with a lithium ionic superconductor”. Desalination. 359: 59—63. Bibcode:2015Desal.359...59H. doi:10.1016/j.desal.2014.12.018
 .
.
- ^ Robert F. Service (13. 7. 2020). „Seawater could provide nearly unlimited amounts of critical battery material”. Science. Архивирано из оригинала 13. 1. 2021. г. Приступљено 26. 12. 2020.
- ^ а б Yang, Sixie; Zhang, Fan; Ding, Huaiping; He, Ping; Zhou, Haoshen (2018-09-19). „Lithium Metal Extraction from Seawater”. Joule (на језику: енглески). 2 (9): 1648—1651. Bibcode:2018Joule...2.1648Y. ISSN 2542-4351. S2CID 189702476. doi:10.1016/j.joule.2018.07.006. Архивирано из оригинала 19. 1. 2021. г. Приступљено 21. 10. 2020.
- ^ а б в Amui, Rachid (фебруар 2020). „Commodities At a Glance: Special issue on strategic battery raw materials” (PDF). United Nations Conference on Trade and Development. 13 (UNCTAD/DITC/COM/2019/5). Архивирано (PDF) из оригинала 3. 2. 2021. г. Приступљено 10. 2. 2021.
- ^ Application of Life-Cycle Assessment to Nanoscale Technology: Lithium-ion Batteries for Electric Vehicles (Извештај). Washington, DC: U.S. Environmental Protection Agency (EPA). 2013. EPA 744-R-12-001. Архивирано из оригинала 11. 7. 2017. г. Приступљено 24. 3. 2021.
- ^ „Can Nanotech Improve Li-ion Battery Performance”. Environmental Leader. 30. 5. 2013. Архивирано из оригинала 21. 8. 2016. г. Приступљено 3. 6. 2013.
- ^ Katwala, Amit. „The spiralling environmental cost of our lithium battery addiction”. Wired. Condé Nast Publications. Архивирано из оригинала 9. 2. 2021. г. Приступљено 10. 2. 2021.
- ^ Draper, Robert. „This metal is powering today's technology—at what price?”. National Geographic (February 2019). National Geographic Partners. Архивирано из оригинала
 18. 1. 2019. г. Приступљено 10. 2. 2021.
18. 1. 2019. г. Приступљено 10. 2. 2021.
- ^ а б „The Lithium Gold Rush: Inside the Race to Power Electric Vehicles”. The New York Times. 6. 5. 2021. Архивирано из оригинала 6. 5. 2021. г. Приступљено 6. 5. 2021.
- ^ Marchegiani Morgera Parks (21. 11. 2019). „Indigenous peoples'rights to natural resources in Argentina: the challenges of impact assessment, consent and fair andequitable benefit-sharing in cases of lithium mining”. The International Journal of Human Rights.
- ^ Price, Austin (лето 2021). „The Rush for White Gold”. Earth Island Journal. Архивирано из оригинала 29. 10. 2021. г. Приступљено 29. 10. 2021.
- ^ Chadwell, Jeri (21. 7. 2021). „Judge to decide on injunction request to halt work on Thacker Pass lithium mine”. This is Reno. Архивирано из оригинала 29. 10. 2021. г. Приступљено 12. 10. 2021.
- ^ „Thacker Pass Lithium mine approval draws around-the-clock protest”. Sierra Nevada Ally. 19. 1. 2021. Архивирано из оригинала 29. 10. 2021. г. Приступљено 16. 3. 2021.
- ^ O litijskim baterijama Архивирано на сајту Wayback Machine (24. јануар 2009) na stranici TU Graz (PDF).
- ^ The Theory and Practice of Mold Fluxes Used in Continuous Casting: A Compilation of Papers on Continuous Casting Fluxes Given at the 61st and 62nd Steelmaking Conference, Iron and Steel Society
- ^ Lu, Y. Q.; Zhang, G. D.; Jiang, M. F.; Liu, H. X.; Li, T. (2011). „Effects of Li2CO3 on Properties of Mould Flux for High Speed Continuous Casting”. Materials Science Forum. 675–677: 877—880. S2CID 136666669. doi:10.4028/www.scientific.net/MSF.675-677.877.
- ^ „Testing 1-2-3: Eliminating Veining Defects”, Modern Casting, јул 2014, Архивирано из оригинала 2. 4. 2015. г., Приступљено 15. 3. 2015
- ^ Haupin, W. (1987), Mamantov, Gleb; Marassi, Roberto, ур., „Chemical and Physical Properties of the Hall-Héroult Electrolyte”, Molten Salt Chemistry: An Introduction and Selected Applications, Springer, стр. 449
- ^ Garrett, Donald E. (2004-04-05). Handbook of Lithium and Natural Calcium Chloride (на језику: енглески). Academic Press. стр. 200. ISBN 978-0-08-047290-4. Архивирано из оригинала 3. 12. 2016. г.
- ^ Prasad, N. Eswara; Gokhale, Amol; Wanhill, R. J. H. (2013-09-20). Aluminum-Lithium Alloys: Processing, Properties, and Applications (на језику: енглески). Butterworth-Heinemann. ISBN 978-0-12-401679-8. Архивирано из оригинала 1. 1. 2021. г. Приступљено 6. 11. 2020.
- ^ Davis, Joseph R. ASM International. Handbook Committee (1993). Aluminum and aluminum alloys. ASM International. стр. 121—. ISBN 978-0-87170-496-2. Архивирано из оригинала 28. 5. 2013. г. Приступљено 16. 5. 2011.
- ^ Karki, Khim; Epstein, Eric; Cho, Jeong-Hyun; Jia, Zheng; Li, Teng; Picraux, S. Tom; Wang, Chunsheng; Cumings, John (2012). „Lithium-Assisted Electrochemical Welding in Silicon Nanowire Battery Electrodes” (PDF). Nano Letters. 12 (3): 1392—7. Bibcode:2012NanoL..12.1392K. PMID 22339576. doi:10.1021/nl204063u. Архивирано (PDF) из оригинала 10. 8. 2017. г.
- ^ „Lithium” (PDF). USGS. Архивирано (PDF) из оригинала 1. 11. 2020. г. Приступљено 15. 11. 2020.
- ^ „Lithium” (PDF). 2016. Архивирано (PDF) из оригинала 30. 11. 2016. г. Приступљено 29. 11. 2016 — преко US Geological Survey (USGS).
- ^ „Fmclithium.com” (PDF). www.fmclithium.com. Архивирано из оригинала (PDF) 7. 9. 2014. г.
- ^ Clark, Jim (2005). „Some Compounds of the Group 1 Elements”. chemguide.co.uk. Архивирано из оригинала 27. 6. 2013. г. Приступљено 8. 8. 2013.
- ^ „Disposable Batteries - Choosing between Alkaline and Lithium Disposable Batteries”. Batteryreview.org. Архивирано из оригинала 6. 1. 2014. г. Приступљено 10. 10. 2013.
- ^ „Battery Anodes > Batteries & Fuel Cells > Research > The Energy Materials Center at Cornell”. Emc2.cornell.edu. Архивирано из оригинала 22. 12. 2013. г. Приступљено 10. 10. 2013.
- ^ Totten, George E.; Westbrook, Steven R.; Shah, Rajesh J. (2003). Fuels and lubricants handbook: technology, properties, performance, and testing. 1. ASTM International. стр. 559. ISBN 978-0-8031-2096-9. Архивирано из оригинала 23. 7. 2016. г.
- ^ Rand, Salvatore J. (2003). Significance of tests for petroleum products. ASTM International. стр. 150—152. ISBN 978-0-8031-2097-6. Архивирано из оригинала 31. 7. 2016. г.
- ^ Koch, Ernst-Christian (2004). „Special Materials in Pyrotechnics: III. Application of Lithium and its Compounds in Energetic Systems”. Propellants, Explosives, Pyrotechnics. 29 (2): 67—80. doi:10.1002/prep.200400032.
- ^ Wiberg, Egon; Wiberg, Nils and Holleman, Arnold Frederick (2001) Wiberg, Egon; Wiberg, Nils (2001). Inorganic Chemistry. Academic Press. ISBN 978-0-12-352651-9. Архивирано из оригинала 19. 1. 2023. г. Приступљено 22. 2. 2016., Academic Press. ISBN 0-12-352651-5, p. 1089
- ^ Mulloth, L.M.; Finn, J.E. (2005). „Air Quality Systems for Related Enclosed Spaces: Spacecraft Air”. The Handbook of Environmental Chemistry. 4H. стр. 383—404. ISBN 978-3-540-25019-7. doi:10.1007/b107253.
- ^ „Application of lithium chemicals for air regeneration of manned spacecraft” (PDF). Lithium Corporation of America & Aerospace Medical Research Laboratories. 1965. Архивирано из оригинала (PDF) 7. 10. 2012. г.
- ^ Markowitz, M. M.; Boryta, D. A.; Stewart, Harvey (1964). „Lithium Perchlorate Oxygen Candle. Pyrochemical Source of Pure Oxygen”. Industrial & Engineering Chemistry Product Research and Development. 3 (4): 321—30. doi:10.1021/i360012a016.
- ^ Hobbs, Philip C. D. (2009). Building Electro-Optical Systems: Making It All Work. John Wiley and Sons. стр. 149. ISBN 978-0-470-40229-0. Архивирано из оригинала 23. 6. 2016. г.
- ^ Point Defects in Lithium Fluoride Films Induced by Gamma Irradiation. Proceedings of the 7th International Conference on Advanced Technology & Particle Physics: (ICATPP-7): Villa Olmo, Como, Italy. 2001. World Scientific. 2002. стр. 819. ISBN 978-981-238-180-4. Архивирано из оригинала 6. 6. 2016. г.
- ^ Sinton, William M. (1962). „Infrared Spectroscopy of Planets and Stars”. Applied Optics. 1 (2): 105. Bibcode:1962ApOpt...1..105S. doi:10.1364/AO.1.000105.
- ^ „You've got the power: the evolution of batteries and the future of fuel cells” (PDF). Toshiba. Архивирано (PDF) из оригинала 17. 7. 2011. г. Приступљено 17. 5. 2009.
- ^ „Organometallics”. IHS Chemicals. фебруар 2012. Архивирано из оригинала 7. 7. 2012. г. Приступљено 2. 1. 2012.
- ^ Yurkovetskii, A. V.; Kofman, V. L.; Makovetskii, K. L. (2005). „Polymerization of 1,2-dimethylenecyclobutane by organolithium initiators”. Russian Chemical Bulletin. 37 (9): 1782—1784. S2CID 94017312. doi:10.1007/BF00962487.
- ^ Quirk, Roderic P.; Cheng, Pao Luo (1986). „Functionalization of polymeric organolithium compounds. Amination of poly(styryl)lithium”. Macromolecules. 19 (5): 1291—1294. Bibcode:1986MaMol..19.1291Q. doi:10.1021/ma00159a001.
- ^ Stone, F. G. A.; West, Robert (1980). Advances in organometallic chemistry. Academic Press. стр. 55. ISBN 978-0-12-031118-7. Архивирано из оригинала 13. 3. 2021. г. Приступљено 6. 11. 2020.
- ^ Bansal, Raj K. (1996). Synthetic approaches in organic chemistry. Jones & Bartlett Learning. стр. 192. ISBN 978-0-7637-0665-4. Архивирано из оригинала 18. 6. 2016. г.
- ^ „An Experimental Investigation of a Lithium Aluminum Hydride–Hydrogen Peroxide Hybrid Rocket” (PDF). 28. 6. 2003. Архивирано из оригинала (PDF) 28. 6. 2003. г.
- ^ Hughes, T.G.; Smith, R.B.; Kiely, D.H. (1983). „Stored Chemical Energy Propulsion System for Underwater Applications”. Journal of Energy. 7 (2): 128—133. Bibcode:1983JEner...7..128H. doi:10.2514/3.62644.
- ^ Emsley, John (2011). Nature's Building Blocks.
- ^ Makhijani, Arjun; Yih, Katherine (2000). Nuclear Wastelands: A Global Guide to Nuclear Weapons Production and Its Health and Environmental Effects. MIT Press. стр. 59—60. ISBN 978-0-262-63204-1. Архивирано из оригинала 13. 6. 2016. г.
- ^ National Research Council (U.S.). Committee on Separations Technology and Transmutation Systems (1996). Nuclear wastes: technologies for separations and transmutation. National Academies Press. стр. 278. ISBN 978-0-309-05226-9. Архивирано из оригинала 13. 6. 2016. г.
- ^ Barnaby, Frank (1993). How nuclear weapons spread: nuclear-weapon proliferation in the 1990s. Routledge. стр. 39. ISBN 978-0-415-07674-6. Архивирано из оригинала 9. 6. 2016. г.
- ^ Baesjr, C. (1974). „The chemistry and thermodynamics of molten salt reactor fuels”. Journal of Nuclear Materials. 51 (1): 149—162. Bibcode:1974JNuM...51..149B. OSTI 4470742. doi:10.1016/0022-3115(74)90124-X. Архивирано из оригинала 13. 3. 2021. г. Приступљено 28. 6. 2019.
- ^ Agarwal, Arun (2008). Nobel Prize Winners in Physics. APH Publishing. стр. 139. ISBN 978-81-7648-743-6. Архивирано из оригинала 29. 6. 2016. г.
- ^ "'Splitting the Atom': Cockcroft and Walton, 1932: 9. Rays or Particles?" Архивирано 2 септембар 2012 на сајту Wayback Machine Department of Physics, University of Cambridge
- ^ „With lithium, more is definitely better”. phys.org.
- ^ „Integrating hot cores and cool edges in fusion reactors”. phys.org. Архивирано из оригинала 29. 4. 2023. г. Приступљено 23. 4. 2023.
- ^ Elements, American. „Lithium-7 Metal Isotope”. American Elements. Архивирано из оригинала 18. 8. 2019. г.
- ^ а б Wald, Matthew L. (8. 10. 2013). „Report Says a Shortage of Nuclear Ingredient Looms”. The New York Times. Архивирано из оригинала 1. 7. 2017. г.
- ^ а б Kean, Sam (2011). The Disappearing Spoon
 .
.
- ^ Yacobi S; Ornoy A (2008). „Is lithium a real teratogen? What can we conclude from the prospective versus retrospective studies? A review”. Isr J Psychiatry Relat Sci. 45 (2): 95—106. PMID 18982835.
- ^ Cade, J. (1949). „Lithium salts in the treatment of psychotic excitement”. Med. J. Australia. 36 (10): 349—352. PMC 2560740
 . PMID 18142718. doi:10.1080/j.1440-1614.1999.06241.x.
. PMID 18142718. doi:10.1080/j.1440-1614.1999.06241.x.
- ^ Schou, M. (2001). Lithiumbehandlung der manisch-depressiven Krankheit. Thieme. ISBN 978-3-13-593304-7.
- ^ „Lithium 265969”. Sigma-Aldrich. Архивирано из оригинала 13. 3. 2021. г. Приступљено 1. 10. 2018.
- ^ Technical data for Lithium Архивирано 23 март 2015 на сајту Wayback Machine. periodictable.com
- ^ Furr, A. K. (2000). CRC handbook of laboratory safety. Boca Raton: CRC Press. стр. 244—246. ISBN 978-0-8493-2523-6. Архивирано из оригинала 13. 3. 2021. г. Приступљено 6. 11. 2020.
Литература
[уреди | уреди извор]- Arblaster, John W. (2018). Selected Values of the Crystallographic Properties of Elements. Materials Park, Ohio: ASM International. ISBN 978-1-62708-155-9.
- Nörtershäuser, W.; Tiedemann, D.; Žáková, M.; Andjelkovic, Z.; Blaum, K.; Bissell, M. L.; Cazan, R.; Drake, G. W. F.; Geppert, Ch.; Kowalska, M.; Krämer, J.; Krieger, A.; Neugart, R.; Sánchez, R.; Schmidt-Kaler, F.; Yan, Z.-C.; Yordanov, D. T.; Zimmermann, C. (2009). „Nuclear Charge Radii of Be7,9,10 and the One-Neutron Halo Nucleus Be11”. Physical Review Letters. 102 (6): 062503. Bibcode:2009PhRvL.102f2503N. PMID 19257582. S2CID 24357745. arXiv:0809.2607
 . doi:10.1103/PhysRevLett.102.062503.
. doi:10.1103/PhysRevLett.102.062503. - „Atomic Nucleus with Halo: For the First Time, Scientists Measure the Size of a One-Neutron Halo with Lasers”. 2009. „The measurements revealed that the average distance between the halo neutrons and the dense core of the [Be-11] nucleus is 7 femtometers. Thus, the halo neutron is about three times as far from the dense core as is the outermost proton, since the core itself has a radius of only 2.5 femtometers.”
- Marqués, F. M.; Labiche, M.; Orr, N. A.; Angélique, J. C.; Axelsson, L.; Benoit, B.; Bergmann, U. C.; Borge, M. J. G.; Catford, W. N.; Chappell, S. P. G.; Clarke, N. M.; Costa, G.; Curtis, N.; d'Arrigo, A.; De Góes Brennand, E.; De Oliveira Santos, F.; Dorvaux, O.; Fazio, G.; Freer, M.; Fulton, B. R.; Giardina, G.; Grévy, S.; Guillemaud-Mueller, D.; Hanappe, F.; Heusch, B.; Jonson, B.; Le Brun, C.; Leenhardt, S.; Lewitowicz, M.; et al. (2002). „Detection of neutron clusters”. Physical Review C. 65 (4): 044006. Bibcode:2002PhRvC..65d4006M. S2CID 37431352. arXiv:nucl-ex/0111001
 . doi:10.1103/PhysRevC.65.044006.
. doi:10.1103/PhysRevC.65.044006. - Le Roy, Robert J.; N. S. Dattani; J. A. Coxon; A. J. Ross; Patrick Crozet; C. Linton (25. 11. 2009). „Accurate analytic potentials for Li2(X) and Li2(A) from 2 to 90 Angstroms, and the radiative lifetime of Li(2p)”. Journal of Chemical Physics. 131 (20): 204309. Bibcode:2009JChPh.131t4309L. PMID 19947682. doi:10.1063/1.3264688.
- Dattani, N. S.; R. J. Le Roy (8. 5. 2013). „A DPF data analysis yields accurate analytic potentials for Li2(a)and Li2(c) that incorporate 3-state mixing near the c-state asymptote”. Journal of Molecular Spectroscopy. 268 (1–2): 199—210. Bibcode:2011JMoSp.268..199.. S2CID 119266866. arXiv:1101.1361
 . doi:10.1016/j.jms.2011.03.030.
. doi:10.1016/j.jms.2011.03.030. - Semczuk, M.; Li, X.; Gunton, W.; Haw, M.; Dattani, N. S.; Witz, J.; Mills, A. K.; Jones, D. J.; Madison, K. W. (2013). „High-resolution photoassociation spectroscopy of the 6Li2 c-state”. Phys. Rev. A. 87 (5): 052505. Bibcode:2013PhRvA..87e2505S. S2CID 119263860. arXiv:1309.6662
 . doi:10.1103/PhysRevA.87.052505.
. doi:10.1103/PhysRevA.87.052505. - Huang, Yiye; R. J. Le Roy (8. 10. 2003). „Potential energy Lambda double and Born-Oppenheimer breakdown functions for the B1Piu "barrier" state of Li2”. Journal of Chemical Physics. 119 (14): 7398—7416. Bibcode:2003JChPh.119.7398H. doi:10.1063/1.1607313.
- Li, Dan; F. Xie; L. Li; A. Lazoudis; A. M. Lyyra (29. 9. 2007). „New observation of the, 13Δg, and 23Πg states and molecular constants with all 6Li2, 7Li2, and 6Li7Li data”. Journal of Molecular Spectroscopy. 246 (2): 180—186. Bibcode:2007JMoSp.246..180L. doi:10.1016/j.jms.2007.09.008.
- Jastrzebski, W; A. Pashov; P. Kowalczyk (22. 6. 2001). „The E-state of lithium dimer revised”. Journal of Chemical Physics. 114 (24): 10725—10727. Bibcode:2001JChPh.11410725J. doi:10.1063/1.1374927.
- Pashov, A; W. Jastzebski; P. Kowalczyk (22. 10. 2000). „The Li2 F "shelf" state: Accurate potential energy curve based on the inverted perturbation approach”. Journal of Chemical Physics. 113 (16): 6624—6628. Bibcode:2000JChPh.113.6624P. doi:10.1063/1.1311297.
- Tang, Li-Yan; Yan, Zong-Chao; Shi, Ting-Yun; Mitroy, J. (2011). „Third-order perturbation theory for van der Waals interaction coefficients” (PDF). Physical Review A. 84 (5): 052502. Bibcode:2011PhRvA..84e2502T. ISSN 1050-2947. S2CID 122544942. doi:10.1103/PhysRevA.84.052502. Архивирано из оригинала (PDF) 2020-06-25. г.
- Hou, S. Q.; He, J.J.; Parikh, A.; Kahl, D.; Bertulani, C.A.; Kajino, T.; Mathews, G.J.; Zhao, G. (2017). „Non-extensive statistics to the cosmological lithium problem”. The Astrophysical Journal. 834 (2): 165. Bibcode:2017ApJ...834..165H. S2CID 568182. arXiv:1701.04149
 . doi:10.3847/1538-4357/834/2/165
. doi:10.3847/1538-4357/834/2/165  .
. - Tanabashi, M.; Hagiwara, K.; Hikasa, K.; Nakamura, K.; Sumino, Y.; et al. (Particle Data Group) (2018-08-17). „Review of Particle Physics”. Physical Review D. American Physical Society (APS). 98 (3): 030001. Bibcode:2018PhRvD..98c0001T. ISSN 2470-0010. doi:10.1103/physrevd.98.030001
 . hdl:10044/1/68623
. hdl:10044/1/68623  .
. - Boesgaard, A. M.; Steigman, G. (1985). „Big bang nucleosynthesis – Theories and observations”. Annual Review of Astronomy and Astrophysics. Palo Alto, CA. 23: 319—378. Bibcode:1985ARA&A..23..319B. doi:10.1146/annurev.aa.23.090185.001535. A86-14507 04–90.
- Tanabashi, M.; et al. (2018). „Big-bang nucleosynthesis”. Ур.: Fields, B. D.; Molaro, P.; Sarkar, S. The Review (PDF). Physical Review D. 98. стр. 377—382. Bibcode:2018PhRvD..98c0001T. doi:10.1103/PhysRevD.98.030001.
- Langmuir, C. H.; Broecker, W. S. (2012). How to Build a Habitable Planet: The Story of Earth from the Big Bang to Humankind. Princeton University Press. ISBN 978-0691140063.
- Fields, B. D. (2011). „The primordial lithium problem”. Annual Review of Nuclear and Particle Science. 61 (1): 47—68. Bibcode:2011ARNPS..61...47F. arXiv:1203.3551
 . doi:10.1146/annurev-nucl-102010-130445
. doi:10.1146/annurev-nucl-102010-130445  .
. - Stiavelli, M. (2009). From First Light to Reionization the End of the Dark Ages. Weinheim, Germany: Wiley-VCH. стр. 8. Bibcode:2009fflr.book.....S. ISBN 9783527627370.
- Woo, M. (21. 2. 2017). „The Cosmic Explosions That Made the Universe”. earth. BBC. Архивирано из оригинала 21. 2. 2017. г. Приступљено 21. 2. 2017. „A mysterious cosmic factory is producing lithium. Scientists are now getting closer at finding out where it comes from”
- Richard, O.; Michaud, G.; Richer, J. (2005-01-20). „Implications of WMAP Observations on Li Abundance and Stellar Evolution Models”. The Astrophysical Journal (на језику: енглески). 619 (1): 538—548. Bibcode:2005ApJ...619..538R. ISSN 0004-637X. S2CID 14299934. arXiv:astro-ph/0409672
 . doi:10.1086/426470.
. doi:10.1086/426470. - Korn, A. J.; Grundahl, F.; Richard, O.; Barklem, P. S.; Mashonkina, L.; Collet, R.; Piskunov, N.; Gustafsson, B. (август 2006). „A probable stellar solution to the cosmological lithium discrepancy”. Nature (на језику: енглески). 442 (7103): 657—659. Bibcode:2006Natur.442..657K. ISSN 1476-4687. PMID 16900193. S2CID 3943644. arXiv:astro-ph/0608201
 . doi:10.1038/nature05011.
. doi:10.1038/nature05011. - Cain, Fraser. „Brown Dwarf”. Universe Today. Архивирано из оригинала 25. 2. 2011. г. Приступљено 17. 11. 2009.
- „First Detection of Lithium from an Exploding Star”. Архивирано из оригинала 1. 8. 2015. г. Приступљено 29. 7. 2015.
- Reid, N. (10. 3. 2002). „L Dwarf Classification”. Архивирано из оригинала 21. 5. 2013. г. Приступљено 6. 3. 2013.
- Plait, P. (11. 11. 2009). „Want a planet? You might want to avoid lithium”. Discover.
- Israelian, G.; et al. (2009). „Enhanced lithium depletion in Sun-like stars with orbiting planets”. Nature. 462 (7270): 189—191. Bibcode:2009Natur.462..189I. PMID 19907489. S2CID 388656. arXiv:0911.4198
 . doi:10.1038/nature08483.
. doi:10.1038/nature08483. - Baumann, P.; Ramírez, I.; et al. (2010). „Lithium depletion in solar-like stars: no planet connection”. Astronomy and Astrophysics. 519: A87. Bibcode:2010A&A...519A..87B. ISSN 0004-6361. arXiv:1008.0575
 . doi:10.1051/0004-6361/201015137
. doi:10.1051/0004-6361/201015137  .
. - Ramírez, I.; Fish, J. R.; et al. (2012). „Lithium abundances in nearby FGK dwarf and subgiant stars: internal destruction, galactic chemical evolution, and exoplanets”. The Astrophysical Journal. 756 (1): 46. Bibcode:2012ApJ...756...46R. ISSN 0004-637X. S2CID 119199829. arXiv:1207.0499
 . doi:10.1088/0004-637X/756/1/46. hdl:2152/34872
. doi:10.1088/0004-637X/756/1/46. hdl:2152/34872  .
. - Figueira, P.; Faria, J. P.; et al. (2014). „Exoplanet hosts reveal lithium depletion”. Astronomy & Astrophysics. 570: A21. ISSN 0004-6361. arXiv:1409.0890
 . doi:10.1051/0004-6361/201424218
. doi:10.1051/0004-6361/201424218  .
. - Delgado Mena, E.; Israelian, G.; et al. (2014). „Li depletion in solar analogues with exoplanets”. Astronomy & Astrophysics. 562: A92. ISSN 0004-6361. arXiv:1311.6414
 . doi:10.1051/0004-6361/201321493
. doi:10.1051/0004-6361/201321493  .
. - Li, H.; Aoki, W.; Matsuno, T.; Kumar, Y. Bharat; Shi, J.; Suda, T.; Zhao, G.; Zhao, G. (2018). „Enormous Li Enhancement Preceding Red Giant Phases in Low-mass Stars in the Milky Way Halo”. The Astrophysical Journal. 852 (2): L31. Bibcode:2018ApJ...852L..31L. S2CID 54205417. arXiv:1801.00090
 . doi:10.3847/2041-8213/aaa438
. doi:10.3847/2041-8213/aaa438  .
. - Emsley, J. (2001). Nature's Building Blocks. Oxford: Oxford University Press. ISBN 978-0-19-850341-5.
- Hou, S. Q.; He, J. J.; Parikh, A.; Kahl, D.; Bertulani, C. A.; Kajino, T.; Mathews, G. J.; Zhao, G. (2017-01-11). „Non-Extensive Statistics to the Cosmological Lithium Problem”. The Astrophysical Journal. 834 (2): 165. Bibcode:2017ApJ...834..165H. ISSN 1538-4357. S2CID 568182. arXiv:1701.04149
 . doi:10.3847/1538-4357/834/2/165
. doi:10.3847/1538-4357/834/2/165  .
. - Angulo, C.; Casarejos, E.; Couder, M.; Demaret, P.; Leleux, P.; Vanderbist, F.; Coc, A.; Kiener, J.; Tatischeff, V.; Davinson, T.; Murphy, A. S. (септембар 2005). „The 7Be(d,p)2α Cross Section at Big Bang Energies and the Primordial 7Li Abundance”. Astrophysical Journal Letters (на језику: енглески). 630 (2): L105—L108. Bibcode:2005ApJ...630L.105A. ISSN 0004-637X. arXiv:astro-ph/0508454
 . doi:10.1086/491732
. doi:10.1086/491732  .
. - Boyd, Richard N.; Brune, Carl R.; Fuller, George M.; Smith, Christel J. (новембар 2010). „New nuclear physics for big bang nucleosynthesis”. Physical Review D (на језику: енглески). 82 (10): 105005. Bibcode:2010PhRvD..82j5005B. ISSN 1550-7998. S2CID 119265813. arXiv:1008.0848
 . doi:10.1103/PhysRevD.82.105005.
. doi:10.1103/PhysRevD.82.105005. - Hammache, F.; Coc, A.; de Séréville, N.; Stefan, I.; Roussel, P.; Ancelin, S.; Assié, M.; Audouin, L.; Beaumel, D.; Franchoo, S.; Fernandez-Dominguez, B. (децембар 2013). „Search for new resonant states in 10C and 11C and their impact on the cosmological lithium problem”. Physical Review C (на језику: енглески). 88 (6): 062802. Bibcode:2013PhRvC..88f2802H. ISSN 0556-2813. S2CID 119110688. arXiv:1312.0894
 . doi:10.1103/PhysRevC.88.062802.
. doi:10.1103/PhysRevC.88.062802. - O'Malley, P. D.; Bardayan, D. W.; Adekola, A. S.; Ahn, S.; Chae, K. Y.; Cizewski, J. A.; Graves, S.; Howard, M. E.; Jones, K. L.; Kozub, R. L.; Lindhardt, L. (октобар 2011). „Search for a resonant enhancement of the 7Be + d reaction and primordial 7Li abundances”. Physical Review C (на језику: енглески). 84 (4): 042801. Bibcode:2011PhRvC..84d2801O. ISSN 0556-2813. doi:10.1103/PhysRevC.84.042801.
- Collaboration, Atlas (2021). „Search for squarks and gluinos in final states with jets and missing transverse momentum using 139 fb$^{-1}$ of $\sqrt{s}$ =13 TeV $pp$ collision data with the ATLAS detector”. Jhep (на језику: енглески). 02: 143. S2CID 256039464. arXiv:2010.14293
 . doi:10.1007/JHEP02(2021)143.
. doi:10.1007/JHEP02(2021)143. - Sutter, Paul (2021-01-07). „From squarks to gluinos: It's not looking good for supersymmetry”. Space.com (на језику: енглески). Приступљено 2021-10-29.
- Holder, Gilbert P.; Nollett, Kenneth M.; van Engelen, Alexander (јун 2010). „On Possible Variation in the Cosmological Baryon Fraction”. Astrophysical Journal (на језику: енглески). 716 (2): 907—913. Bibcode:2010ApJ...716..907H. ISSN 0004-637X. arXiv:0907.3919
 . doi:10.1088/0004-637X/716/2/907
. doi:10.1088/0004-637X/716/2/907  .
. - Wu, G.; Huang, M. (2006). „Organolithium Reagents in Pharmaceutical Asymmetric Processes”. Chem. Rev. 106 (7): 2596—2616. PMID 16836294. doi:10.1021/cr040694k.
- Eisch, John J. (2002). „Henry Gilman: American Pioneer in the Rise of Organometallic Chemistry in Modern Science and Technology†”. Organometallics. 21 (25): 5439—5463. ISSN 0276-7333. doi:10.1021/om0109408.
- Rappoport, Z.; Marek, I., ур. (2004). The Chemistry of Organolithium Compounds (2 parts). John Wiley & Sons, Ltd. ISBN 978-0-470-84339-0.
- Reich, H. J.; Borst, J. P; Dykstra, R. R.; Green, P. D. (1993). „A nuclear magnetic resonance spectroscopic technique for the characterization of lithium ion pair structures in THF and THF/HMPA solution”. J. Am. Chem. Soc. 115 (19): 8728—8741. doi:10.1021/ja00072a028.
Спољашње везе
[уреди | уреди извор]- International Lithium Alliance
- McKinsey review of 2018 Архивирано 16 новембар 2020 на сајту Wayback Machine (PDF)
- Lithium Архивирано 16 јул 2016 на сајту Wayback Machine at The Periodic Table of Videos (University of Nottingham)
- USGS: Lithium Statistics and Information Архивирано 29 јул 2018 на сајту Wayback Machine
- Lithium Supply & Markets 2009 IM Conference 2009 Sustainable lithium supplies through 2020 in the face of sustainable market growth Архивирано 4 јун 2016 на сајту Wayback Machine
- University of Southampton, Mountbatten Centre for International Studies, Nuclear History Working Paper No5. (PDF) (archived February 26 February 2008)
- Lithium preserves by Country Архивирано 20 октобар 2022 на сајту Wayback Machine at investingnews.com
- Alastair Gunn (16. 6. 2023). „The lithium problem: Why the element keeps disappearing”. BBC Science Focus Magazine. Приступљено 17. 6. 2023.












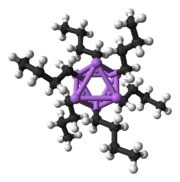


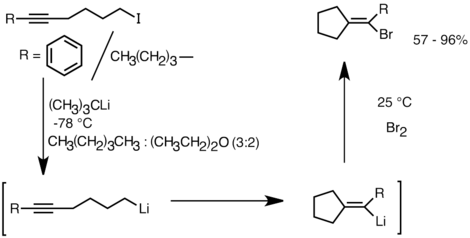
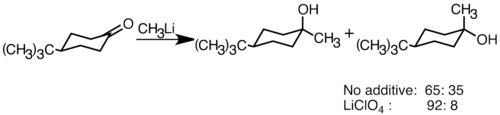
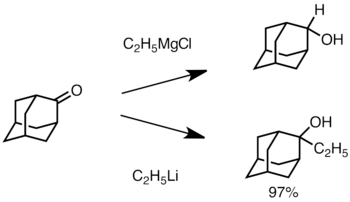













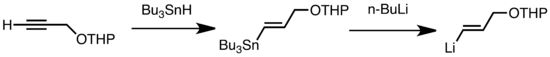







![{\displaystyle \mathrm {Li^{+}+\mathrm {e} ^{-}\ {\xrightarrow[{elektroliza}]{352\,^{\circ }C}}\ Li} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9c4f392667eae5fea5bd062050b0b8883488c53c)
![{\displaystyle \mathrm {KCl+LiCl\ {\xrightarrow[{elektroliza}]{352\,^{\circ }C}}\ K+Li+Cl_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/cacbb963ddc07c91454983764f2376c1e594a01e)
